El término calcifilaxis o la expresión arteriolopatía urémica calcificante (AUC) definen la calcificación sistémica de la media de las arteriolas que da lugar a isquemia y a necrosis subcutánea. La calcifilaxis se asocia con la enfermedad renal crónica (ERC) y con el trasplante renal. Las formas de tratar esta entidad se basan en anular factores implicados en su aparición, tratar el componente inflamatorio y los depósitos de calcio, curas intensivas de las úlceras (en este apartado incluimos: el sistema Vacuum Assisted Closure [VAC] y la cámara hiperbárica) y tratamiento de los episodios infecciosos en las lesiones. También es importante el tratamiento del dolor y mantener un buen estado nutricional.
De acuerdo con las recientes publicaciones, el uso intensivo y combinado de medidas terapéuticas ofrece mejores resultados.
Durante un extenso período de tiempo aplicamos una combinación de tratamientos a una paciente con calcifilaxis distal. Las lesiones comenzaron a los 20 años de haber sido sometida a un trasplante con nefropatía crónica del injerto y ERC estadio 3. Tanto la ERC como las lesiones progresaron, iniciando hemodiálisis y los tratamientos combinados de la calcifilaxis.
Los buenos resultados alcanzados nos permiten afirmar que el uso de tratamientos combinados puede ser efectivo en pacientes con AUC.
INTRODUCCIÓN
La calcifilaxis o arteriolopatía urémica calcificante (AUC) se caracteriza por la calcificación de la media de las arteriolas, que da lugar a lesiones dolorosas en la piel, que consisten en nódulos subcutáneos que progresan a isquemia y necrosis con formación de úlceras.
La histología es específica y se caracteriza por depósitos de calcio en la media de pequeñas arterias de la piel con hiperplasia intimal y trombosis luminal1.
La mortalidad es alta por las complicaciones derivadas de la infección de las lesiones, y es diferente según la localización: las lesiones dístales tienen una mortalidad de un 32% y las proximales de un 63%.
La patogenia es compleja; se barajan diversos mecanismos en la aparición de esta entidad, en la que puede intervenir un medio adecuado para su desarrollo, como es el medio urémico, aunque también se ha descrito en pacientes con función renal normal2.
Se ha relacionado con hiperparatiroidismo, hiperfosforemia, tratamientos que producen hipercalcemia, como la vitamina D (calcitriol), y los quelantes del fósforo que aportan calcio. También con la deficiencia de inhibidores de la calcificación vascular como la fetuína A y la proteína GIa, con la obesidad, con el sexo femenino, con la diabetes, con la hipoalbuminemia y con estados de hipercoagulabilidad por deficiencia de proteínas C y S o con anticoagulantes orales tipo cumarínicos3.
En la actualidad, el tratamiento de la calcifilaxis se basa en: 1) la eliminación de factores implicados en su aparición y desarrollo; 2) el tratamiento del componente inflamatorio de las lesiones y los depósitos de calcio; 3) las curas intensivas de las úlceras, utilizando el sistema Vacuum Assisted Closure (VAC)4,5 y la cámara hiperbárica6,7; 4) tratamiento de los episodios infecciosos de las lesiones, y 5) tratamiento del dolor y el mantenimiento de un buen estado nutricional.
De acuerdo con las recientes publicaciones, la aplicación de medidas terapéuticas de forma combinada ofrece mejores resultados8,9.
Presentamos el caso de una paciente que había sido sometida a trasplante renal hacía 20 años, con nefropatía crónica del injerto y ERC estadio 3. En esta situación clínica, comienza a desarrollar las lesiones de calcifilaxis distal. Entre la aparición de las primeras lesiones y el comienzo de la diálisis trascurrieron 3 años. Las lesiones siguieron un curso tórpido, con aumento del tamaño y del número. Al inicio de la diálisis iniciamos diversos tratamientos de forma combinada, que a continuación se detallan.
CASO CLÍNICO
Mujer de 53 años de edad con ERC secundaria a glomerulonefritis IgA, HTA y cardiopatía hipertensiva. Inició hemodiálisis en el año 1984 y fue sometida a trasplante de riñón de cadáver en el año 1985. En el año 2005, ya sometida a trasplante y con ERC estadio 3 por nefropatía crónica del injerto, se inició tratamiento con anticoagulación con sintrom por fibrilación auricular; desde entonces refería la aparición de dos nódulos en miembro inferior derecho (MID), dolorosos, que progresaron hacia ulceración y necrosis.
Fue atendida en el servicio de dermatología de otro hospital, donde se le realizaron dos biopsias de las lesiones. El diagnóstico anatomopatológico fue compatible con calcifilaxis.
Desde el año 2007 fue seguida en nuestro hospital en la consulta de prediálisis por ERC estadio 4-5. Los datos bioquímicos se exponen a continuación (tabla 1).
Seguía tratamiento con aziatropina 50 mg y prednisona 10 mg/día, hipotensores en número de dos o tres, quelantes del fósforo (hidróxido de aluminio), calcitriol oral 2,5 microg/semana y anticoagulación con sintrom. Las úlceras del MID aumentaron en número y tamaño a pesar de las curas locales y aparecieron otras dos pequeñas úlceras superficiales en el miembro inferior izquierdo (MII).
En junio de 2008 inició de nuevo diálisis. En la exploración física: el índice de masa corporal era de 23 kg/m2, la TA de 140/80 mmHg, la auscultación cardíiaca era arrítmica, con frecuencia ventricular controlada, y a la palpación de miembros inferiores se evidenciaban múltiples nódulos de pequeño tamaño relacionados con depósitos de calcio.
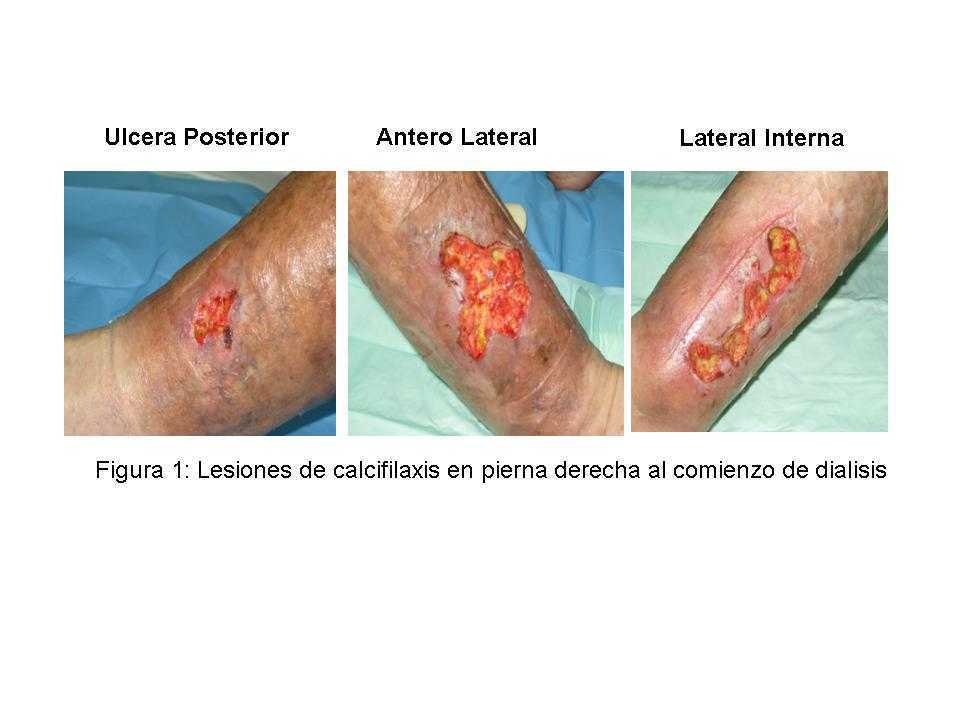
Las lesiones de calcifilaxis en el MID al comenzar diálisis se exponen en la figura 1. Observamos 3 úlceras extensas, con bordes irregulares y fondo necrótico con localización anterolateral, lateral interna y posterior. En el MII, las lesiones eran 3 úlceras puntiformes y superficiales.
Los parámetros bioquímicos al inicio de diálisis se exponen a continuación (tabla 1).
En la radiografía simple de ambos miembros inferiores aparecían calcificaciones vasculares y en partes blandas.
Medidas terapéuticas aplicadas y evolución
Supresión de posibles factores implicados en su aparición
La anticoagulación oral con sintrom fue suspendida y en su lugar se inició tratamiento con antiagregantes plaquetarios.
La vitamina D (calcitriol) también fue suspendida y los niveles de fósforo se controlaron con sevelamer e hidróxido de aluminio.
La PTH se mantuvo alrededor de 150-200 pg/ml con calcimiméticos, siendo la dosis necesaria de 30 mg en días alternos o 5 días a la semana.
Las sesiones de diálisis se intensificaron: en los primeros 2 meses las sesiones fueron diarias, con un dializador de alta permeabilidad con técnica de hemodialfiltracion on-line y calcio en el baño de diálisis de 3,5 mEq/l.
Tratamiento de los depósitos de calcio y del componente inflamatorio
Utilizamos bifosfonatos para inhibir las calcificaciones ectópicas y por su efecto antiinflamatorio. Inicialmente la paciente fue tratada con pamidronato intravenoso a dosis de 30 mg después de la hemodiálisis durante 5 días y luego continuamos con risedronato oral a dosis de 35 mg a la semana.
Tratamos con tiosulfato sódico al 25% intravenoso, 25 g después de la hemodiálisis durante cinco sesiones de hemodiálisis en días alternos; la dosis se redujo a 12,5 g por la aparición de vómitos y acidosis metabólica. Ante la persistencia de estos síntomas se suspendió el tratamiento a los 15 días del inicio. Durante el tratamiento con tiosulfato el calcio en el baño de diálisis fue de 3 mEq/l.
Para el componente inflamatorio de las lesiones también tratamos con pentoxifilina, 600 mg/12 horas.
Curas de las úlceras
Las curas eran realizadas por el equipo de enfermería de la unidad de diálisis. Se hacían tres veces a la semana después de la hemodiálisis, bajo tratamiento con cloruro mórfico subcutáneo. Previa limpieza con suero fisiológico de esfacelos y tejidos necrótico, se aplicaba en cada una de las úlceras Purilon Gel para desbridamiento autolítico, aplicando a continuación los parches de Biatain-Ibu.
Las úlceras en el MII se curaron en los primeros 5 meses y las de MID no progresaban pero no experimentaban mejoría, y eran extensas, profundas y dolorosas.
En diciembre del 2008 se comenzó el tratamiento con el sistema de cierre al vacío VAC. Éste se implantó en las 3 úlceras de la pierna derecha; en ese momento las úlceras no estaban infectadas. Por la localización de éstas, la implantación fue complicada e incómoda para la paciente. El VAC se mantuvo durante 7 días, con cambios de los parches VAC cada 48 horas de forma ambulatoria.
Al séptimo día de su implantación la paciente presentó fiebre y dolor intenso en las úlceras lateral interna y anterolateral, con una intensa reacción inflamatoria perilesional que obligó a la retirada del VAC; no obstante, se observaron la limpieza de las úlceras y la disminución del tamaño y de la profundidad de la úlcera posterior.
Las curas se continuaron realizando con Purilon Gel y los parches de Biatain-Ibu, cada 48 horas.
En enero de 2009, tras suspender el VAC, comenzamos el tratamiento con la cámara hiperbárica. Este tratamiento consiste en respirar a una concentración de oxigeno al 100% durante 60 minutos. Se realizó de forma continuada de lunes a viernes hasta junio de 2009*.
Tratamiento de los episodios infecciosos
Durante todo el proceso los episodios infecciosos fueron cinco, todos en las úlceras anterolateral y lateral interna de la pierna derecha. Siempre se acompañaron de aumento del dolor y de la proteína C reactiva (PCR), a veces con fiebre y con hemocultivos negativos.
Los gérmenes obtenidos en el exudado de las úlceras durante los cinco episodios fueron: Staphylococcus aureus y Eschericha coli en dos, S. epidermidis en uno, Candida, glabrata y parapsilosis en otro, y en el quinto se aislaron enterococo y E. coli multirresistente portador de betalactamasa plasmídica, que obligó al aislamiento de contacto durante la sesiones de hemodiálisis, hasta la desaparición de la infección.
Los episodios infecciosos fueron tratados con antibióticos por vía sistémica según antibiograma de forma prolongada y las micosis fueron tratadas con fluconazol oral.
Para el control del dolor utilizamos parches de fentanilo transdérmico a dosis de 2,5 mg cada 72 horas en los primeros meses, posteriormente, las necesidades fueron disminuyendo hasta la suspensión.
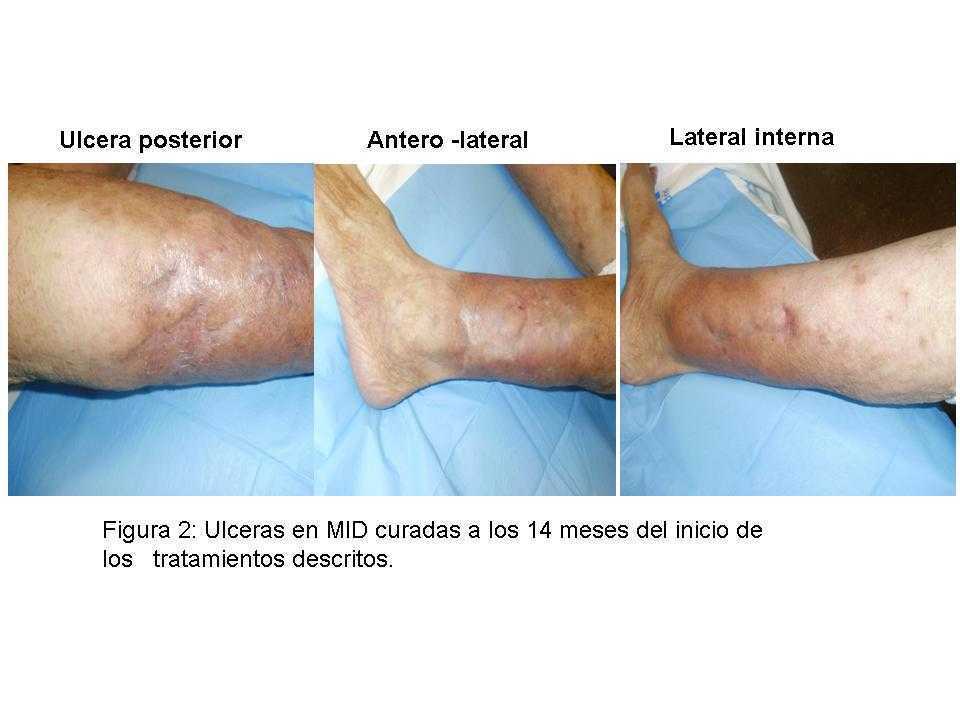
Las úlceras fueron mejorando progresivamente, hasta la curación total en agosto de 2009 (figura 2).
DISCUSIÓN
En este caso, los factores de riesgo para el desarrollo de la calcifilaxis fueron: sexo femenino, ERC, trasplante renal y tratamientos con sintrom y calcitriol.
Después de 3 años de aparición de las primeras lesiones, éstas siguieron un curso tórpido y la ERC evolucionó a un estadio 5, comenzando hemodiálisis y las medidas terapéuticas descritas.
La aparición de las primeras lesiones se produjo coincidiendo con el inicio del tratamiento con sintrom. Se ha descrito un aumento de calcificaciones valvulares y de arterias coronarias en pacientes tratados con cumarínicos. Los anticoagulantes disminuyen la síntesis y la función de la matriz proteica G1a; esta proteína, sintetizada en los vasos sanguíneos, inhibe las calcificaciones vasculares10,11.
Al inicio de diálisis, suspendimos el tratamiento con aziatropina y disminuimos la prednisona a 5 mg/día, que mantuvimos durante todo el proceso. Es objeto de discusión el uso de esteroides en el tratamiento de la calcifilaxis, ya que pueden desempeñar un papel beneficioso por su efecto antiinflamatorio, pero también pueden favorecer los procesos infecciosos.
Con la idea de mantener un medio urémico adecuado y un nivel óptimo de fósforo intensificamos el tratamiento dialítico, en el número de sesiones y con la técnica de hemodialfiltración on-line.
Para el control del fósforo, los quelantes que utilizamos fueron hidróxido de aluminio y sevelamer, que no aportan calcio. El sevelamer12,13 también reduce el colesterol y aumenta la fetuína A, que inhibe las calcificaciones ectópicas. El déficit de esta glucoproteína se ha relacionado con un estado inflamatorio y con el desarrollo de calcificaciones cardiovasculares14.
Se suspendió el tratamiento con vitamina D (calcitriol), ya que puede contribuir al desarrollo de calcifilaxis por su efecto vascular directo y por la hipercalcemia e hiperfosforemia que puede producir y que puede dar lugar a depósitos de calcio intravascular en arteriolas y vénulas, así como en la piel y en el tejido adiposo.
Los niveles aumentados de PTH se han relacionado con calcificaciones vasculares y lesiones de calcifilaxis. En nuestra paciente, las cifras de PTH nunca fueron elevadas y desde el inicio de hemodiálisis la PTH se controló con dosis bajas de calcimiméticos9. En el esquema terapéutico clásico, el aumento de PTH y las lesiones de calcifilaxis obligaban a la paratiroidectomía quirúrgica. Hoy día, la disponibilidad terapéutica de los calcimiméticos nos permite, en muchos casos, controlar las cifras de PTH, de calcio y de fósforo sin necesidad de realizar una paratiroidectomía quirúrgica.
Se han descrito casos de calcifilaxis con los niveles PTH no elevados2 y también después de paratiroidectomías quirúrgicas15. El bajo recambio (turnover) óseo también es un riesgo para producir calcificaciones vasculares y, entre ellas, las calcificaciones de la calcifilaxis.
Los bifosfonatos están contraindicado en los estadios 4 y 5 de la ERC por su nefrotoxicidad, pero su uso está admitido en la calcifilaxis porque inhibe la formación de calcificaciones ectópicas y por su efecto antiinflamatorio, inhibiendo la actividad de macrófagos y la producción de citokinas proinflamatorias vasculares16,17. Se han usado con éxito el pamidronato18,19 y el etidronato20. Nosotros tratamos en un primer lugar con pamidronato intravenoso, según pauta descrita18 y seguimos con risedronato oral semanal21,22, siempre teniendo en cuenta la reducción del turnover óseo producido por los bifosfonatos.
Con la finalidad de disminuir las calcificaciones vasculares, tratamos con tiosulfato sódico23,24; éste moviliza el calcio depositado en los pequeños vasos y también tiene un efecto antiinflamatorio. La aparición de efectos secundarios nos obligó a suspender el tratamiento.
El componente inflamatorio vascular de la calcifilaxis puede mejorar con pentoxifilina (inhibidor de fosfodiesterasa), al reducir la expresión de células T, de TNF-alfa y de IFN-gamma25,26; a este efecto se sumaría el aumento del flujo sanguíneo en las úlceras, que ayuda a su cicatrización.
Las curas se realizaban bajo analgesia; en cada una de las úlceras se aplicaban Purilon y los parches de Biatain-Ibu para mantener el medio húmedo favoreciendo la cicatrización; el contenido en ibuprofeno disminuye el dolor27.
A los 7 meses de evolución no aparecieron nuevas úlceras, pero las 3 úlceras de la pierna derecha no disminuían de tamaño ni de profundidad; por ello iniciamos el tratamiento con el sistema VAC. Éste consiste en la aplicación de apósitos VAC, hidrófobos, no adherentes, adaptados al tamaño de las úlceras, que quedan sellados con un material adhesivo en las lesiones y conectados a un tubo no colapsable que termina en un pequeño contenedor. La aplicación, a través de una bomba portátil, de una presión subatmosférica de 120 mmHg, produce succión, que da lugar a limpieza de las úlceras y disminución de la carga bacteriana, con aumento del tejido de granulación, que acelera la cicatrización de las úlceras.
El VAC se ha empleado con éxito en el tratamiento de úlceras de distinta naturaleza: isquémicas, traumáticas, inflamatorias4 y relacionadas con calcifilaxis5.
Con el VAC, se observó la limpieza de las úlceras, con una recogida de material necrótico en el contenedor y con formación de nuevo tejido de granulación, sobre todo en la úlcera posterior, que disminuyó de tamaño y de profundidad, pero las úlceras anterolateral y lateral interna presentaron una intensa reacción inflamatoria perilesional con aumento del dolor que nos obligó a la suspensión del VAC.
Al suspender el VAC, iniciamos el tratamiento con la cámara hiperbárica. Con este tratamiento aumentamos el oxígeno en los tejidos dañados, promoviendo la proliferación de fibroblastos con producción de colágeno y angiogénesis que ayuda a la formación de tejido de granulación y a la curación de las úlceras6-8.
En la evolución del proceso es importante el tratamiento de los episodios infecciosos de las úlceras. Con la toma de muestras del exudado de las úlceras identificamos los gérmenes causales y el tratamiento antibiótico pudo ser el más adecuado.
Todas las medidas terapéuticas fueron aplicadas de forma simultánea, con mejoría progresiva hasta la curación total en agosto de 2009 (figura 2), lo que corrobora lo descrito por otros autores en relación con la necesidad de los tratamientos combinados en la calcifilaxis8,9.
En la evolución con éxito del caso es de destacar la implicación de la enfermería de la unidad de diálisis en las curas de las úlceras y la actitud de colaboración de la paciente ante un proceso lento y doloroso, con tratamientos que se prolongan en el tiempo.
En la actualidad la paciente continúa en hemodiáfiltración, sin lesiones y con disminución de los nódulos en relación con los depósitos de calcio. Somos conscientes de que las calcificaciones vasculares de la calcifilaxis pueden existir sin aparición de las úlceras28; por ello, seguimos controlando el metabolismo mineral y el medio urémico, sin administrar anticoagulantes orales ni calcitriol, continuamos el tratamiento con pentoxifilina y se han suspendido el risedronato y el cinacalcet por cifras de PTH disminuidas.
*El tratamiento con la cámara hiperbárica fue financiado por el sistema de salud de la Comunidad de Madrid. Se realizó en la Clínica Censalud (Zapata, 3. 28002 Madrid), bajo la supervisión médica del Dr. Ramón Morales Frías.
Figura 1. Lesiones de calcifilaxis en la pierna derecha al comienzo de la diálisis.
Figura 2. Úlceras en miembro inferior derecho curadas a las 14 meses del inicio de los tratamientos descritos.
10502_18107_9989_es_10502_15858_6153_es_tabla_11.doc
Tabla 1. Datos bioquímicos