Revisión del artículo: Kawamvra T, Yoshimura M, Miyazaki Y, Okamoto H, Kimura K, Hirano K, et al. A multicenter randomized controlled trial of tonsillectomy combined with steroid pulse therapy in patients with immunoglobulin A nephropathy. Nephrol Dial Transplant 2014;29:1546-53.
¿Tipo de diseño y seguimiento
Estudio prospectivo, controlado, aleatorizado, multicéntrico, para comparar la eficacia y seguridad de dos pautas de tratamiento en la nefropatía IgA: amigdalectomía asociada a esteroides frente a esteroides.
¿Asignación
Asignación no estratificada por centro, realizada centralmente por ordenador.
¿Enmascaramiento
Estudio abierto para pacientes y médicos.
¿Ámbito
Dieciocho centros de nefrología de Japón.
¿Pacientes
Ochenta enfermos con edades comprendidas entre 18 y 69 años, afectos de nefropatía IgA idiopática diagnosticada por biopsia renal, creatinina < 1,5 mg/dl, proteinuria entre 1 y 3,5 g/día, diversos grados de lesión renal en la biopsia renal y cifras de presión arterial sistólica < 140 mmHg y diastólica < 90 mmHg. Se excluyó a los enfermos con creatinina > 1,5 mg/dl, a los previamente tratados con glucocorticoides y/o inmunosupresores, y a los que presentaban contraindicación para anestesia general o para amigdalectomía.
¿Intervenciones
Grupo A: se realizó amigdalectomía y posteriormente recibieron 0,5 g/día de metilprednisolona por vía intravenosa durante tres días consecutivos en la primera y la tercera semana, y posteriormente el segundo y el cuarto mes; además, prednisolona oral en una dosis de 0,5 mg/kg cada dos días durante seis meses.
Grupo B: se les administraron las mismas dosis y pauta de glucorticoides, pero no se realizó amigdalectomía.
El seguimiento total fue de 12 meses.
El análisis estadístico fue por intención de tratar.
¿Variables de resultado
Los criterios principales de valoración fueron la disminución porcentual en la excreción urinaria de proteínas a partir de los valores basales y la frecuencia de desaparición de la proteinuria y/o hematuria 12 meses tras el inicio del tratamiento. Los criterios de valoración secundarios fueron los cambios en el filtrado glomerular estimado (FGe) en relación con los valores basales, el porcentaje de enfermos con aumento del 100 % en la creatinina sérica sobre los valores basales o disminución del FGe del 50 % en relación con los valores basales, la frecuencia de indicación de tratamiento sustitutivo de la función renal y los efectos adversos.
¿Tamaño muestral
Calculado sobre la estimación de una frecuencia de remisión de la proteinuria a los 12 meses del 40 % en los enfermos tratados con amigdalectomía y glucocorticoides, y del 10 % en los tratados con glucocorticoides, con un poder estadístico del 80 % y un error α del 0,05. El tamaño muestral estimado fue de 38 enfermos por grupo y se incluyeron 40 para compensar por los enfermos no evaluables.
¿Patrocinio
Financiado con fondos procedentes del Grant-in-Aid for Progressive Renal Diseases Research (Research on Intractable Disease) from the Ministry of Health, Labour and Welfare of Japan.
¿ RESULTADOS PRINCIPALES
Análisis basal de los grupos
No se observaron diferencias basales entre los grupos en relación con la edad, el sexo, variables clínicas, bioquímicas o anatomopatológicas.
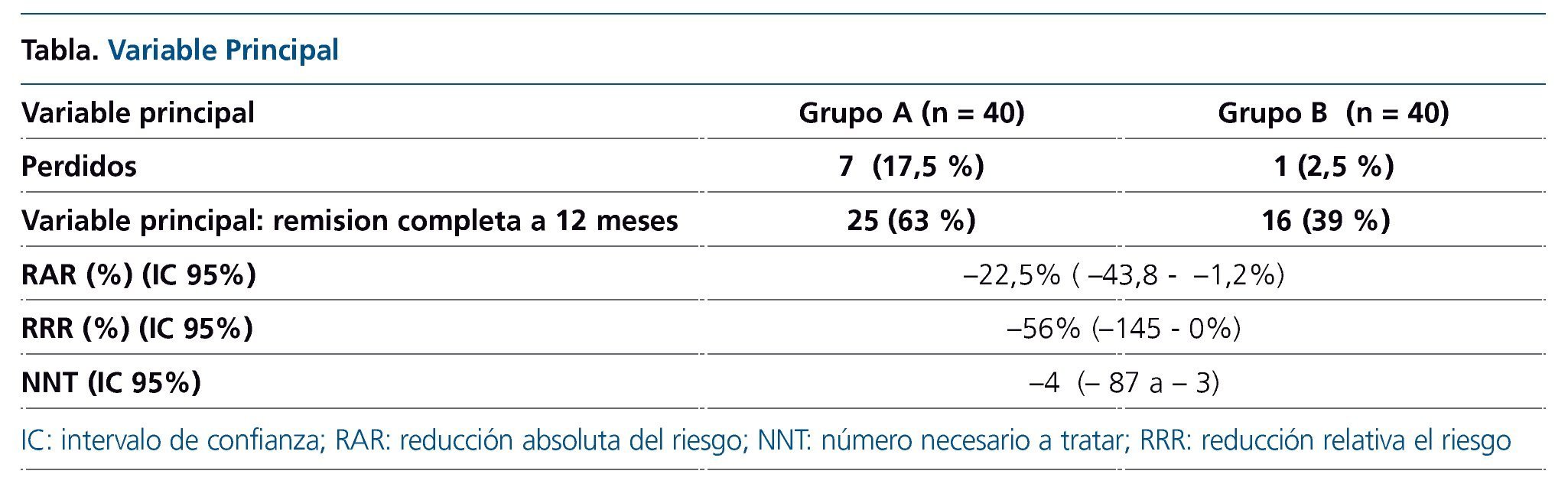
Se incluyeron 40 enfermos en cada grupo. En el grupo A hubo 7 pérdidas, 3 por no cumplir los criterios de inclusión y 4 por retirada del consentimiento informado. En el grupo B, hubo 1 pérdida por retirada del consentimiento. El número de pacientes evaluables fue de 33 en el grupo A y de 39 en el grupo B.
Variables principales
La disminución porcentual en la excreción urinaria de proteínas durante los 12 meses de seguimiento fue significativamente superior en el grupo A que en el B (–1,316, intervalo de confianza [IC] al 95 % –2,617 - –0,015, P = 0,047).
El porcentaje de pacientes en los que la proteinuria se redujo a valores inferiores a 0,3 g/día fue significativamente mayor en el grupo A que en el B a los 10 meses (P = 0,029), pero no a los 12 meses (grupo A: 63 %; grupo B: 39 %; p = 0,052). No hubo diferencias en cuanto a la remisión clínica ni de la hematuria entre ambos grupos.
Variables secundarias
La función renal se mantuvo estable y no se apreciaron diferencias entre ambos grupos en ninguna de las medidas de resultado relacionadas con ella.
Efectos secundarios
No se especifican.
¿ CONCLUSIONES DE LOS AUTORES
La amigdalectomía asociada a tratamiento con glucocorticoides no tiene ningún efecto beneficioso en comparación con los glucocorticoides aislados sobre la remisión de la hematuria o la incidencia de remisión clínica. El efecto antiproteinúrico fue significativamente mayor con el tratamiento combinado, pero la diferencia fue marginal. Su impacto sobre la función renal queda por definir.
¿ COMENTARIOS
Se trata de un ensayo clínico multicéntrico, con diseño inicialmente adecuado, en el que se evalúa la hipótesis de superioridad de amigdalectomía asociada a esteroides frente a esteroides en la remisión de la proteinuria en enfermos con nefropatía IgA con función renal normal y diversos grados anatomopatológicos de lesión renal. Desde un punto de vista metodológico, hay que destacar los siguientes aspectos: en la selección de los enfermos, llama la atención que los autores han seguido criterios distintos a los aconsejados en las guías de práctica clínica, ya que menos del 50 % de los incluidos seguían tratamiento con bloqueantes de la angiotensina II en el momento de su inclusión. Por otra parte, durante el seguimiento, iniciaron tratamiento con bloqueantes de la angiotensina II un total de 7 enfermos, 3 en el grupo A y 4 en el B, lo que supone casi un 9 % del total de los pacientes reclutados. Por ello, parte del efecto antiproteinúrico observado podría no ser debido a las intervenciones evaluadas en el estudio, sino al efecto del bloqueo de la angiotensina II. Por razones obvias, ligadas al tipo de intervención realizada (amigdalectomía), el estudio no es ciego ni para los investigadores ni para los evaluadores. Se describen pérdidas de seguimiento justificadas, pero estas afectan de forma desigual a ambos grupos de tratamiento (17,5 % en el grupo A frente a 2,5 % en el grupo B), por lo que podría haber un sesgo diferencial entre ambos. Como consecuencia de las pérdidas, el número final de enfermos evaluables es distinto en cada grupo (33 en el grupo A y 39 en el grupo B). Además, hay una pérdida de datos a lo largo del período de observación, ya que el número de enfermos con determinaciones válidas es distinto en cada control y, en el control final a los 12 meses, solo se dispone de datos de 32 enfermos del grupo A y de 36 del B. Esta cifra representa el total de enfermos evaluables para la variable principal y contabiliza un total de 68 de los 80 pacientes inicialmente reclutados, lo que representa una pérdida del 15 % de la muestra inicial. Las pérdidas no debidas a no cumplimiento de los criterios de inclusión o a retirada del consentimiento no están debidamente justificadas y, por ello, no se explica por qué razón solo se dispone de proteinuria a los 12 meses en 32 enfermos del grupo A y en 36 del grupo B. En las medidas de definición de los desenlaces (o medidas de resultado), la reducción porcentual de la proteinuria a lo largo del período de observación es una medida cuantitativa que parece adecuada, ya que ambos grupos parten de proteinurias iniciales similares. Sin embargo, llama la atención que, como medida de remisión, se defina el porcentaje de enfermos con proteinuria < 0,3 g/día a las 12 meses, en lugar de utilizar una medida de incidencia como la tasa de remisión, y que en el análisis multivariado, en consecuencia, se utilice la regresión logística en lugar de la regresión de Cox. La regresión logística permite estimar probabilidades, mientras que la regresión de Cox proporcionaría datos comparativos sobre el tiempo (rapidez) de la respuesta.
Los autores indican que el análisis de los datos se realiza por intención de tratar. En consecuencia, cada paciente es analizado en el grupo al que ha sido asignado inicialmente, independientemente de que cumpliera o no con la intervención que se analiza. De hecho, en el grupo A, 1 no fue sometido a amigdalectomía, y en el B, 2 sí lo fueron. Los autores, sin embargo, proporcionan tan solo prevalencias de la variable principal a los 10 y 12 meses, pero no las cifras absolutas, por lo que resulta muy difícil saber sobre qué número total de enfermos se calcularon las prevalencias. Si se rehacen los cálculos, no obstante, se obtiene el mismo resultado tanto si se realizan sobre la muestra inicial de 40 enfermos (p: 0,07) como si se realizan sobre el conjunto de los 68 con proteinuria evaluable a los 12 meses (p: 0,09). En ambos casos, las diferencias entre grupos en el número de personas con remisión de la proteinuria a los 12 meses no son estadísticamente significativas. Un aspecto importante para interpretar la aplicabilidad clínica de los resultados es la definición del criterio de remisión. Los autores fijan la remisión en niveles de proteinuria inferiores a 0,3 g/ día. Esta definición es coherente con un criterio académico de remisión y permite tener una idea del porcentaje de enfermos en los que la proteinuria desaparece. Sin embargo, es poco relevante desde el punto de vista pronóstico, ya que los datos disponibles indican que en la nefropatía IgA proteinurias inferiores a 1 g/día se asocian a un buen pronóstico a largo plazo, especialmente si los enfermos reciben tratamiento con bloqueantes de la angiotensina II. Dado que entre los dos grupos se apreciaron diferencias significativas en la reducción relativa de la proteinuria y que ambos partían de proteinurias similares, las diferencias en la evolución de la proteinuria deberían ser evidentes también en cifras de reducción absoluta. Una medida lógica de análisis de resultados hubiera sido analizar si, entre ambos tratamientos, hubo diferencias en el porcentaje de enfermos con proteinurias superiores a 500 mg/día o a 1000 mg/día. Ambas medidas podrían tener un significado pronóstico más claro que la utilizada.
En relación con el tratamiento con bloqueantes de la angiotensina II, debe destacarse que en el estudio la indicación de tratamiento con esteroides con o sin amigdalectomía se realizó con un criterio distinto al contemplado en las distintas guías de práctica clínica publicadas. En todas ellas, se aconseja la terapia con esteroides solo en los enfermos con proteinuria persistente a pesar del bloqueo de la angiotensina II. Desde un punto de vista formal, hubiera sido deseable que en los criterios de inclusión se contemplara la indicación de los tratamientos analizados solo en los pacientes que presentaran proteinuria a pesar del bloqueo adecuado de la angiotensina II. Como alternativa, hubiera sido deseable que, en los resultados, se analizara si el efecto antiproteinúrico de los esteroides y de la amigdalectomía fue distinto en enfermos tratados y no tratados con bloqueo de la angiotensina II.
Finalmente, hay que destacar que el período de seguimiento fue corto. En el curso clínico de la nefropatía IgA, que se caracteriza por la presencia de brotes recurrentes y por la necesidad de seguimientos muy prolongados para identificar las variables predictoras del pronóstico, 12 meses de evolución suponen un seguimiento excesivamente corto e insuficiente para analizar medidas de desenlace relacionadas con la evolución de la función renal. Las conclusiones sobre el efecto del tratamiento sobre la evolución de la función renal son válidas solo para el período de observación, durante el cual, como era de esperar, no se apreciaron cambios significativos. Los autores plantean el análisis del efecto del tratamiento sobre la evolución de la función renal como un objetivo secundario. Sin embargo, debe destacarse que, por el diseño, tiempo de seguimiento, función renal inicial y tamaño muestral, el estudio carece de poder estadístico para analizar adecuadamente esta medida de desenlace. No debería interpretarse que el significado clínico de la reducción de la proteinuria es incierto. Simplemente debería clarificarse que la interpretación del significado de la reducción de la proteinuria sobre el pronóstico de la función renal queda fuera de los objetivos del estudio y, por ello, no es posible llegar a ninguna conclusión acerca de este aspecto.
¿ CONCLUSIONES DEL REVISOR
En enfermos con nefropatía IgA que presentan proteinuria superior a 1 g/día, la amigdalectomía asociada a tratamiento con glucocorticoides se relaciona con una mayor reducción de la proteinuria durante el período de observación de 12 meses que el tratamiento con glucocorticoides, pero no con una mayor frecuencia de remisión completa ni de remisión clínica. El diseño del estudio contempla un tiempo de seguimiento y un tamaño muestral insuficientes para analizar de manera adecuada la influencia de ambos tratamientos sobre la evolución de la función renal.
¿NOTA METODOLÓGICA
Hay dos aspectos del diseño del estudio y del análisis de los resultados que, en mi opinión, merecen un comentario. El primero se refiere al tipo de análisis de resultados utilizado. Las formas más habituales de analizar los resultados de un ensayo clínico aleatorizado son tres: el análisis por intención de tratar, el análisis de casos válidos o por protocolo y el análisis del «peor de los casos». En el análisis por casos válidos o «por protocolo», solo se incluye a los participantes en los que se ha podido medir la variable de respuesta y que, además, han cumplido adecuadamente la intervención que les fue asignada. Al excluir pacientes del análisis, puede suceder que los grupos que terminan los tratamientos asignados de manera adecuada ya no sean equiparables en cuanto a la distribución de las variables iniciales, sobre todo si el número de exclusiones es elevado. Además, excluir pacientes del análisis de los resultados disminuye el tamaño muestral, lo que conlleva riesgo de disminución de la potencia del estudio. El análisis en función «del peor de los casos» puede ser útil en los estudios en los que se ha producido pérdida de sujetos en los cuales, además, no ha podido determinarse la variable de respuesta. Las pérdidas pueden ser fuente de sesgos si tienen relación con la intervención objeto de estudio o si se producen de forma diferencial en ambos grupos de estudio. El análisis por intención de tratar es el que se ha empleado en el presente estudio. En él, cada paciente es analizado en el grupo al que ha sido asignado inicialmente, independientemente de que no haya cumplido con la intervención que se analiza. Sus ventajas son:
1. La conservación de las consecuencias de la asignación aleatoria de los sujetos de estudio. Por ello, los grupos son comparables en todas las variables excepto en el factor de intervención que es objetivo del estudio. Los potenciales factores de confusión se distribuyen de manera equilibrada entre ambos grupos. De este modo, su efecto de confusión queda anulado o mitigado.
2. Es el tipo de análisis que más se asemeja a la realidad de la práctica clínica diaria, ya que contempla el hecho de que con frecuencia los pacientes no cumplen de manera íntegra el tratamiento que les ha sido prescrito o bien simplemente lo rechazan. Al incluir a los pacientes en los que, a pesar de ser no cumplidores, se ha podido medir la variable de respuesta, permite una mayor aproximación a la práctica médica habitual.
El segundo aspecto que considerar se refiere a las medidas de resultado utilizadas. En un ensayo clínico en el que se dispone del seguimiento prospectivo de dos cohortes de enfermos y de los resultados de una intervención a lo largo del tiempo, parece lógico utilizar medidas de desenlace que contemplen incidencia e incluyan el tiempo hasta un suceso, en lugar de utilizar medidas de prevalencia. En el caso particular del presente estudio, este aspecto es importante, ya que las diferencias en la remisión de la proteinuria entre ambos grupos son significativas a los 10 meses, pero no a los 12 meses. Estos datos parecen sugerir que la respuesta antiproteinúrica es más rápida en caso de amigdalectomía y este aspecto no puede ser analizado utilizando medidas de prevalencia. De los resultados comunicados por los autores y en el supuesto de un análisis por intención de tratar, se deduce que unos 25 de los 40 enfermos (63 %) del grupo A y unos 16 de los 40 (39 %) del grupo B presentaron remisión de proteinuria a los 12 meses. Traducido en medidas de asociación, estos datos significarían una hazard ratio de remisión de 1,56 (IC 95 % 1-2,45) para el grupo amigdalectomía que no tendría significación estadística, pero estaría muy próximo a ella. Por otra parte, resulta difícil saber con qué valores finales se realizaron los cálculos del número de remisiones a los 12 meses, ya que el 63 % de 40 no es un número exacto y el 39 % de 40 tampoco. Además, en las figuras se observa que solo se pudo disponer de determinaciones de proteinuria a los 12 meses en 32 de los 40 enfermos del grupo A y en 36 de los 40 enfermos del grupo B, lo que no permite adscribir respuestas en sentido positivo o negativo a los demás casos. Con los valores de p descritos para las diferencias de prevalencia a los 12 meses (p: 0,07), un cambio de tan solo 1 remisión en uno de los grupos podría implicar que las diferencias pasaran de no ser a ser estadísticamente significativas.
¿ CLASIFICACIÓN
Palabras clave: (20)
NIVEL DE EVIDENCIA: 1B
GRADO DE RECOMENDACIÓN: B
(Levels of Evidence CEBM. Universidad de Oxford: http://www.cebm.net/levels_of_evidence.asp).