La insuficiencia renal aguda (IRA) se define como una disminución brusca de la capacidad de los riñones para eliminar productos nitrogenados y con frecuencia se acompaña de una disminución de la diuresis1. La clasificación de RIFLE y AKIN y, más recientemente, la clasificación KDIGO1 han definido criterios diagnósticos y de gravedad de la IRA. Sin embargo, ninguna de ellas aporta información útil para la detección precoz y la monitorización de la evolución del daño renal agudo2.
La elevación de la concentración sérica de creatinina y de urea determinan el diagnóstico de la IRA; sin embargo, estas determinaciones presentan importantes limitaciones para el diagnóstico de IRA. La concentración sérica de creatinina se eleva de forma tardía en el daño renal agudo, mientras que la concentración sérica de urea está influida por otros factores no renales3. Se han descritos otros marcadores de daño renal, como proteínas y péptidos (como la cistatina C, interleucina 18, kidney injury molecule 1, neutrophil gelatinase-associated lipocalin, entre otros)4. La mayoría de estos biomarcadores están correlacionados con lesión tubular pero también con otras enfermedades inflamatorias como la sepsis o la enfermedad renal crónica (ERC)4, por lo cual pierden utilidad para el diagnóstico específico, la detección precoz y la predicción del pronóstico del daño renal agudo.
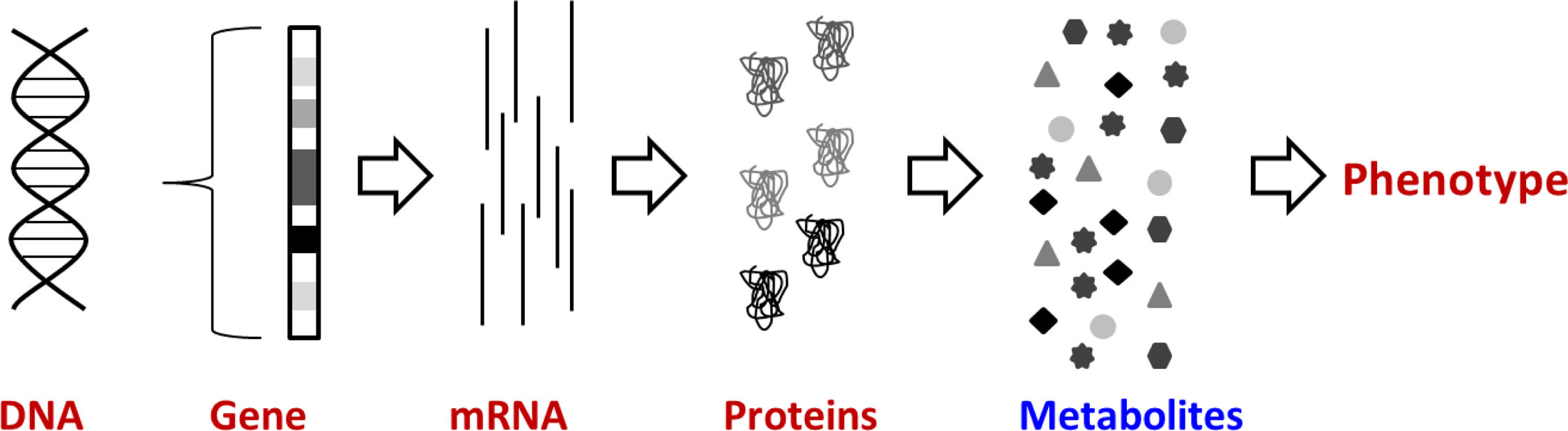
En este contexto se ha propuesto el uso de nuevas herramientas para el diagnóstico, pronóstico y monitorización de la IRA, como la proteómica y la metabolómica. Las proteínas constituyen las principales unidades funcionales y estructurales de las células, y sus efectos sobre la función celular se definen por el conjunto de metabolitos que se sintetizan o degradan por la acción enzimática específica de ciertas proteínas. El patrón específico de expresión de las proteínas (proteoma) y de metabolitos (metaboloma) define el estado biológico del órgano o tejido5.
El estudio del proteoma (proteómica) y del metaboloma (metabolómica) se ha propuesto como una herramienta útil para el descubrimiento de biomarcadores diagnósticos y pronósicos de IRA. A diferencia de la proteómica, la metabolómica proporciona información completa sobre los procesos metabólicos de la célula mediante la identificación de los productos de las reacciones metabólicas. La descripción del proteoma (mediante, por ejemplo, espectrometría de masas) y del metaboloma (mediante, por ejemplo, espectroscopía de resonancia magnética) permite la descripción de patrones moleculares que son útiles como biomarcadores de diagnóstico, pronóstico o de respuesta terapéutica5.
En la metabolómica existen 2enfoques principales: análisis no dirigidos (no supervisados) y análisis dirigidos (supervisados). El análisis dirigido se centra en un conjunto específico de compuestos, que a menudo son similares en estructura y propiedades químicas o se derivan de la misma vía biológica. Por el contrario, los enfoques no dirigidos adoptan un enfoque global al intentar medir de forma no supervisada tantos metabolitos como sea posible y utilizar herramientas estadísticas para identificar aquellos que difieren entre individuos sanos y enfermos4,6. Los enfoques no dirigidos presentan mayor dificultad y de sus resultados pueden derivarse nuevas hipótesis para el diagnóstico de enfermedades fig. 1.
En la ERC varios estudios han identificado metabolitos asociados a la progresión de la misma. Se han descrito cambios significativos en el aclaramiento de solutos endógenos urémicos (como p-cresol, indoxyl sulfato y fenilacetilglutamina)7 que podrían considerarse señales para la detección temprana de la ERC. El estudio de la utilidad de la metabolómica en la IRA se encuentra todavía en estadios precoces y aún hay muchos aspectos que esclarecer. Se han identificado en pacientes con IRA compuestos relacionados con el metabolismo de xenobióticos (como citocromo P450, arginina y prolina)8,9. Asimismo, en pacientes críticos se ha descrito que la concentración de tissue inhibitor of metalloproteinase (TIMP)-2 e insulin-like growth factor-binding protein (IGFBP)-7 se relaciona con la gravedad y el tiempo de evolución de la IRA5,10.
En resumen, el abordaje tradicional basado en la determinación de la concentración de ciertas moléculas como biomarcadores de IRA presenta importantes limitaciones. Futuros abordajes utilizando técnicas no supervisadas que describan patrones metabolómicos que reflejen el estado metabólico de la célula son prometedores para el descubrimiento de biomarcadores útiles para el diagnóstico precoz, el pronóstico y la monitorización de la IRA.