Síndrome tóxico en paciente trasplantado renal: sin cartas para el descarte
Maria Quero Ramos1, Laura Martínez Valenzuela1, Ángela Casas Parra1, Anna Manonelles Montero1, August Vidal Bel2, Oriol Bestard Matamoros1, Edoardo Melilli1, Xavier Fulladosa Oliveras1 y Josep Maria Cruzado Garrit1
1Servicio de Nefrología. Unidad de Trasplante Renal. Hospital Universitari de Bellvitge. 2Servicio de Anatomía Patológica. Hospital Universitari de Bellvitge, L¿Hospitalet de Llobregat, Barcelona
Resumen
Hombre de 56 años hipertenso, con enfermedad renal crónica no filiada que requirió tratamiento renal sustitutivo con diálisis peritoneal y transferencia a hemodiálisis un año después por peritonitis por Staphylococcus aureus.
Receptor de trasplante renal en enero/2013 de donante de criterios expandidos, compartiendo 2 identidades. Recibió inducción con basiliximab, tacrolimus, micofenolato mofetilo y esteroides. Serologías del donante negativas excepto CMV, siendo las del receptor CMV y VEB positivas. En el post trasplante presentó desprendimiento de placa de ateroma de la arteria ilíaca comprometiendo el flujo vascular con creatinina nadir 240umol/L.
Al mes presentó infección por CMV que recidivó tras suspensión del tratamiento con valganciclovir, por lo que se convirtió desde MMF a iMtor (Sirolimus), viremias sucesivas negativas.
En consulta mostraba deterioro de la función renal hasta cifras de 350 umol/L, FG de 19ml/min, con niveles correctos, proteinuria de 1gr/día y sedimento negativo. Rechazó someterse a biopsia renal.
Ingresa el 23/enero/2014 por cuadro de 10 días de evolución de astenia, hiporexia y pérdida de peso. Destacaba fiebre (38ºC) con diaforesis y sin focalidad infecciosa. PA 110/70mmHg sin taquicardia. Explicaba consumo, durante el último mes, de productos de herboristería/homeopatía.
Analíticamente creatinina de 497umol/L, hipoalbuminemia (25g/L), anemia microcítica, plaquetopenia leve, linfopenia y monocitosis (29,4%), con acidosis metabólica, patrón urinario funcional sin aumento de proteinuria y niveles de Tacrolimus y Sirolimus elevados (11 y 9µg/L respectivamente).
Ante el síndrome tóxico severo, se solicitó PET-TAC que destacaba imagen pulmonar en vidrio deslustrado y adenopatías milimétricas mediastínicas, hiliares y retroperitoneales, con débil captación. No presentaba otras captaciones patológicas.
Se solicitó PCR virus influenza A y B, CMV, cuantiferón TBC, serología para Leishmania, virus hepatotropos, VHS, VH6, VEB, LUES y toxoplasma, Brucela siendo todas negativas. Se realizó broncoscopia sin lesiones endobronquiales. Se realizó BAL.
Evolucionó con persistencia de fiebre, diarreas, empeoramiento del síndrome tóxico, edema generalizado, ascitis y empeoramiento de la función renal, requiriendo inicio de hemodiálisis. Se repitió PCR CMV que fue negativa y se realizó colonoscopía con biopsias sin hallazgos patológicos. Estudio de líquido ascítico compatible con trasudado con cultivo negativo.
En seguimiento analítico había progresión de la plaquetopenia (10.000), pancitopenia y aumento de índices inflamatorios (PCR, VSG y Ferritina) y patrón de colostasis. Dada la mala evolución se decidió retirar Sirolimus.
Ante la ausencia de adenopatías significativas, se realizó biopsia de médula ósea objetivando médula hiperplásica sin evidencia de neoplasia ni hematofagocitosis.
Se inició tratamiento antibiótico empírico para tuberculosis y antifúngico, posteriormente salieron resultados de BAL: Aspergillus, TBC y Pneumocistis negativos. Se retiró el Tacrolimus y se dejó corticoide(mg/kg).
No se observó mejoría clínica y por empeoramiento del patrón de colostasis y transaminitis se realizó TAC-ABD: Hepato-esplenomegalia, ascitis y vesícula biliar distendida. No se observaron otros hallazgos patológicos. Se descartó obstrucción biliar por colangioresonancia.
Finalmente se realizó biopsia hepática transyugular (9000 plaquetas) que no mostró hallazgos sugestivos de proceso neoplásico/linfomatoso ni proceso viral. Se descartó presencia de metales tóxicos en sangre periférica.
Evolución hacia fracaso multiorgánico, siendo éxitus tras 45 días de ingreso. Se realizó el diagnostico post mortem.
Introducción
En el postrasplante tardío las complicaciones más frecuentes en contexto de síndrome tóxico y febril son las infecciones y los procesos neoplásicos.
En cuanto a las infecciones se refiere, la aparición de infecciones graves por gérmenes oportunistas (Cryptococcus neoformans, Listeria, Aspergillus, Pneumocistis carinii, Nocardia, tuberculosis y monocytogenes) son más frecuentes en pacientes que han estado sobre inmunodeprimidos, por ejemplo pacientes que han recibido tratamiento por episodios de rechazo agudo, y por lo tanto se suelen presentar en los primeros meses post trasplante.
La tuberculosis presenta una incidencia de 36 a74 veces mayor en pacientes inmunodeprimidos y debe ser tenida en cuenta en el diagnóstico diferencial de fiebre de origen desconocido en los pacientes receptores de órganos, sobretodo después del primer año del trasplante1.
Con respecto al desarrollo de neoplasias, es notorio que los pacientes trasplantados presentan un riesgo de 2 a 5 veces superior que la población general, siendo las más frecuentes los procesos linfoproliferativos (1¿20%), los cánceres cutáneos no melanomas, cáncer de vejiga, testículo y renal2,3.
Determinadas neoplasias guardan estrecha relación con infecciones víricas como es el caso de VEB con procesos linfoproliferativos, sobre todo en los casos de PTLD durante el primer año postrasplante4 , Herpes virus humano 8 (HHV-8) con el sarcoma de Kaposi, síndrome de Castleman y linfoma de cavidades y el virus del papiloma humano (VPH) con las neoplasias de pene, vulva y cuello uterino.
Os presentamos el caso de un paciente trasplantado renal de un año de evolución que ingresó en nuestro servicio por presentar síndrome tóxico y fiebre sin focalidad infecciosa asociada.
Caso clínico
Se trata de un varón de 56 años hipertenso, con enfermedad renal crónica no filiada que requirió inicio de tratamiento renal sustitutivo (02/2011) con diálisis peritoneal y transferencia a hemodiálisis un año después por peritonitis por Staphylococcus aureus.
Fue receptor de un primer trasplante renal en enero/2013 de donante de criterios expandidos de bajo riesgo inmunológico con PRA 0% y aloanticuerpos de fase sólida clase 1 y 2 negativos, compartiendo 2 identidades con el donante (1 DR y 1 B), por lo que recibió inducción con basiliximab, tacrolimus, micofenolato mofetilo (MMF) y esteroides. Serologías de VIH, LUES y hepatitis B y C de donante y receptor negativas con CMV y VEB positivos. En el post trasplante inmediato presentó desprendimiento de placa de ateroma de la arteria ilíaca según informe quirúrgico, destacando empeoramiento de perfusión renal y ausencia de pulso arterial por lo que se deshizo la anastomosis arterial y se objetivó placa de ateroma parcialmente despegada realizando fijación de la placa y colocación de parche de Dacron, con reanastomosis posterior sin incidencias. Doppler de control mostró perfusión homogénea del injerto, condicionando compromiso del flujo vascular quedando con disfunción importante: creatinina 270µmol/L con filtrado glomerular según CKD EPI de 21ml/min.
Al mes post trasplante presentó infección por CMV que recidivó tras suspensión del tratamiento con valganciclovir, por lo que se convirtió de MMF a iMtor (Sirolimus), destacando posteriormente viremias sucesivas negativas. Niveles post conversión de Tacrolimus de 6,8µg/L y Sirolimus 5,3µg/L.
En el seguimiento en consultas mostraba deterioro de la función renal hasta cifras de 350 µmol/L, que le condicionaba un FG de 19ml/min, proteinuria de 1gr/día y sedimento negativo. El paciente rechazó someterse a biopsia renal en el seguimiento en consultas.
Ingresó el 23/enero/2014 por cuadro de diez días de evolución de astenia, hiporexia y pérdida de peso. Destacaba fiebre (38ºC) con diaforesis y sin focalidad infecciosa. Tendencia a hipotensión arterial, con valores de 110/70mmHg sin taquicardia.
Explicaba consumo, durante el último mes, de productos de herboristería/homeopatía.
Analíticamente creatinina de 497µmol/L, hipoalbuminemia (25g/L), anemia microcítica, plaquetopenia leve, linfopenia y monocitosis (29,4%), con acidosis metabólica, patrón urinario funcional sin aumento de proteinuria y niveles de Tacrolimus y Sirolimus elevados (11 y 9µg/L respectivamente).
Ante el síndrome tóxico severo, se solicitó PET-TAC (ilustración 1) que destacaba imagen pulmonar en vidrio deslustrado y adenopatías milimétricas mediastínicas, hiliares y retroperitoneales, con débil captación. No presentaba otras captaciones patológicas.
Se solicitó PCR virus influenza A y B, CMV, cuantiferón TBC, serología para Leishmania, virus hepatotropos, VHS, VH6, VEB, LUES, toxoplasma y Brucela siendo todas negativas. Se realizó broncoscopia que no objetivó lesiones endobronquiales y se realizó BAL.
Evolucionó con persistencia de fiebre, diarreas, empeoramiento del síndrome tóxico, anasarca, ascitis y empeoramiento de la función renal, requiriendo inicio de hemodiálisis. Se repitió PCR CMV que fue negativa y se realizó colonoscopia con biopsias sin hallazgos patológicos. Estudio de líquido ascítico compatible con trasudado (glucosa 6.1mmol/L, proteínas 11g/L, 500 células (18% PMN, 45% histiocitos y 37% linfocitos) con cultivo negativo.
En el seguimiento analítico había progresión de la plaquetopenia (10.000), pancitopenia, elevación de reactantes de fase aguda (PCR, VSG y Ferritina) y patrón de colostasis. Dada la mala evolución se decidió retirar progresivamente los inmunosupresores manteniendo únicamente monoterapia con corticoides.
Ante la ausencia de adenopatías significativas y la sospecha clínica de enfermedad hematológica, se realizó biopsia de médula ósea objetivando médula hiperplásica sin evidencia de neoplasia ni hematofagocitosis.
Se inició tratamiento antibiótico empírico para tuberculosis y antifúngico, obteniendo posteriormente los resultados del BAL: Aspergillus, TBC y Pneumocistis negativos.
No se observó mejoría clínica y ante empeoramiento del patrón de colostasis y transaminitis se realizó TAC-ABD destacando hepato-esplenomegalia, ascitis y vesícula biliar distendida, sin otros hallazgos patológicos. Se descartó obstrucción biliar por colangioresonancia.
Finalmente se realizó biopsia hepática transyugular (9000 plaquetas) que no mostró hallazgos sugestivos de proceso neoplásico/linfomatoso ni proceso viral. Se descartó presencia de metales tóxicos en sangre periférica.
Evolucionó hacia fracaso multiorgánico, siendo éxitus tras 45 días de ingreso. Se realizó el diagnóstico post mortem de síndrome hemofagocítico asociado a sarcoma de Kaposi ganglionar y linfoma primario de cavidades con afectación parcheada a nivel ganglionar, esplénica, hepática, pulmonar, adrenal, tiroidal y renal.
Destacaba obstrucción de la vía biliar condicionada por adenopatías pericoledocales.
Discusión
El herpes virus humano 8 (HHV-8) se asociaba con el sarcoma de Kaposi, enfermedad de Castleman y el linfoma de cavidades.
El linfoma primario de cavidades (LPC) es un linfoma célula B no Hodgkin poco frecuente. Se describió por primera vez en 1989 y a pesar de que su patogénesis no es del todo conocida, se considera que la infección por el HHV-8 juega un rol importante en esta enfermedad.
La evidencia de la infección por HHV-8 de las células tumorales se caracteriza por elevados niveles de DNA de HHV-8 e inmunotinción positiva para LANA-1 (antígeno nuclear de latencia asociado).
Se han descrito muy pocos casos en la literatura de LPC en pacientes trasplantados, presentando todos ellos anticuerpos anti HHV-8 5,6,7.
En los pacientes trasplantados originarios de países con seroprevalencia media alta para el HHV-8, el riesgo de sarcoma de Kaposi depende principalmente de la reactivación del virus más que de la transmisión de infección primaria a través del órgano, y se considera que el proceso es el mismo en el LPC 8.
Clínicamente se caracteriza por la presencia de derrame linfomatoso en cavidades serosas: pleural, pericárdica o peritoneal.
Para establecer el diagnóstico es importante la realización del inmunofenotipo de las células neoplásicas linfoides siendo característico de este linfoma las células no T, no B, CD138+ y LANA-1 +.
Por lo que a la evolución y al tratamiento se refiere, los pacientes presentan evolución tórpida con mortalidad del 100% de los casos descritos durante los primeros 6 meses tras el diagnóstico, a pesar de recibir tratamiento específico (quimioterapia CHOP) y de la modificación de inhibidores de la calcineurina por Rapamicina (se han descrito efectos antitumorales de los iMtor en líneas murinas)9.
El síndrome hemofagocítico es una enfermedad sistémica inflamatoria fulminante que puede ser primaria (enfermedad genética) o secundaria (adquirida) en contexto de enfermedades hematológicas, neoplásicas o en contexto de infecciones virales (VEB, VIH, HHV8)10.
Se caracteriza por la infiltración histiocitaria del sistema retículo endotelial produciendo destrucción de los elementos formes de la sangre11.
El HHV-8 se asocia raramente al síndrome hemofagocítico, siendo esta relación más frecuente en pacientes inmunodeprimidos12.
En pacientes con síndrome hemofagocítico adquirido, como en el caso que presentamos, el tratamiento del linfoma es el tratamiento de elección para tratar el síndrome hemofagocítico.
En nuestro caso, a pesar de múltiples test diagnósticos para intentar filiar la causa del síndrome tóxico, esto fue únicamente posible post mortem. En el material histológico obtenido a través de las biopsias hepáticas, de colon y de médula ósea no fue posible identificar las características histológicas típicas del linfoma de cavidades ni del Kaposi probablemente por la naturaleza ¿focal¿ o ¿parcheada¿ de las lesiones. Cabe destacar la ausencia de lesiones cutáneas típicas del Kaposi.
Analizando el caso a posteriori, el estudio anatomopatológico del líquido ascítico hubiera podido detectar la presencia de células linfomatosas típicas del linfoma de cavidades y la determinación del HHV-8 en sangre periférica hubiera podido orientarnos en el diagnóstico ante mortem.
Por este motivo consideramos añadir la determinación de HHV-8 en el estudio de síndrome tóxico en paciente trasplantado renal de forma sistemática.
Conclusiones
El linfoma de cavidades, el sarcoma de Kaposi y el síndrome hemofagocítico son entidades de mal pronóstico que pueden asociarse a HHV8. Según nuestra revisión bibliográfica el caso que describimos es el primero con presencia de las tres enfermedades en un paciente portador de trasplante renal.
Figuras
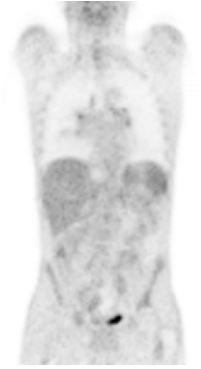
Figura 1
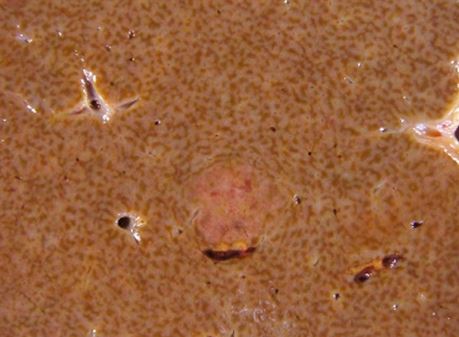
Figura 2. Macroscópica del hígado que muestra el carácter parcheado de las lesiones.
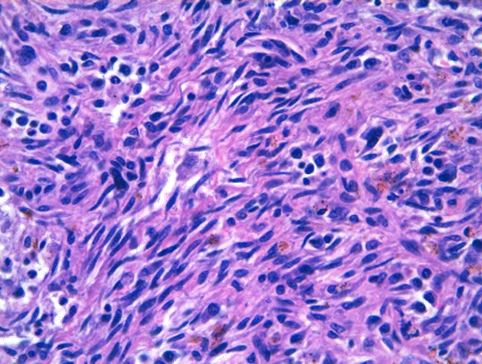
Figura 3. Hematoxilina eosina de un ganglio 630X. Células fusiformes características del sarcoma de Kaposi.
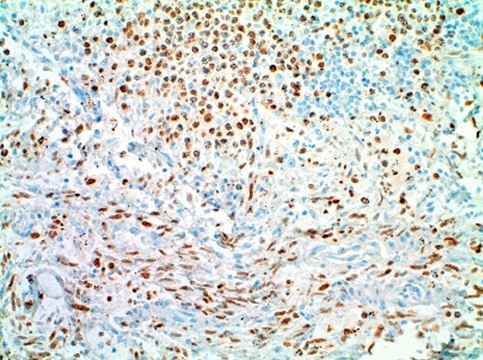
Figura 4. Inmunohistiquímica positiva para VHH-8 200X de un ganglio. En la parte superior se objetiva el linfoma de cavidades y la inferior el sarcoma de Kaposi.
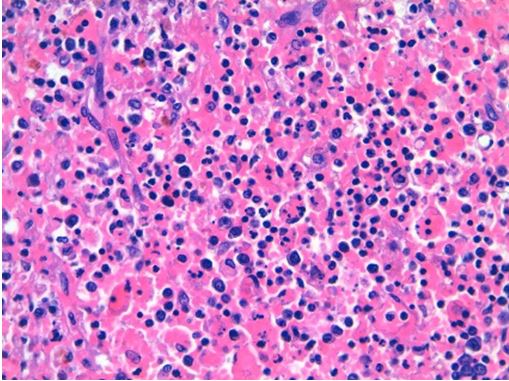
Figura 5. Hematoxilina/eosina de ganglio 400X. Hemofagocitos.
Bibliografía
1 Tabarsi P et al. Mycobacterial infection and the impact of rifabutin treatment in organ transplant recipients: a single-center study. Saudi J Kidney Dis Transpl. 2015;26:6-11.
2 CM Vajdic, S.P. McDonald, M.R. McCredie, M.T. van Leeuwen, J.H. Stewart, M. Law, et al., Cancer incidence before and after kidney transplantation, JAMA 296 (2006) 2823¿2831
3 J. Morscio, D. Dierickx, T. Tousseyn, Molecular pathogenesis of B-cell posttransplant lymphoproliferative disorder: what do we know so far?, Clin. Dev. Immunol. 2013 (2013) 150835.
4 Petrara MR et al. Post- transplant lymphoproliferative disorders: From epidemiology to pathogenesis-driven treatment. Cancer Letters 369 (2015) 37¿44
5 A rare case of HHV- 8 possitive/HIV-negative/EBV-negative primary effusion lymphoma in a renal transplant recipient, Cytopathology 2012, 23, 133-139
6 E. Boulanger et al., Human Herpesvirus-8 (HHV-8)-Associated Primary Effusion Lymphoma in two Renal Transplant Recipients Receiving Rapamycin. American Journal of Transplantation 2008; 8: 707-710
7 N.C.V.Melo et al., Pleural Primary Effusion Lymphoma in a Renal Transplant Recipient. American Journal of Transplantation 2008; 8: 906-907
8 Parravicini C, Olsen SJ, Capra M, et al. Risk of Kaposi¿s sarcoma associated herpes virus transmission from donor allografts among Italian posttransplant Kaposi¿s sarcoma patients. Blood 1997; 90: 2826-2829
9 Sin SH, Roy D, Wang et al. Rapamycin is efficacious against primary effusion lymphoma (PEL) cell lines in vivo by inhibiting autocrine signaling. Blood 2007; 109: 2165-2173
10 Shah NN et al., Extracavitary primary effusion lymphoma initially presenting with hemophagocytic lymphohistocytosis. Clinical Lymphoma, Myeloma & Leukemia, Vol. 14, No. 5, e157-60
11 Raymond D. Pastore et al., Novel association of haemophagocytic syndrome with Kaposi¿s sarcoma-associated herpesvirus-related primary effusion lymphoma. British Journal of Haematology, 2000, 111, 1112-1115
12 Bomi Kim, Yoon Kyung Jeon and Chul Woo Kim. Kaposi Sarcoma Herpes Virus-associated Hemophagocytic Syndrome complicated by multicentric Castleman Disease and Kaposi Sarcoma in a HIV- negative Immunocompetent Patient: An Autopsy Case. J Korean Med Sci 2009; 24: 970-4











