INTRODUCCIÓN
La infección urinaria (ITU) es una patología frecuente en la infancia, y frecuentemente se acompaña de anomalías en el tracto urinario, estando sobre todo asociada al reflujo vesicoureteral (RUV) que presentan entre un 30 y un 40% de los niños con ITU1,2.
La indicación de estudios de imagen en los niños con ITU es controvertida. La última guía de la Asociación Americana de Pediatría2 recomienda la realización de CUMS a todos los menores de 2 años con ITU, aunque posteriormente existe una amplia disparidad de opiniones sobre cuales son las exploraciones indicadas y sobre el momento de su realización3-9.
En este contexto recientemente se ha propugando una fórmula para predecir la presencia de RUV y evitar CUMS innecesarios10, fórmula cuya validez ha sido cuestionada por otros autores11. El objetivo de nuestro estudio es valorar la fórmula previamente presentada y proponer alternativas a la misma.
SUJETOS Y MÉTODOS
Se han estudiado a los niños diagnosticados de la primera Infección Urinaria (ITU) en la Sección de Lactantes desde enero de 2005 a junio de 2007, bien en consulta externa o en hospitalización.
Se incluyeron en el estudio todos los que tenían urocultivos positivos, valores de PCR al diagnóstico, ecografía realizada durante el episodio de ITU y cistouretrografía miccional seriada (CUMS), en un plazo máximo de 1 mes tras el diagnóstico de ITU, excluyéndose a 15 casos por faltar alguna de las variables analizadas.
Se calculó la puntuación de riesgo según el score de Oostenbrink (puntuación = 6* genero masculino + 7* historia familiar positiva ¿ 1* edad + 1*PCR + 14 por dilatación en ecografía renal)10.
Se calcularon también la sensibilidad, especificidad y cocientes de probabilidad positivos y negativos, con sus IC 95%, utilizando la página estadística 2-way Contingency Table Analysis disponible en Internet12.
Se realizó estudio multivariante mediante regresión logística binaria, utilizando el programa comercial SPSS 11.0©13, partiendo del modelo máximo en el que incluyeron todas las variables presentes en la fórmula de Oostenbrick mas la presencia de urocultivos positivos por gérmenes distintos al E Coli. Se fueron retirando del modelo, una a una, todas las que no alcanzaron valores de significación para p < 0,05.
RESULTADOS
El total de niños incluidos en el estudio fue 267. La edad osciló entre 2 días y 24 meses, con media de edad de 4,20 meses (desviación estándar de 4,79 meses, mediana 2,50 meses). De ellos 160 (59,9%) fueron niños. En la historia clínica 4 (1,5%) tenían antecedentes familiares de RUV, y 137 (51,3%) mantenían lactancia materna o la habían tenido al menos 3 meses.
Los gérmenes responsables de las ITU se agruparon en 2 grupos: E Coli (82,67%), y no E Coli (17, 33%), entre estos últimos el germen más frecuente fue la Klebsiella (22 casos), seguida por el Enterococo (14 casos), Proteus, Citrobacter y Estreptococo agalactie.
Presentaron anomalías en los riñones y/o vías urinarias en la ecografía un total de 40 niños, el 14,98% de los casos, en la mayoría de los casos dilataciones del sistema pielocalicial y pieloueteral (considerándose dilatación piélica a partir de 18 mm en el eje transversal y ureteral a partir de 10 mm en el uréter distal) y CUMS patológico 108 (40,44%). con un total de 175 riñones con RUV. Se calculó la probabilidad de RUV utilizando la fórmula de Oostenbrink10. La tabla I recoge los casos con puntuación mayor y menor de 0 (punto de corte propugnado) y RUV, observándose que la mayoría de los casos superaban este valor y solo 14 lo presentaban, de los cuales 8 tenían RUV.
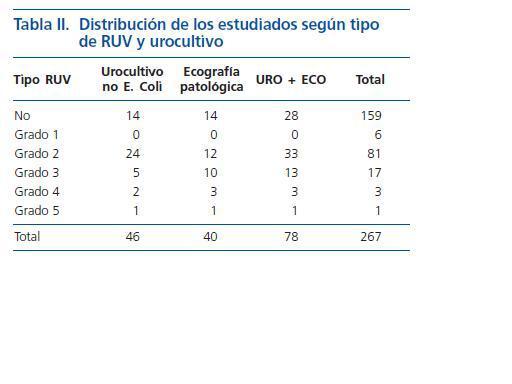
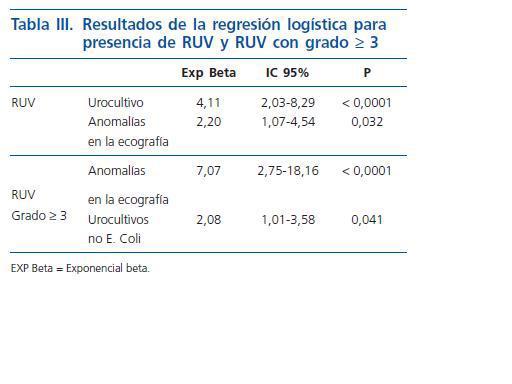
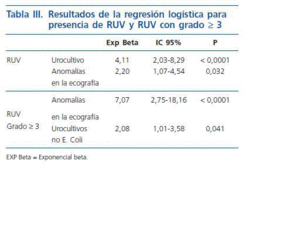
La tabla II recoge la distribución de la presencia de RUV y su grado, de acuerdo con la Internacional Study Classification14 (se consideró el máximo grado en los bilaterales) según hubieran presentado ecografía anormal e ITU por gérmenes distintos de E Coli o alguna de ambas características, y la tabla III los resultados de la regresión logística para la presencia de RUV y RUV grado ³ 3. Solo se encontró significación estadística con la presencia de anomalías en la ecografía e ITU no E Coli en ambos casos.
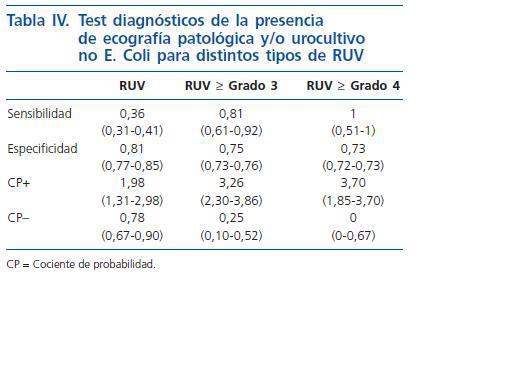
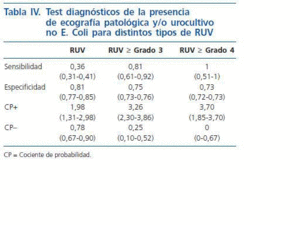
La tabla III recoge la sensibilidad, especificidad, y cocientes de probabilidad positivos y negativos para la presencia de urocultivos no E Coli y/o anomalías ecográficas para la presencia de RUV, y de RUV grado < 3 y RUV grado < 4. El cociente de probabilidad negativo fue de 0 para RUV < 4 y de 0,25 para RUV < 3.
DISCUSIÓN
La incidencia acumulada de ITU en los menores de 6 años se ha calculado entre el 3-7% en las niñas y el 1-2% en los niños, habiéndose recomendado la realización de pruebas de imagen después de la primera ITU para evaluar la presencia y grado de RUV, entre las que el CUMS tiene un lugar fundamental porque permite identificar la presencia o no de RUV y su grado2-4,6. Las decisiones terapéuticas que se derivan de la presencia de RUV están relacionadas con el grado de RUV e incluyen la corrección quirúrgica, el tratamiento profiláctico y el seguimiento sin tratamiento, existiendo una amplia controversia al respecto, si bien los estudios más recientes parecen señalar que la evolución es similar en los enfermos con RUV que siguen tratamiento profiláctico, respecto a los que no lo siguen, al menos en aquellos en los que el RUV es menor (grados I-II) que son la mayoría de los casos15-17.
La presencia de RUV se constata entre el 30-40% de los niños con ITU2, en nuestro caso en el 40,44%. Para evitar la realización del CUMS, que es una exploración traumática y con elevada cantidad de radiaciones, en el 60-70% de los niños en que no se presentara RUV, se ha propugnado por Oostenbrik una fórmula que consideraba la edad, la presencia de antecedentes familiares, el hallazgo de dilataciones en la ecografía renal y los valores de PCR, utilizando esta fórmula en su estudio sólo quedaba excluido del diagnóstico un caso con VUR10. Otros autores han cuestionado esta fórmula señalando que solo tenía una especificidad del 3% para cualquier tipo de RUV y del 13% para grados < 311. En nuestro caso la aplicación de la fórmula de Oostenbrik se demostró poco útil, en primer lugar porque solo en 14 casos (5,24%) quedaría excluida la realización de un CUMS, pero además porque en 8 de ellos se encontró RUV.
Se ha señalado también que la presencia de ITU por gérmenes distintos al E Coli sería un factor de riesgo para la presencia de anomalías del tracto urinario incluyendo RUV (OR 8, 16; IC 95%: 1,88-35,48)8, lo que también se observa en nuestro caso para la presencia de RUV (OR 3,98; IC95%: 1,99-7,95).
En el cálculo realizado mediante regresión logística tanto para presencia de cualquier tipo de RUV como para RUV grado < 3 se han introducido tanto las variables de la fórmula de Oostenbrik como la presencia de urocultivo por germen distinto al E Coli, objetivándose que solo la presencia de anomalías en la ecografía y la presencia de urocultivos no E Coli mantenian la significación estadística. Todos los RUV con grado < 4 eran detectados con estas condiciones, así como el 80,6% de los que tenían un grado < 3 y el 57,47% del total de RUV, si bien debe de tenerse en cuenta que solo encontramos 4 casos con grados superiores al 4.
Hay que tener en cuenta además que se ha puesto en cuestión la necesidad de la detección de los RUV de grado I-II debido a su buena evolución sin tratamiento, por lo que no esta clara la indicación de la realización de CUMS en todos los casos de ITU tal y como se había propugnando2,15-17,19.
Nuestro trabajo tiene como principal limitación el circunscribirse a niños menores de 24 meses remitidos a un hospital, que se supone son los que tienen una sintomatología más grave, si bien es cierto que la mayoría de los niños de pocos meses con síndrome febril suelen remitirse para su tratamiento y diagnóstico hospitalario.
En conclusión de nuestro estudio se deduce que parece razonable propugnar la limitación de la realización de CUMS en el primer episodio de ITU en menores de 2 años, a aquellos casos que presenten anomalías en la ecografía renal y/o urocultivos por gérmenes no E Coli. En todo caso sería conveniente la realización de estudios más amplios para confirmar estos hallazgos.
Tabla 1.
Tabla 2.
Tabla 3.
Tabla 4.