La ecografía basal (modo B, Doppler color y pulsado) ha sido considerada la técnica diagnóstica de elección para la valoración del trasplante renal1 ya que permite el estudio del parénquima y los vasos principales, segmentarios e interlobares. Sin embargo, no ofrece información acerca de la microvascularización que suele ser el sustrato patológico subyacente de la nefropatía del injerto2. Es por ello que el diagnóstico de rechazo, necrosis tubular aguda (NTA) o toxicidad medicamentosa frecuentemente recae en la biopsia3 ya que sus manifestaciones en la ecografía basal son en múltiples ocasiones inespecíficas4.
La ecografía con contraste intravenoso (CEUS) emplea un contraste puramente intravascular, y permite valorar en tiempo real la microcirculación y la perfusión vascular y tisular del injerto. Se puede emplear en pacientes con fracaso renal agudo, y presenta un riesgo de reacciones alérgicas sensiblemente menor que los contrastes yodados5.
Presentamos un estudio retrospectivo, observacional descriptivo que incluye a los pacientes adultos trasplantados de nuestro centro desde enero de 2011 hasta enero de 2015, con el objetivo de valorar el rendimiento de la CEUS en el diagnóstico de complicaciones parenquimatosas y vasculares del injerto.
A todos los pacientes (edad media: 57,7 años) se les realizó una primera ecografía basal en las primeras 24h postrasplante. Se confeccionó un programa de seguimiento ecográfico individualizado en función de los hallazgos de este estudio inicial.
En aquellos casos con alteraciones en modo B (engrosamiento cortical difuso, alteración focal de la ecoestructura y pérdida de la diferenciación corticomedular), así como en el estudio Doppler (ausencia de registro, inversión de color, pérdida de diástole, morfología en «parvus-tardus» o «alisasing»), previo consentimiento informado se procedió a la administración de 2,4ml de contraste ecográfico intravenoso de segunda generación (hexafluoruro de azufre, Sonovue®, Bracco) mediante técnica habitual. A continuación se realizó el estudio CEUS con un ecógrafo de altas prestaciones (Toshiba Aplio XG®) para valoración cualitativa de la captación del parénquima, así como las características de realce de estructuras vasculares del injerto. No se registraron complicaciones en ninguna de las exploraciones, las cuales fueron todas realizadas por el mismo radiólogo experto.
De los 131 injertos, un total de 27 pacientes (15 mujeres y 12 varones) presentaron alteraciones en la ecografía basal, y a continuación se les realizó la CEUS en acto único.
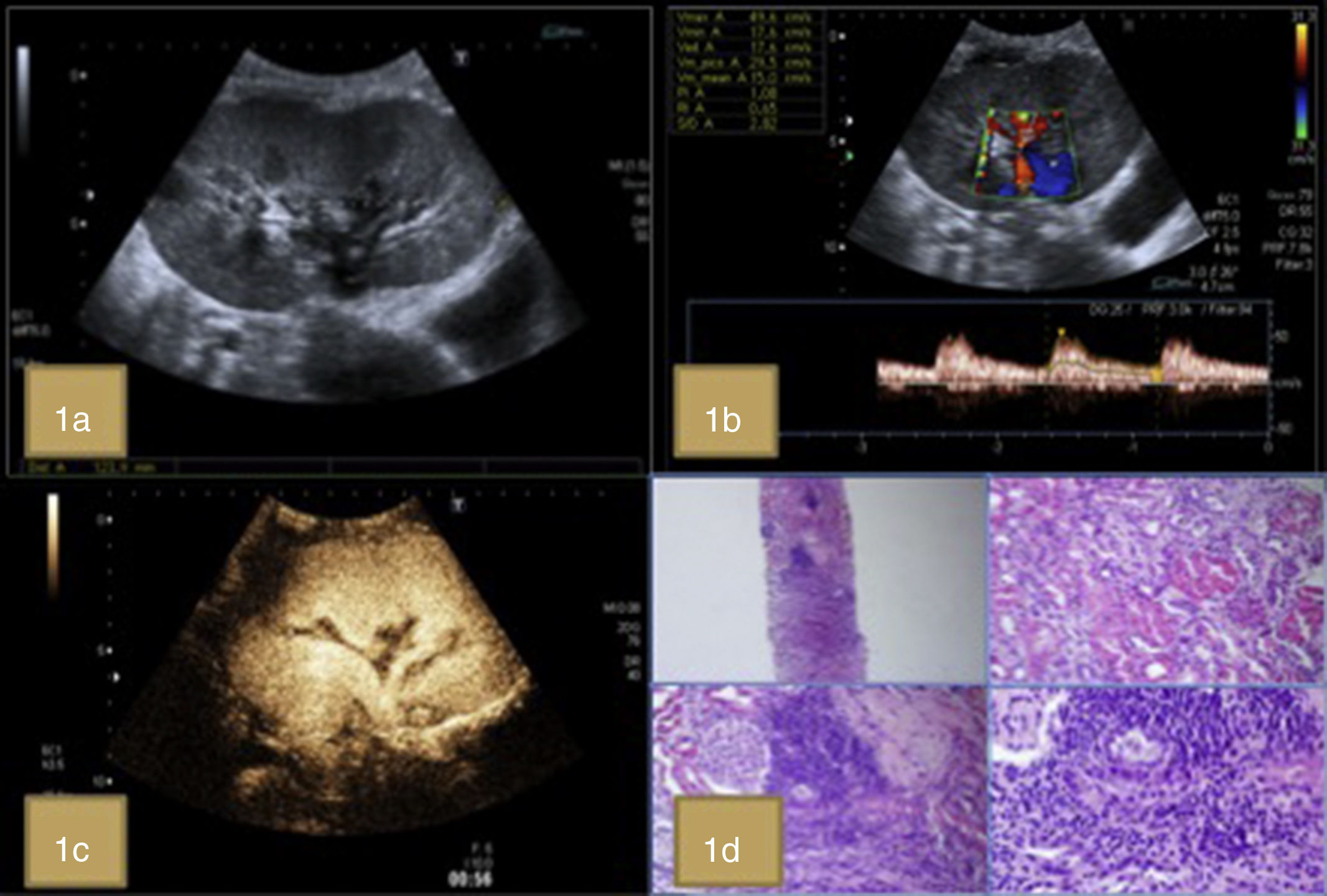
Seis pacientes presentaron hallazgos patológicos en modo B si bien la CEUS no demostró alteraciones significativas. Estos casos correspondieron a afectación parenquimatosa tipo rechazo agudo en un paciente (comprobación histológica; fig. 1) y 5 casos con NTA (diagnosticada analíticamente).
a) Estudio en modo B con engrosamiento cortical y pérdida de la diferenciación corticomedular. b y c) Ecografía Doppler pulsado y tras la administración de CIV sin alteraciones. d) Rechazo agudo celular grado IA de Banff. Los cortes histológicos muestran un infiltrado linfoide que afecta al 25% de la muestra (A) con edema intersticial (B) y frecuentes imágenes de tubulitis (C y D) (H&E).
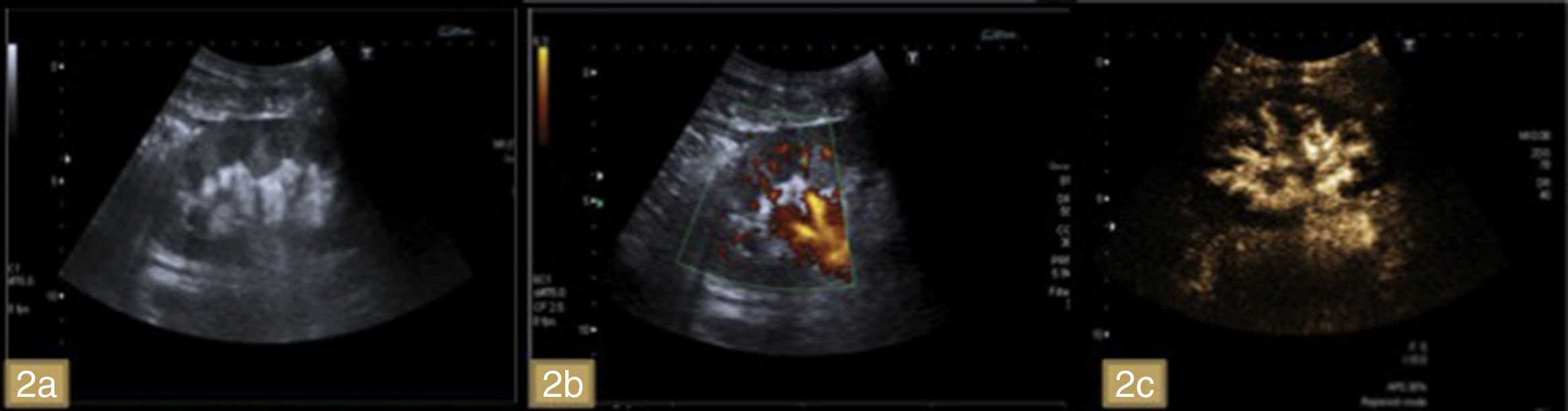
Se recogieron un total de 25 complicaciones en los 21 pacientes restantes siendo la más frecuente el infarto (defecto de captación corticomedular focal tras la administración de contraste intravenoso [CIV]), la estenosis de la arteria (estrechamiento focal de la arteria nivel extrarrenal) y la necrosis cortical (defecto de captación exclusivamente cortical con morfología en semiluna; fig. 2), seguidos de la estenosis de la vena renal (estrechamiento focal de la vena), trombosis arteria (ausencia de realce), fístula arteriovenosa (imagen seudonodular intraparenquimatosa en donde se delimita vena eferente de manera precoz) y acodamiento vascular (plegamiento de estructura vascular que adopta morfología en horquilla).
Se realizaron de manera complementaria 6 tomografías computarizadas (TC) sin CIV, 4 TC con CIV y 3 arteriografías, que no aportaron información adicional a las CEUS.
En los pacientes con anomalías en modo B, la CEUS proporcionó un diagnóstico rápido y fiable de infarto renal y necrosis cortical.
En pacientes con anomalías en estudio Doppler, la CEUS demostró en tiempo real las estenosis, acodaduras y trombosis de arteria y vena renales proporcionando detalle exquisito acerca de su localización y extensión sin necesidad de recurrir a exploraciones con radiaciones ionizantes6 ni al empleo de contrastes yodados.
Asimismo, la CEUS confirmó de manera inmediata las sospechas de trombosis arterial o venosa, mostrando la severidad de la lesión y el compromiso de la perfusión del injerto con la misma concordancia que los TC realizados.
Cabe señalar que la valoración cualitativa de la captación parenquimatosa de contraste ecográfico resultó insuficiente para el diagnóstico de NTA y rechazo, ya que la CEUS en estos pacientes fue normal a pesar de presentar anomalías en el estudio en modo B y Doppler.
No obstante, el desarrollo de nuevos algoritmos de valoración cuantitativa de la captación de CIV con ecografía prometen ser una herramienta revolucionaria para el diagnóstico de la disfunción parenquimatosa del injerto2,7, en donde los valores analíticos pueden estar escasamente alterados, especialmente en estadios precoces.
Se propone desde este trabajo una nueva línea de investigación más compleja, compuesta por una cohorte superior de pacientes, para corroborar estos resultados y dar respuesta a esta nueva hipótesis.
A todo el personal de la Sección de Ecografía y al personal de Enfermería del Servicio de Radiodiagnóstico del Hospital Virgen de la Salud.