La diálisis sostenida de baja eficiencia (SLED) es una modalidad intermitente de reemplazo renal híbrida entre la hemodiálisis intermitente convencional (HDI) y las técnicas continuas de reemplazo renal (TCRR)1. La superioridad de las técnicas continuas comparada con la de las intermitentes convencionales en cuanto a tolerancia hemodinámica en pacientes críticos no ha sido demostrada2,3, por lo que la elección de la modalidad depende de la disponibilidad de estas y de la experiencia del prescriptor. No obstante, es una realidad clínica que aproximadamente dos tercios de las sesiones de HDI en pacientes críticos no son bien toleradas4, requiriendo en un menor porcentaje la transferencia a técnicas continuas.
Presentamos la experiencia del uso de SLED en un hospital de tercer nivel donde existe la disponibilidad de uso de ambas modalidades y en el que la prescripción tanto de técnicas continuas como intermitentes depende del Servicio de Nefrología.
El objetivo de nuestro estudio fue describir las características de los pacientes que recibieron tratamiento sustitutivo renal tipo SLED en unidades de cuidados intensivos por indicación no protocolizada del especialista en Nefrología. Como objetivos secundarios nos planteamos valorar las complicaciones en cuanto a tolerancia hemodinámica y diselectrolitemias.
Para ello se realizó un estudio retrospectivo a partir del registro de pacientes en unidades de cuidados intensivos tratados con SLED entre 2014 y 2016, incluyendo aquellos que la recibieron, bien como primera opción terapéutica, bien inmediatamente después de recibir TCRR, bien después de HDI. La técnica fue definida como QB 100-150ml/min, QD 200-250ml/min y tiempo de diálisis 7-8h. La presencia de inestabilidad hemodinámica en una sesión se definió como la necesidad de inicio o aumento de fármacos vasoactivos durante la sesión según el registro de enfermería, caída de la presión arterial sistólica<90mmHg cuando los valores fueron superiores a 90mmHg al inicio de la sesión o descenso de>25% de la presión arterial sistólica o diastólica durante la sesión. Se definió como mortalidad aquella sucedida durante el ingreso hospitalario.
Se analizaron un total de 54 pacientes, de los cuales 26 recibieron la técnica después de HDI, 11 como primera opción terapéutica y 17 como primera opción después de TCRR. Las características de los 3 grupos, además de las complicaciones, se exponen en la tabla 1.
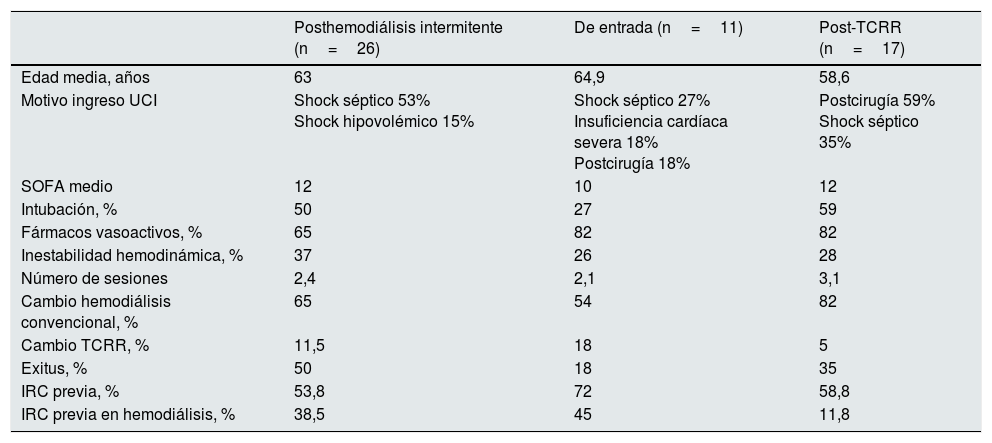
Características de los pacientes tratados con diálisis sostenida de baja eficiencia divididos según el momento de su realización
| Posthemodiálisis intermitente (n=26) | De entrada (n=11) | Post-TCRR (n=17) | |
|---|---|---|---|
| Edad media, años | 63 | 64,9 | 58,6 |
| Motivo ingreso UCI | Shock séptico 53% Shock hipovolémico 15% | Shock séptico 27% Insuficiencia cardíaca severa 18% Postcirugía 18% | Postcirugía 59% Shock séptico 35% |
| SOFA medio | 12 | 10 | 12 |
| Intubación, % | 50 | 27 | 59 |
| Fármacos vasoactivos, % | 65 | 82 | 82 |
| Inestabilidad hemodinámica, % | 37 | 26 | 28 |
| Número de sesiones | 2,4 | 2,1 | 3,1 |
| Cambio hemodiálisis convencional, % | 65 | 54 | 82 |
| Cambio TCRR, % | 11,5 | 18 | 5 |
| Exitus, % | 50 | 18 | 35 |
| IRC previa, % | 53,8 | 72 | 58,8 |
| IRC previa en hemodiálisis, % | 38,5 | 45 | 11,8 |
En la primera columna, después de hemodiálisis intermitente convencional; en la segunda, como primera opción terapéutica, y en la tercera, como primera opción después de TCRR.
Como otras complicaciones a destacar, además de las relacionadas con la tolerancia hemodinámica, en un 29,6% de los casos se detectó hipocalemia en relación con la sesión y se describieron también hipoglucemia severa, dolor torácico y sangrado, en un caso aislado cada una de ellas.
En cuanto a la recuperación de la función renal, excluyendo los pacientes que recibían diálisis como tratamiento crónico o que fueron exitus durante el ingreso (n=21), un 66,6% la recuperaron completamente y un 19% requirió hemodiálisis al alta. Un 29% del total de los pacientes no requirió HDI después de las sesiones de SLED.
Así, según nuestro registro, la mayor parte de los tratamientos con SLED son indicados después de una HDI mal tolerada; en segundo lugar, como paso entre la TCRR y la HDI, y menos frecuentemente, como un primer tratamiento en pacientes críticos. El perfil del paciente es portador de fármacos vasoactivos, mayoritariamente intubado cuando usamos la técnica después de TCRR. En cuanto a la tolerancia hemodinámica, más de un 70% de las sesiones fueron bien toleradas, siendo el porcentaje de un 63% cuando realizamos la técnica después de HDI, aunque ninguna de las sesiones tuvo que ser suspendida por mala tolerancia hemodinámica. Un punto interesante es que de entre todos los pacientes a los que se indicó SLED después de una HDI mal tolerada, solo un 11,5% recibió posteriormente TCRR, lo que parece indicar que la técnica ha cumplido su objetivo de mantener la modalidad intermitente.
Creemos, por lo tanto, que la SLED es una técnica intermitente de reemplazo renal poco extendida como primera modalidad de tratamiento en las unidades de cuidados intensivos y más utilizada como paso intermedio entre TCRR y HDI. Una de las posibles causas de su uso reducido de entrada es la disponibilidad de la técnica debido a su larga duración5, al depender de personal de enfermería de diálisis para su aplicación. Creemos que si se expande su conocimiento, esta técnica puede tener un rol importante al ser bien tolerada en pacientes críticos.