Los pacientes con enfermedad renal crónica (ERC) tienen tendencias hemorrágicas y trombóticas, por lo que la indicación de anticoagulación ante la aparición de fibrilación auricular (FA) es compleja. La FA es la arritmia cardíaca crónica más frecuente, siendo el tromboembolismo y el ictus isquémico en particular las complicaciones más importantes. En los últimos años se han desarrollado nuevos fármacos anticoagulantes orales que han mostrado superioridad respecto a los clásicos antagonistas de la vitaminaK (AVK) en la prevención de ictus, embolismo sistémico y riesgo de sangrado, constituyendo una alternativa eficaz a ellos.
Patients with chronic kidney disease (CKD) develop bleeding and thrombotic tendencies, so the indication of anticoagulation at the onset of atrial fibrillation (AF) is complex. AF is the most common chronic cardiac arrhythmia, and thromboembolism and ischemic stroke in particular are major complications. In recent years, new oral anticoagulant drugs have been developed, and they have shown superiority over the classical AVK in preventing stroke, systemic embolism and bleeding risk, constituting an effective alternative to those resources.
Los pacientes con enfermedad renal crónica (ERC) presentan un problema difícil de resolver en la práctica clínica diaria. Por un lado tienen una tendencia hemorrágica debido a una alteración de la hemostasia primaria, consecuencia de una disfunción plaquetaria y una alteración de la interacción plaqueta-subendotelio1, y por otro, una tendencia trombótica motivada por múltiples factores, como daño endotelial, aumento de factores de coagulación y disminución de proteínas fibrinolíticas2. Por consiguiente, la indicación de anticoagulación ante la aparición de fibrilación auricular (FA) es compleja, y aún más ante la aparición de nuevos anticoagulantes orales que difieren en su farmacocinética renal.
El objetivo de esta contribución es clarificar las decisiones sobre la anticoagulación o no en un paciente con ERC que desarrolla FA y cuál sería el mejor fármaco anticoagulante en cada caso.
Epidemiología y factores predisponentes de la fibrilación auricular en enfermedad renal crónicaLa FA es la arritmia cardíaca crónica más frecuente y su prevalencia en la ERC es 10-20 veces mayor que en la población general3. De hecho, la FA y la ERC coinciden muy frecuentemente: un tercio de los pacientes con FA tienen ERC, y el 15% de los pacientes con ERC parecen tener FA4. En pacientes en hemodiálisis estudiados con Holter la frecuencia de FA llega hasta el 27%. No se tiene datos precisos en pacientes con ERC que no están en diálisis (tabla 1).
Prevalencia de fibrilación auricular3
| Población general<60 años: | 1% |
| Población general<80 años: | 8% |
| Pacientes en diálisis Peritoneal | 7% |
| Pacientes en hemodiálisis | 13%-27% |
Los pacientes con ERC presentan un riesgo elevado de desarrollar enfermedad cardiovascular y, al mismo tiempo y en sentido opuesto, la prevalencia de ERC es mayor en personas con enfermedad cardiovascular que en la población general, lo que se asocia a un peor pronóstico. En concreto, predisponen a la aparición de FA factores como: calcificación vascular y valvular, hipertrofia ventricular izquierda, alteraciones hidroelectrolíticas durante la sesión de diálisis e hiperactividad del sistema renina angiotensina (RAAS). Recientemente un estudio ha demostrado que la inhibición del RAAS con IECA y/o ARA2 es efectiva en la prevención primaria de la FA en pacientes en diálisis5.
Riesgo de ictus en enfermedad renal crónicaLas complicaciones más importantes de la FA son el tromboembolismo y el ictus isquémico en particular, que suelen resultar más graves en cuanto a discapacidad residual, así como a mortalidad a corto y a medio plazo6. La incidencia de ictus es mayor entre los pacientes en hemodiálisis que en la población general. En un estudio realizado en nuestro servicio de Nefrología en el Hospital Universitario Valdecilla, en Santander, la incidencia acumulada de accidentes cerebrovasculares fue del 5,8%. La tasa de incidencia en el primer año en hemodiálisis fue un 6,5% superior a la media observada a lo largo de todo el período estudiado7. Murray et al.8 observaron que el número de ictus en el primer mes en hemodiálisis incrementaba su incidencia hasta 7 veces. Lo mismo hemos encontrado nosotros en una base de datos europea de pacientes en hemodiálisis9. No están claras las razones de este aumento de incidencia en los primeros momentos de la hemodiálisis, habiéndose señalado como posibles factores la disminución de la perfusión cerebral y la velocidad del flujo sanguíneo o el incremento, en pacientes tratados con agentes estimulantes de la eritropoyesis (ESA), de la viscosidad y la resistencia vascular que pueden originar incrementos de la presión sanguínea. En la base de datos americana USRDS, la incidencia de ictus fue del 15,1% en hemodiálisis, del 9,6% en pacientes con ERC pero no en hemodiálisis y del 2,6% en pacientes sin ERC10. Vázquez et al.11, en Jaén, encontraron complicaciones tromboembólicas del 24% por año en pacientes en diálisis en FA comparados con 5% en pacientes con ritmo sinusal. En la USRDS10 se reporta un 80% más de posibilidades de ictus isquémicos en pacientes con FA con similar incidencia de ictus hemorrágicos. La presencia de ictus aumenta claramente la mortalidad en pacientes con ERC comparados con aquellos sin ERC3.
Riesgo de ictus en enfermedad renal crónica con fibrilación auricular, índice CHA2DS2-VASc vs riesgo de sangrado, índice HAS-BLEDEntre los factores asociados a ictus, en nuestro servicio encontramos diabetes, infarto de miocardio o angina de pecho, hipertensión, arteriosclerosis/claudicación intermitente y antecedentes de accidente cerebrovascular antes de la hemodiálisis7. Sin embargo, no encontramos la FA como factor asociado, al igual que otros trabajos más recientes12, pero posiblemente por no diferenciar ictus isquémico de ictus hemorrágico. En la guía de práctica clínica 2014 de la Amercican Heart Association13 se recomienda (1B) el índice CHA2DS2-VASc para evaluación del riesgo de ictus en pacientes en FA. Podemos observar que los pacientes renales tienen en su mayoría un riesgo elevado de ictus14 (tabla 2). Igualmente, podemos observar que los pacientes renales tienen un riesgo de sangrado elevado según el score HAS-BLED15 (tabla 3).
Índice CHA2DS2-VASc para valoración del riesgo de ictus en fibrilación auricular
| Factor | Puntos | |
|---|---|---|
| C | Insuficiencia cardíaca congestiva o disfunción sistólica del VI | 1 |
| H | Hipertensión arterial | 1 |
| A2 | Edad>75 años | 2 |
| D | Diabetes mellitus | 1 |
| S2 | Ictus, AIT o tromboembolismo | 2 |
| V | Enfermedad vascular (IAM previo, arteriopatía periférica, placa aórtica) | 1 |
| A | Edad 65-74 años | 1 |
| Sc | Sexo femenino | 1 |
AIT: accidente isquémico transitorio; IAM: infarto agudo de miocardio; VI: ventrículo izquierdo.
Máximo: 9 puntos. Riesgo bajo: 0; riesgo intermedio: 1; riesgo alto ≥ 2.
Fuente: Camm et al.14,
Estimación del riesgo de sangrado: HAS-BLED
| Características clínicas | Puntos | |
|---|---|---|
| H | Hipertensión sistólica ≥ 160mmHg | 1 |
| A | Insuficiencia renal y/o hepática (1 punto cada una) | 1 o 2 |
| S | Ictus | 1 |
| B | Sangrado mayor o predisposición al mismo | 1 |
| L | INR lábil (< 60% en rango terapéutico) | 1 |
| E | Edad > 65 años | 1 |
| D | Drogas o alcohol (1 punto cada uno) | 1 o 2 |
INR: international normalized ratio (ratio normalizada internacional).
Máximo: 9 puntos. Puntuación ≥ 3 indica «alto riesgo».
Fuente: Pisters et al.15.
En los últimos años la investigación se ha centrado en el desarrollo de nuevos fármacos anticoagulantes orales (NACO), con amplio margen terapéutico, escasa variabilidad, susceptibles de administrarse con una dosis fija, sin necesidad de controles dada su corta vida media y propiedades farmacocinéticas y farmacodinámicas, con pocas interacciones y un grado variable de eliminación renal.
Uno de los principales inconvenientes de los NACO era la ausencia de agentes específicos eficaces para revertir su efecto anticoagulante. Recientemente ha hecho su aparición el idarucizumab16, un agente de reversión específico para dabigatrán, indicado en pacientes adultos que precisan una reversión rápida de sus efectos anticoagulantes para intervenciones quirúrgicas de urgencia o procedimientos urgentes y en el caso de hemorragias potencialmente mortales o no controladas. Para el resto de NACO se esperan próximamente nuevos agentes específicos de reversión.
El otro gran inconveniente radica en que los NACO son más caros que los antagonistas de la vitaminaK (AVK), si bien su costo tiende a disminuir ante la llegada al mercado de nuevos medicamentos y el menor riesgo de eventos tromboembólicos y riesgo de sangrado, por lo que proporcionan un alternativa rentable en comparación con los AVK.
En la actualidad existe un inhibidor directo de la trombina (dabigatrán) y 3 inhibidores directos del factorX activado (rivaroxabán, apixabán y edoxabán), con indicaciones aprobadas en profilaxis y tratamiento antitrombótico en diferentes situaciones, que han demostrado un beneficio-riesgo favorable en diversas condiciones clínicas en las que está indicada la anticoagulación17. La utilización de estos NACO de acción directa se asocia con beneficios e inconvenientes respecto del uso de AVK, pero quizás uno de los aspectos más interesantes que clarificar es su utilización en pacientes con ERC.
Según concluye el estudio RE-LY18, dabigatrán a dosis de 110mg 2veces al día (D110) se demostró superior a warfarina en la prevención del ictus y de la embolia sistémica, presentando menor riesgo hemorrágico. A dosis de 150mg 2veces al día (D150) fue superior a warfarina en la reducción de ictus o del embolismo sistémico, sin diferencias significativas en hemorragias mayores y con mayor riesgo de hemorragias digestivas. Igualmente se constató un aumento no significativo de infartos de miocardio con ambas dosis de dabigatrán. El estudio ROCKET AF19 indica que rivaroxabán, a dosis de 20mg, frente a warfarina, no fue inferior en la prevención del ictus o de la embolia sistémica. Tampoco mostró diferencias en el riesgo de hemorragia mayor, aunque sí menor ocurrencia de hemorragia intracraneal y fatal. El estudio ARISTOTLE20 refleja que apixabán a dosis de 5mg 2veces al día mostró superioridad frente a warfarina en la prevención de ictus, de embolia sistémica y de sangrado mayor. Por su parte, el estudio AVERROES21 reflejó idéntica superioridad de apixabán respecto del ácido acetilsalicílico (AAS).
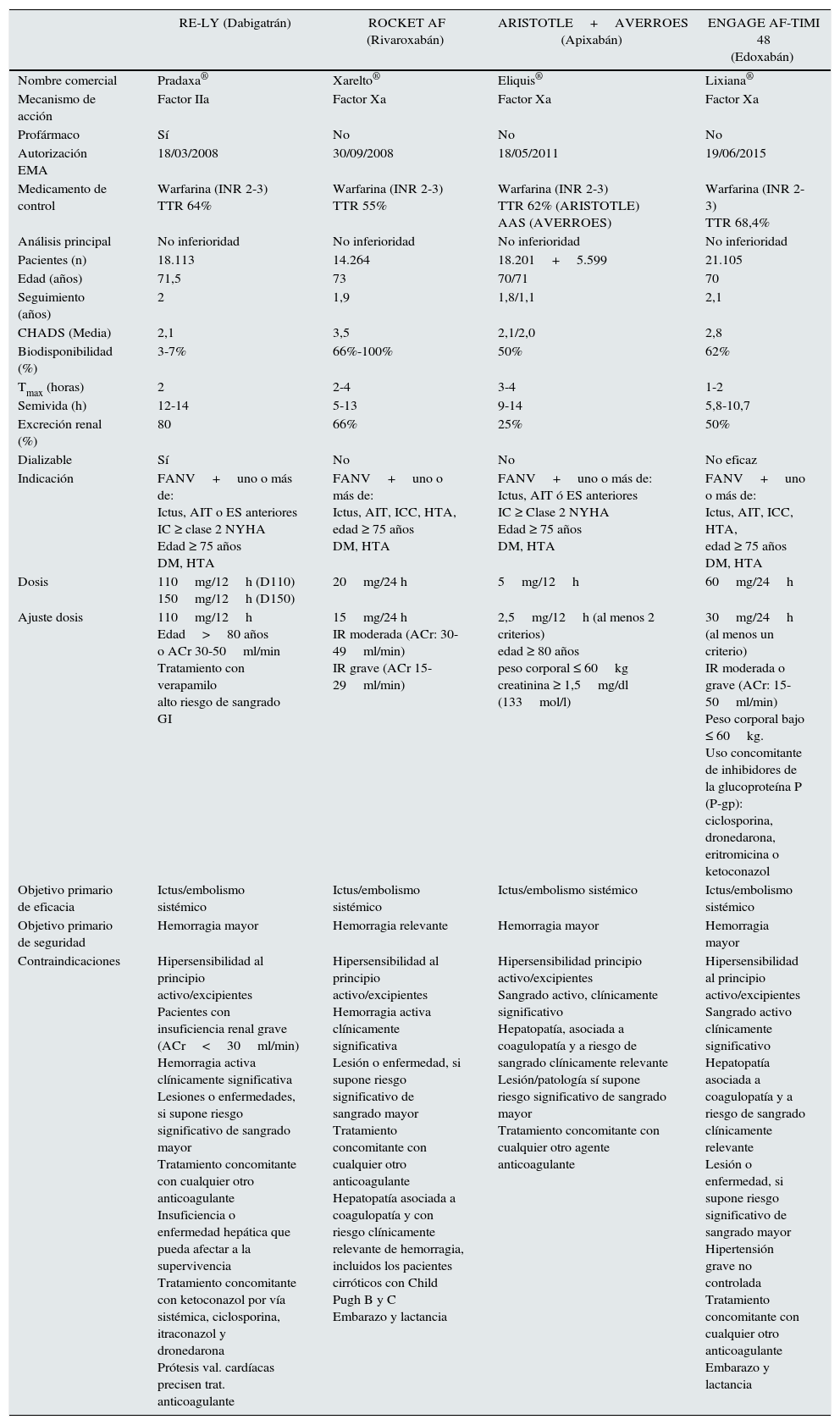
Por último, según el estudio ENGAGE AF-TIMI 4822, edoxabán a dosis de 60mg no fue inferior a warfarina en la prevención de ictus y de embolia sistémica. Respecto al sangrado mayor, así como en hemorragia intracraneal y otros tipos de sangrado, edoxabán (30/60mg) mostró una reducción significativa del riesgo en comparación con el grupo de warfarina. Las tablas 4 y 5 resumen las principales características de los 4 estudios principales que recogen la evidencia clínica de la eficacia de estos NACO.
Principales características de los ensayos clínicos de fase iii en la prevención embólica en pacientes con fibrilación auricular no valvular
| RE-LY (Dabigatrán) | ROCKET AF (Rivaroxabán) | ARISTOTLE+AVERROES (Apixabán) | ENGAGE AF-TIMI 48 (Edoxabán) | |
|---|---|---|---|---|
| Nombre comercial | Pradaxa® | Xarelto® | Eliquis® | Lixiana® |
| Mecanismo de acción | Factor IIa | Factor Xa | Factor Xa | Factor Xa |
| Profármaco | Sí | No | No | No |
| Autorización EMA | 18/03/2008 | 30/09/2008 | 18/05/2011 | 19/06/2015 |
| Medicamento de control | Warfarina (INR 2-3) TTR 64% | Warfarina (INR 2-3) TTR 55% | Warfarina (INR 2-3) TTR 62% (ARISTOTLE) AAS (AVERROES) | Warfarina (INR 2-3) TTR 68,4% |
| Análisis principal | No inferioridad | No inferioridad | No inferioridad | No inferioridad |
| Pacientes (n) | 18.113 | 14.264 | 18.201+5.599 | 21.105 |
| Edad (años) | 71,5 | 73 | 70/71 | 70 |
| Seguimiento (años) | 2 | 1,9 | 1,8/1,1 | 2,1 |
| CHADS (Media) | 2,1 | 3,5 | 2,1/2,0 | 2,8 |
| Biodisponibilidad (%) | 3-7% | 66%-100% | 50% | 62% |
| Tmax (horas) | 2 | 2-4 | 3-4 | 1-2 |
| Semivida (h) | 12-14 | 5-13 | 9-14 | 5,8-10,7 |
| Excreción renal (%) | 80 | 66% | 25% | 50% |
| Dializable | Sí | No | No | No eficaz |
| Indicación | FANV+uno o más de: Ictus, AIT o ES anteriores IC ≥ clase 2 NYHA Edad ≥ 75 años DM, HTA | FANV+uno o más de: Ictus, AIT, ICC, HTA, edad ≥ 75 años DM, HTA | FANV+uno o más de: Ictus, AIT ó ES anteriores IC ≥ Clase 2 NYHA Edad ≥ 75 años DM, HTA | FANV+uno o más de: Ictus, AIT, ICC, HTA, edad ≥ 75 años DM, HTA |
| Dosis | 110mg/12h (D110) 150mg/12h (D150) | 20mg/24 h | 5mg/12h | 60mg/24h |
| Ajuste dosis | 110mg/12h Edad>80 años o ACr 30-50ml/min Tratamiento con verapamilo alto riesgo de sangrado GI | 15mg/24 h IR moderada (ACr: 30-49ml/min) IR grave (ACr 15-29ml/min) | 2,5mg/12h (al menos 2 criterios) edad ≥ 80 años peso corporal ≤ 60kg creatinina ≥ 1,5mg/dl (133mol/l) | 30mg/24h (al menos un criterio) IR moderada o grave (ACr: 15-50ml/min) Peso corporal bajo ≤ 60kg. Uso concomitante de inhibidores de la glucoproteína P (P-gp): ciclosporina, dronedarona, eritromicina o ketoconazol |
| Objetivo primario de eficacia | Ictus/embolismo sistémico | Ictus/embolismo sistémico | Ictus/embolismo sistémico | Ictus/embolismo sistémico |
| Objetivo primario de seguridad | Hemorragia mayor | Hemorragia relevante | Hemorragia mayor | Hemorragia mayor |
| Contraindicaciones | Hipersensibilidad al principio activo/excipientes Pacientes con insuficiencia renal grave (ACr<30ml/min) Hemorragia activa clínicamente significativa Lesiones o enfermedades, si supone riesgo significativo de sangrado mayor Tratamiento concomitante con cualquier otro anticoagulante Insuficiencia o enfermedad hepática que pueda afectar a la supervivencia Tratamiento concomitante con ketoconazol por vía sistémica, ciclosporina, itraconazol y dronedarona Prótesis val. cardíacas precisen trat. anticoagulante | Hipersensibilidad al principio activo/excipientes Hemorragia activa clínicamente significativa Lesión o enfermedad, si supone riesgo significativo de sangrado mayor Tratamiento concomitante con cualquier otro anticoagulante Hepatopatía asociada a coagulopatía y con riesgo clínicamente relevante de hemorragia, incluidos los pacientes cirróticos con Child Pugh B y C Embarazo y lactancia | Hipersensibilidad principio activo/excipientes Sangrado activo, clínicamente significativo Hepatopatía, asociada a coagulopatía y a riesgo de sangrado clínicamente relevante Lesión/patología sí supone riesgo significativo de sangrado mayor Tratamiento concomitante con cualquier otro agente anticoagulante | Hipersensibilidad al principio activo/excipientes Sangrado activo clínicamente significativo Hepatopatía asociada a coagulopatía y a riesgo de sangrado clínicamente relevante Lesión o enfermedad, si supone riesgo significativo de sangrado mayor Hipertensión grave no controlada Tratamiento concomitante con cualquier otro anticoagulante Embarazo y lactancia |
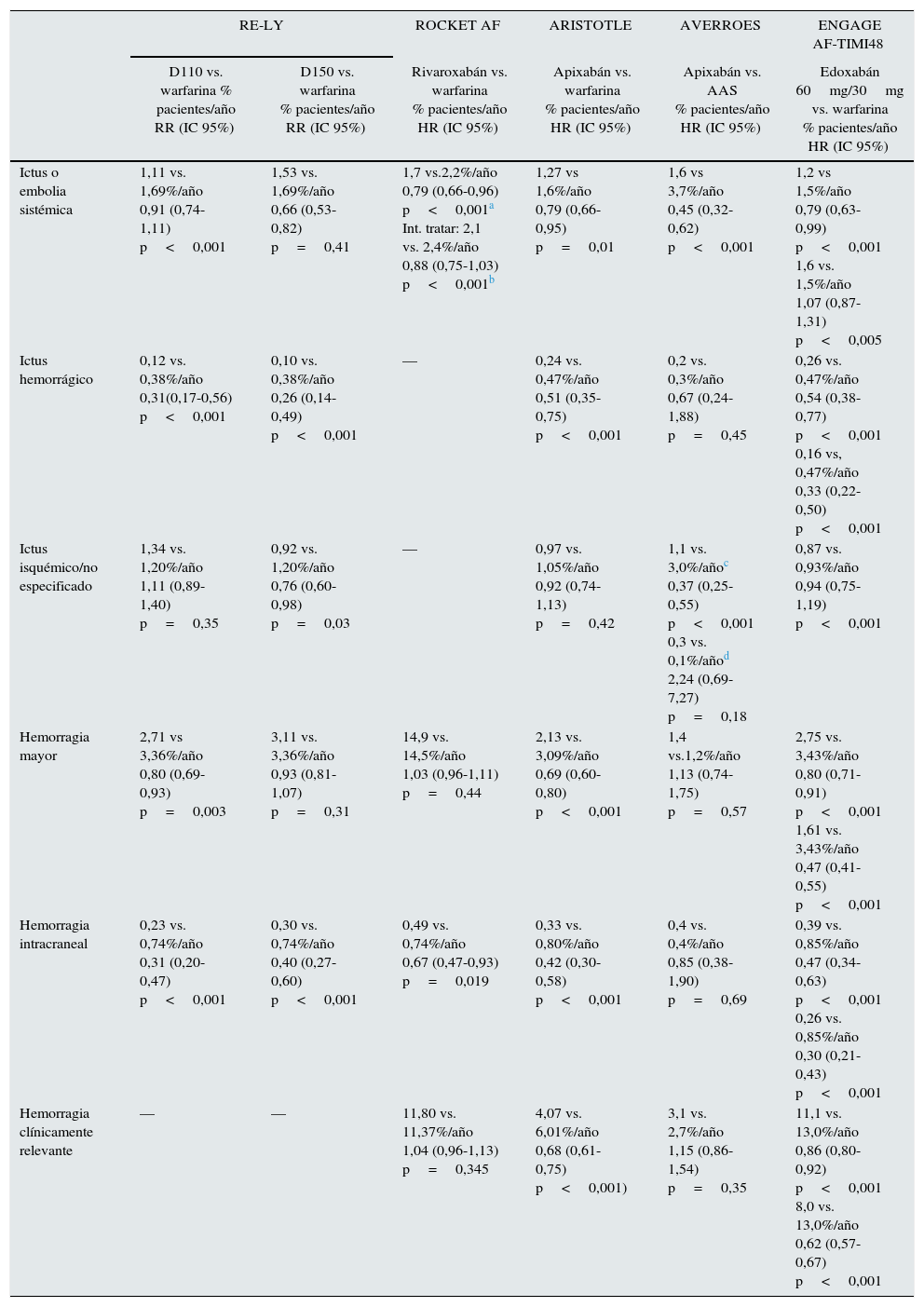
Principales resultados de eficacia y seguridad de ensayos clínicos de fase iii en la prevención embólica en pacientes con fibrilación auricular no valvular
| RE-LY | ROCKET AF | ARISTOTLE | AVERROES | ENGAGE AF-TIMI48 | ||
|---|---|---|---|---|---|---|
| D110 vs. warfarina % pacientes/año RR (IC 95%) | D150 vs. warfarina % pacientes/año RR (IC 95%) | Rivaroxabán vs. warfarina % pacientes/año HR (IC 95%) | Apixabán vs. warfarina % pacientes/año HR (IC 95%) | Apixabán vs. AAS % pacientes/año HR (IC 95%) | Edoxabán 60mg/30mg vs. warfarina % pacientes/año HR (IC 95%) | |
| Ictus o embolia sistémica | 1,11 vs. 1,69%/año 0,91 (0,74-1,11) p<0,001 | 1,53 vs. 1,69%/año 0,66 (0,53-0,82) p=0,41 | 1,7 vs.2,2%/año 0,79 (0,66-0,96) p<0,001a Int. tratar: 2,1 vs. 2,4%/año 0,88 (0,75-1,03) p<0,001b | 1,27 vs 1,6%/año 0,79 (0,66-0,95) p=0,01 | 1,6 vs 3,7%/año 0,45 (0,32-0,62) p<0,001 | 1,2 vs 1,5%/año 0,79 (0,63-0,99) p<0,001 1,6 vs. 1,5%/año 1,07 (0,87-1,31) p<0,005 |
| Ictus hemorrágico | 0,12 vs. 0,38%/año 0,31(0,17-0,56) p<0,001 | 0,10 vs. 0,38%/año 0,26 (0,14-0,49) p<0,001 | — | 0,24 vs. 0,47%/año 0,51 (0,35-0,75) p<0,001 | 0,2 vs. 0,3%/año 0,67 (0,24-1,88) p=0,45 | 0,26 vs. 0,47%/año 0,54 (0,38-0,77) p<0,001 0,16 vs, 0,47%/año 0,33 (0,22-0,50) p<0,001 |
| Ictus isquémico/no especificado | 1,34 vs. 1,20%/año 1,11 (0,89-1,40) p=0,35 | 0,92 vs. 1,20%/año 0,76 (0,60-0,98) p=0,03 | — | 0,97 vs. 1,05%/año 0,92 (0,74-1,13) p=0,42 | 1,1 vs. 3,0%/añoc 0,37 (0,25-0,55) p<0,001 0,3 vs. 0,1%/añod 2,24 (0,69-7,27) p=0,18 | 0,87 vs. 0,93%/año 0,94 (0,75-1,19) p<0,001 |
| Hemorragia mayor | 2,71 vs 3,36%/año 0,80 (0,69-0,93) p=0,003 | 3,11 vs. 3,36%/año 0,93 (0,81-1,07) p=0,31 | 14,9 vs. 14,5%/año 1,03 (0,96-1,11) p=0,44 | 2,13 vs. 3,09%/año 0,69 (0,60-0,80) p<0,001 | 1,4 vs.1,2%/año 1,13 (0,74-1,75) p=0,57 | 2,75 vs. 3,43%/año 0,80 (0,71-0,91) p<0,001 1,61 vs. 3,43%/año 0,47 (0,41-0,55) p<0,001 |
| Hemorragia intracraneal | 0,23 vs. 0,74%/año 0,31 (0,20-0,47) p<0,001 | 0,30 vs. 0,74%/año 0,40 (0,27-0,60) p<0,001 | 0,49 vs. 0,74%/año 0,67 (0,47-0,93) p=0,019 | 0,33 vs. 0,80%/año 0,42 (0,30-0,58) p<0,001 | 0,4 vs. 0,4%/año 0,85 (0,38-1,90) p=0,69 | 0,39 vs. 0,85%/año 0,47 (0,34-0,63) p<0,001 0,26 vs. 0,85%/año 0,30 (0,21-0,43) p<0,001 |
| Hemorragia clínicamente relevante | — | — | 11,80 vs. 11,37%/año 1,04 (0,96-1,13) p=0,345 | 4,07 vs. 6,01%/año 0,68 (0,61-0,75) p<0,001) | 3,1 vs. 2,7%/año 1,15 (0,86-1,54) p=0,35 | 11,1 vs. 13,0%/año 0,86 (0,80-0,92) p<0,001 8,0 vs. 13,0%/año 0,62 (0,57-0,67) p<0,001 |
Tras su comercialización y varios años de uso se han publicado diversos estudios sobre su eficacia y seguridad en la práctica clínica habitual, que en su mayoría vienen a ratificar las conclusiones de los estudios que sustentan la evidencia clínica de estos NACO.
Una revisión sistemática y metaanálisis de Miller et al.23 asigna a los NACO (dabigatrán, rivaroxabán, apixabán vs. warfarina) una reducción del riesgo para todas las causas de ictus y embolia sistémica, accidente cerebrovascular isquémico y no identificado, accidente cerebrovascular hemorrágico, todas las causas de mortalidad y la mortalidad vascular. Igualmente se asociaron con un menor riesgo de hemorragia intracraneal. Sin embargo, los datos sobre hemorragia grave y hemorragia digestiva no fueron concluyentes.
Un metaanálisis de los 4 ensayos principales de Ruff et al.24 constató que los NACO, en comparación con warfarina, reducen significativamente la tasa de accidente cerebrovascular y la embolia sistémica. Sin embargo, salvo la excepción de apixabán, los NACO se asociaron con un aumento del riesgo de hemorragia gastrointestinal. Otro reciente metaanálisis determina, excepto para D110 y edoxabán 30mg, la superioridad de los NACO frente a los AVK en el objetivo primario de eficacia de reducción de ictus-embolismo; apixabán y edoxabán presentaron un menor número de eventos de sangrado que D150, rivaroxabán y AVK. Sin embargo, D110 y D150 se asociaron con una incidencia mayor de infarto de miocardio en comparación con apixabán, edoxabán 60mg y rivaroxabán25. Si bien algunos otros estudios asocian al dabigatrán con un aumento del riesgo de infarto de miocardio26, la Food and Drug Administration (FDA) ha concluido, tras el análisis de los datos de 134.000 pacientes de Medicare, que en la práctica real la incidencia de infarto de miocardio fue similar con dabigatrán y warfarina27.
En el análisis de subgrupos no existen referencias de uso en población pediátrica, y por supuesto en mujeres gestantes o durante el periodo de lactancia. Un metaanálisis de género de Pancholy et al.28 sugiere un beneficio clínico neto de los NACO en comparación con la warfarina en el tratamiento de las mujeres con fibrilación auricular no valvular (FANV). Otros estudios sobre grupos de pacientes con o sin ictus-accidente isquémico transitorio (AIT) previos o insuficiencia cardiaca sintomática vinieron a corroborar, en relación con el objetivo primario de eficacia de reducción de ictus y embolia sistémica, la superioridad de D150, mientras D110, apixabán y rivaroxabán, no eran inferiores a warfarina, lo que era consistente con los resultados observados en los estudios principales previos29-31.
Criterios de anticoagulación en pacientes con fibrilación auricularAdemás de intentar revertir a ritmo sinusal en los casos en que esté indicado, o controlar la frecuencia cardíaca en las personas con FA persistente o permanente, la prevención de los fenómenos embólicos debe acompañar a ambas estrategias.
Los anticoagulantes clásicos por excelencia son los AVK. El tratamiento anticoagulante con AVK reduce el riesgo de ictus en un 67% y de mortalidad por todas las causas en un 26%32. Sin embargo, sus perfiles farmacocinéticos y farmacodinámicos se ven afectados de forma importante por múltiples interacciones farmacológicas y polimorfismos genéticos, así como por la ingesta de vitaminaK en la dieta, lo que obliga a mantener una continua vigilancia clínica con objeto de intentar mantener el international normalized ratio (INR) en rango terapéutico entre 2 y 333.
El tiempo en que los pacientes están en rango terapéutico influye en los resultados del fármaco, de tal forma que estarlo el 70% del tiempo disminuye el riesgo de ictus a la quinta parte en comparación con aquellos que solo lo están el 30% del tiempo. También decrece el riesgo de sangrado, de muerte y de infarto de miocardio34.
Dos recientes revisiones Cochrane estudian los efectos de los anticoagulantes orales en la prevención del ictus. En pacientes sin historia previa de ictus35 el tratamiento con acenocumarol con INR entre 2-3 reduce los episodios de ictus y muerte en pacientes con FA no valvular. En pacientes con antecedentes de ictus los anticoagulantes orales se asociaron con un aumento significativo en el riesgo de hemorragias extracraneales graves36. En la guía de práctica clínica 2014 de la American Heart Association (AHA)37 en pacientes con FA no valvular con ictus previo, episodio isquémico transitorio o CHA2DS2-VASc score ≥2 se recomiendan anticoagulantes orales: warfarina con INR 2-3 (evidenciaA), dabigatrán (evidenciaB), rivaroxabán (evidenciaB) o apixabán (evidenciaB).
Criterios de anticoagulación en pacientes con fibrilación auricular y enfermedad renal crónica avanzada. ControversiaUno de los problemas para conocer la eficacia de los anticoagulantes en pacientes con ERC es que aquellos con estadios avanzados de ERC han sido normalmente excluidos en los principales ensayos ante el importante grado de excreción renal (dabigatrán, 80%; rivaroxabán, 1/3 directamente como principio activo no modificado, así como la mitad de los 2/3 restantes, y un 25 y un 35% en los casos de apixabán y edoxabán, respectivamente).
El número de pacientes con ERC estadio4 incluidos en los estudios RE-LY y ROCKET-AF con dabigatrán y rivaroxabán, respectivamente, es pequeño y no permite extraer conclusiones, a pesar de lo cual la FDA ha aprobado una dosis reducida de dabigatrán de 75mg 2veces al día basándose exclusivamente en datos farmacocinéticos y farmacodinámicos, y algunas agencias han aprobado rivaroxabán a dosis de 15mg en esta población. Se aconsejan dosis reducidas de apixabán (2,5mg/12h) y edoxabán (30mg/24h). Podemos añadir, no obstante, que tampoco existen datos relevantes a este respecto con AVK en ERC estadio4, a pesar de lo cual se recomienda su utilización en las guías canadienses de tratamiento de la FA
Respecto a los pacientes con ERC estadio5, la guía de la AHA precisa los siguientes términos:
- •
En pacientes con FA no valvular y CHA2DS2-VASc score ≥2 con aclaramiento de creatinina (Acr)<15ml/min) o en hemodiálisis, se aconseja anticoagulación con warfarina (INR 2,0-3,0) (evidenciaB).
- •
Respecto a los nuevos anticoagulantes orales, no se recomiendan en pacientes Acrl<15ml/min o en hemodiálisis por ausencia de evidencia en ensayos clínicos de un balance riesgo beneficio (tabla 6).
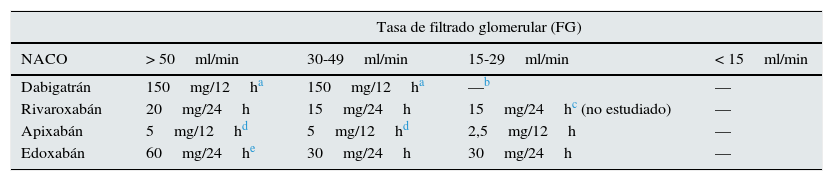
Tabla 6.Dosis recomendadas de nuevos fármacos anticoagulantes orales (NACO) según tasas de filtrado glomerular
Tasa de filtrado glomerular (FG) NACO > 50ml/min 30-49ml/min 15-29ml/min < 15ml/min Dabigatrán 150mg/12ha 150mg/12ha —b — Rivaroxabán 20mg/24h 15mg/24h 15mg/24hc (no estudiado) — Apixabán 5mg/12hd 5mg/12hd 2,5mg/12h — Edoxabán 60mg/24he 30mg/24h 30mg/24h — aEn pacientes con alto riesgo de sangrado se debe considerar una reducción de la dosis a 220mg (110mg/12h).
bLa FDA autoriza una dosis de 75mg/12h para los pacientes con Acr 15-30ml/min basándose en modelos farmacocinéticos. Las demás agencias reguladoras contraindican el dabigatrán si ACr<30ml/min.
Sin embargo, la indicación de warfarina en pacientes en estadio5 de ERC (FG<15ml/min o diálisis) es controvertida. Olesen et al.38 concluyen en favor de la anticoagulación con acenocumarol. En pacientes con FA, la ERC aumenta el riesgo de ictus, tromboembolismo y hemorragia, y la anticoagulación con warfarina, al igual que en los pacientes sin ERC, reduce el riesgo de ictus y tromboembolismo, aumentando el riesgo de sangrado. El AAS aumenta el riesgo de sangrado pero sin reducir los episodios de ictus o tromboembolismo.
Pero hay 3 publicaciones de registros amplios que concluyen que en pacientes con FA en hemodiálisis la anticoagulación con warfarina se asoció a un aumento en el riesgo de ictus39-41. Además, en pacientes en hemodiálisis anticoagulados con warfarina aumentan los riesgos de sangrado y de calcificación vascular y calcifilaxis42.
En consecuencia, se desaconseja el uso de acenocumarol en la prevención de eventos tromboembólicos en pacientes en diálisis con FA no valvular. De hecho, la Sociedad Europea de Cardiología, debido a la falta de evidencia, expresa lo siguiente: «la ERC puede aumentar el riesgo de tromboembolismo en la FA, aunque estos pacientes también tienen mayor riesgo de mortalidad y hemorragia y no hay estudios prospectivos»14.
Comparación entre nuevos anticoagulantes orales. Criterios de elecciónHasta la fecha no se han publicado estudios en los que se lleve a cabo una comparación directa entre estos 4 NACO, por lo que resulta complicado formular opiniones sobre la superioridad de alguno de ellos. Un estudio de Schneeweiss et al.43, en el que se efectuaba la comparación indirecta entre dabigatrán, rivaroxabán y apixabán, indicaba que en pacientes con un CHADS2 ≥3, D150mg, apixabán 5mg y rivaroxabán 20mg resultaron estadísticamente similares en tasas de ictus y embolia sistémica, pero apixabán tenía un menor riesgo de hemorragia mayor en comparación con dabigatrán y rivaroxabán. Otro reciente metaanálisis de Fu et al.44 lleva a cabo comparaciones indirectas de la seguridad y eficacia de estos 4 NACO. Comparado con D150, rivaroxabán y edoxabán 30mg mostraron de forma significativa mayor riesgo de ictus o embolia sistémica, y rivaroxabán mayor riesgo de ictus hemorrágico. Existía mayor riesgo de ictus o embolia sistémica, cualquier AIT, ictus isquémicos y AIT incapacitante o fatal para edoxabán 30mg en comparación con apixabán y rivaroxabán, salvo para este último en lo relativo a ictus o embolia sistémica. Apixabán, rivaroxabán y edoxabán 60mg podrían significativamente reducir el riesgo de infarto de miocardio en comparación con D150. En relación a la variable de seguridad, los riesgos de hemorragia mayor, gastrointestinal y cualquier tipo de sangrado fueron de forma significativa mayores con rivaroxabán que con apixabán y D110, al igual que con edoxabán 60mg frente a edoxabán 30mg. Edoxabán 30mg mostró reducciones significativas de hemorragia mayor frente al resto de NACO, así como frente a D150, D110 y rivaroxabán.
Ante la ausencia de estudios comparativos directos entre estos NACO, la selección de uno u otro dependerá de la percepción del médico sobre el beneficio en cada estudio, de las recomendaciones específicas aceptadas por las agencias reguladoras y, sobre todo, de las restricciones económicas (necesarias) impuestas por los diferentes organismos de financiación, incluida aquí la capacidad adquisitiva del paciente. Una reciente revisión sistemática sobre 23 estudios de Ferreira et al.45 concluye que los NACO son rentables para la prevención del ictus en la FA y, sin analizar edoxabán, dada su muy reciente aprobación, parece que apixabán es el más rentable, seguido de dabigatrán y de rivaroxabán. No obstante, dadas las limitaciones de los distintos modelos de análisis utilizados, y en tanto no se lleven a cabo estudios adicionales, estos resultados deben tomarse con la debida precaución.
Conceptos clave- •
La FA es la arritmia cardíaca crónica más frecuente, y su prevalencia en la ERC es 10-20 veces mayor que en la población general, con un aumento de la frecuencia de ictus isquémico a medida que la función renal declina.
- •
Los AVK reducen el riesgo de ictus y de mortalidad por todas las causas. Sin embargo, sus perfiles farmacocinéticos y farmacodinámicos se ven afectados de forma importante por múltiples interacciones farmacológicas y polimorfismos genéticos, así como por la ingesta de vitaminaK en la dieta.
- •
Los NACO, además de un amplio margen terapéutico, poseen escasa variabilidad, un rápido inicio de acción y una vida media corta, son susceptibles de administrarse con una dosis fija sin necesidad de monitorización dadas sus propiedades farmacocinéticas y farmacodinámicas, cuentan con escasas interacciones y presentan un grado variable de eliminación renal.
- •
En la actualidad existe un inhibidor directo de la trombina (dabigatrán) y 3 inhibidores directos del factorX activado (rivaroxabán, apixabán y edoxabán), con indicaciones aprobadas para la prevención del ictus y de la embolia sistémica en pacientes adultos con FANV.
- •
Para aclaramientos entre 30 y 50ml/min hay que reducir la dosis con dabigatrán (si existe alto riesgo de sangrado) y rivaroxabán, y no es necesario reducir dosis con apixabán y edoxabán. Para aclaramientos entre 15-29ml/min, dabigatrán está contraindicado, rivaroxabán y edoxabán no precisan ajuste, mientras apixabán sí. Ninguno de los NACO está indicado para aclaramientos inferiores a 15ml/min.
- •
En la actualidad existe un agente de reversión específico para dabigatrán, indicado en pacientes que precisen cirugía o con hemorragias graves. Para el resto de NACO se esperan próximamente nuevos agentes específicos de reversión.
- •
Los NACO son más caros que los AVK. Sin embargo, su costo tiende a disminuir ante la llegada al mercado de nuevos medicamentos. No obstante, el menor riesgo de eventos tromboembólicos y de sangrado proporciona una alternativa rentable en comparación con los AVK.
Los autores declaran no tener ningún conflicto de intereses.