Objetivo: Describir el funcionamiento del Registro Español Pediátrico de Insuficiencia Renal (REPIR II), dar a conocer la epidemiología de la enfermedad y estudiar aquellos factores que puedan influir en el curso de ésta. Material y métodos: En el REPIR II participan 46 centros distribuidos por toda la geografía española. Para la clasificación y la valoración de la comorbilidad de la enfermedad, hemos utilizado los criterios de las Guías de Práctica Clínica K/DOQI. Cada centro aporta, con una periodicidad anual, los datos evolutivos de cada paciente, que quedan registrados en una base de datos on-line. Criterios de inclusión: Pacientes diagnosticados de enfermedad renal crónica (ERC) que se encuentren entre el estadio 2 y 5 en predialisis y con una edad igual o inferior a 18 años. Resultados: En el año 2008 se habían incluido 605 pacientes de 37 centros; la incidencia de la ERC no terminal era de 8,66 por millón de población (ppm) menores 18 años y la prevalencia de 71,06. La patología estructural era la primera causa de ERC (59% de casos). El porcentaje de glomerulopatías fue muy reducido (3%). Había un claro predominio de hombres (66%) y de la raza caucásica (88%). El valor medio del GFR era de 52 ± 2 ml/min/1,73 m2, con un 82% de pacientes en estadios 2 y 3. La prevalencia de la anemia era del 30%. Solamente el 19% de nuestros pacientes presentaban HTA y únicamente el 17% de ellos cumplían las cuatro recomendaciones de las Guías K/DOQI sobre el metabolismo calcio-fósforo. El valor medio global del Z-Score de la talla era del —1,03 ± 2. Había 136 pacientes (25%) que tenían un Z-Score de la talla ≤1,88. En un análisis de regresión logística multivariante, sólo se detectó una relación significativa entre la edad y la talla baja. Los menores de 2 años tenían una probabilidad un 40% mayor de tener una talla baja (OR = 1,40; p <0,01). El porcentaje de malnutrición (Z-Score de IMC ≤1,88) era del 7%, la mayoría en el grupo de edad de 0-2 años. Conclusiones: Presentamos el primer estudio que realiza un análisis prospectivo sobre la incidencia, prevalencia, etiología y comorbilidad de la ERC en la población pediátrica del estado español. Teniendo en cuenta la corta vida de este registro, los datos presentados son provisionales, y pueden estar sometidos a cambios importantes en los próximos años.
Objective: A national registry of children with Chronic Kidney Disease (CKD) was started in 2007. We analize it to know the incidence, prevalence, demography, etiology, clinical and metabolic state of the children with CKD, in stages 2-5 pre-dialysis, and complying with the K/DOQI guidelines. Material and methods: In the REPIR II 46 centers distributed throughout the Spanish geography are involved. To classify and evaluate comorbidity of the disease, the Clinical Practice Guidelines K/DOQI criteria are used. Each center provides an annual developmental data of each patient which is recorded in a On-line database. Inclusion criteria: patients with CKD who are between stage 2 and 5 in predialysis and which are 18 years old or less. Results: In 2008 there were 605 patients with CKD, the incidence was 8.66 per million of pediatric population (pmpp) and the prevalence was 71.06 pmpp. Structural anomalies was the primary cause of CKD (59% of the cases). The percentage of glomerular diseases was very low (3%). There was a clear predominance of males (66%) and Caucasian race (88%). Mean GFR was 52 ± 2 ml/min/1.73 m2 with 82% of them in stage 2 and 3. The prevalence of anaemia was 30%. Only 19% of our patients had hypertension and only 17% of them fulfilled the 4 recommendations for calcium-phosphorus metabolism of K/DOQI Guidelines. Mean height Z-Score was —1.03 ± 2. There were 136 patients (25%) who had a mean height Z-Score of size < —1.88. In a multivariate logistic regression analysis only a meaningful relationship between age and height was identified. All the children under 2 years old had a 40% higher probability of having a short height (OR = 1.40; P <0.01). The percentage of malnutrition (BMI Z-Score < 1.88) was 7%, mostly in the 0-2 years old group. Conclusions: We report the first study that performs a prospective analysis of incidence, prevalence, etiology and comorbidity of CKD in the pediatric population of the Spanish State. Given the short life of this record the data presented is provisional and may suffer meanful changes in coming years.
INTRODUCCIÓN
La enfermedad renal crónica (ERC) en la edad pediátrica es poco frecuente, pero cuando aparece sus efectos son devastadores para el desarrollo del niño, generando una alta morbilidad.
La mayoría de los pacientes se encuentran en etapas poco avanzadas de la enfermedad, en las que todavía pueden aplicarse intervenciones terapéuticas que cambien su curso. Un número reducido de pacientes evolucionan cada año hacia enfermedad renal crónica terminal (ERCT) en la que la única medida terapéutica posible es el tratamiento sustitutivo (diálisis-trasplante). De ahí la importancia del diagnóstico precoz1.
La información sobre las características de la ERC en pediatría es bastante limitada y se ha extraído preferentemente de pacientes que se encontraban en fases terminales de la enfermedad2,3.
Los datos de los que se dispone se refieren a pequeñas poblaciones en áreas geográficas concretas, en ocasiones no referidas a la población general. En los registros existentes, la metodología utilizada para clasificar y graduar la enfermedad renal no ha sido uniforme, lo que ha dificultado la realización de comparaciones sobre las características de la enfermedad entre las distintas áreas geográficas4-6.
Entre los registros vigentes en la actualidad cabe mencionar el de la European Diálisis Transplant Asociation (EDTA) que en la actualidad recopila los datos de 12 registros europeos de pacientes en situación terminal y en tratamiento sustitutivo (diálisis-trasplante)7, el Registro de Australia y Nueva Zelanda8, el de Lorrain en Francia y el Registro Chileno, entre otros. La Sociedad Japonesa de Nefrología Pediátrica ha proporcionado informes muy valiosos sobre la ERC.
El registro Americano, The Registry of the North American Pediatric Renal Trials and Collaborative Studies Organization (NAPRTCSC)9, se inició en 1987 con el objetivo de recoger los datos de la mayoría de los centros de trasplante renal pediátricos de EE.UU., Canadá, México y Costa Rica. En 1992 se incluyeron también los datos de los pacientes que se encontraban en diálisis. A partir de 1994 se incorporaron al registro, todos los pacientes menores de 20 años en situación de ERC no terminal con un GFR < 75 ml/min/1,73 m2, de manera que a fecha de 31 de diciembre de 2008 estaban ya incluidos en el registro 7.037 pacientes con ERC no terminal. La participación en este registro es voluntaria y su principal inconveniente radica en que sólo están incluidos el 75%, aproximadamente, de todos los pacientes americanos con ERC.
En 2003 se publicaron los datos del registro italiano ITALKID10. Se trata de un proyecto prospectivo que incluye a todos los pacientes pediátricos con ERC del estado italiano. Es el proyecto más completo sobre la epidemiología de la ERC en el niño. Se inició en 1990 y se refiere a una población infantil total de 16,8 millones de niños.
En el año 2007, la Asociación Española de Nefrología Pediátrica (AENP) puso en marcha el Registro Español Pediátrico de Insuficiencia Renal (REPIR II) en el que se pretende incluir a todos los pacientes pediátricos con ERC no terminal del estado español. El objetivo de este registro es conocer la incidencia y prevalencia de la ERC infantil, describir la historia natural de la enfermedad, estudiar aquellos factores que puedan influir en el curso de la misma y elaborar un protocolo estándar para la vigilancia y el tratamiento de estos pacientes.
Este trabajo describe las características del proyecto REPIR II en sus comienzos y aporta los primeros datos de incidencia y prevalencia sobre la ERC no terminal en la edad pediátrica de nuestro pais.
MATERIAL Y MÉTODOS
Dentro de la AENP en el año 2007 se creó una comisión encargada de llevar a cabo el proyecto REPIR II. Dicha comisión está constituida por un presidente, 2 coordinadores y 10 representantes de todos los centros participantes en el proyecto. El número de centros participantes es de 46 y están distribuidos por toda la geografía española en representación de todas la autonomías que constituyen el estado español. En cada centro existe un médico pediatra responsable del control de todos los niños con enfermedades renales de la región correspondiente, que es el investigador responsable de incluir en el registro a todos los pacientes que, teniendo una ERC no terminal, cumplan los criterios de inclusión establecidos. A su vez, tiene la responsabilidad de aportar al registro, con una periodicidad anual, los datos evolutivos de cada uno de sus pacientes registrados, los cuales deben referirse a la última visita anterior a cada 31 de diciembre del año en curso.
Clasificación de la enfermedad renal crónica
En este registro hemos adoptado la clasificación de la ERC descrita por las Guías de Práctica Clínica (GPC) The National Kidney Foundation's Kidney Disease Outcomes Quality Initiative (Guías K/DOQI)11, que gradúa la gravedad de la enfermedad en cinco estadios: estadio 1, cuando el GFR es > 90 ml/min/1,73 m2, estadio 2 cuando se encuentra entre 89 y 60 ml/min/1,73 m2, estadio 3 cuando se encuentra entre 59 y 30, estadio 4 cuando está entre 29 y 15, y estadio 5 si es < 15 ml/min/1m73 m2.
Criterios de inclusión
Solamente se pueden incluir en el registro aquellos niños que, teniendo una edad igual o inferior a 18 años, hayan sido diagnosticados de una ERC que se encuentre entre el estadio 2 y el estadio 5 de la clasificación de las Guías K/DOQI. Tras iniciar el tratamiento sustitutivo (diálisis o trasplante), aunque los datos quedan almacenados en la base de datos, el paciente debe ser trasladado a otra base de datos, el REPIR I, que registra exclusivamente a los casos que se encuentran en programa de diálisis-trasplante.
Como las Guías K/DOQI no incluyen a pacientes menores de 2 años, para conocer el estadio en que se encuentra la enfermedad renal de estos niños hemos extrapolado el porcentaje de pérdida de función renal en cada estadio de las Guías K/DOQI, teniendo en cuenta los valores de referencia del GFR en los niños de 0 a 24 meses de edad.
Para poder incluir a un paciente en el registro es necesario, también, que la disminución del GFR se mantenga como mínimo durante 3 meses evitando así que se registren pacientes que recuperan función y que, por tanto, no cumplen los criterios de inclusión.
La valoración del GFR se lleva a cabo según la fórmula de Schwartz12:
GFR en ml/min/1,73 m2 = K x T/PCr
donde: la K es una constante cuyo valor varía con la edad (en los < 2 años su valor es 0,45; de 2 a 16 años es de 0,55, y de 16 a los 21 años es de 0,70 en los hombres y de 0,55 en las mujeres); la T es la talla en cm y la PCr es la concentración de creatinina en sangre expresada en mg/dl.
En la base de datos también existe la posibilidad de valorar el GFR, utilizando la cistatina C según la fórmula de Filler13. No obstante, el criterio de inclusión de un paciente se basa exclusivamente en el GFR estimado por la fórmula de Schwartz.
Para definir la presencia de anemia se han seguido los criterios de las Guías K/DOQI, que utilizan los valores de referencia de la hemoglobina (Hb) de la NHANES III14, considerando que un paciente tiene anemia cuando su Hb se encuentra por debajo del percentil 5 para su edad y su sexo.
Para definir la existencia de hipertensión arterial (HTA) hemos utilizado los valores de referencia de la tensión arterial (TA) de la Task Force obtenidos de una población normal con una edad igual o menor a 18 años15. Hemos considerado que un paciente es hipertenso cuando la tensión arterial sistólica (TAS) y/o la tensión arterial diastólica (TAD) se encuentran por encima del percentil 90 para su sexo, su edad y su talla.
Para valorar la situación del metabolismo calcio-fósforo, hemos utilizado los criterios aconsejados por las Guías KDOQI16 para cuatro parámetros (calcio, fósforo, producto Ca x P y PTH), los cuales deben mantenerse, según la edad y estadio de la ERC, entre los rangos de referencia indicados en dichas Guías.
Base de datos
El registro dispone de una base de datos on-line diseñada específicamente para tal fin, a la que se puede acceder mediante una clave. Se trata de una base de datos gestionada por la Comisión del Registro dentro de la AENP. Para registrar a un paciente es necesario disponer del consentimiento informado de los padres o de las personas responsables. Dicha base de datos cumple en su totalidad con la normativa vigente sobre confidencialidad y protección de datos.
La base de datos dispone de cuatro ventanas fundamentales. La primera de ellas incluye los datos demográficos: clave de identificación del paciente, fecha de diagnóstico, fecha de recogida de datos, fecha de nacimiento, lugar de residencia, lista desplegable de diagnósticos predefinidos sobre la nefropatía primaria (ello asegura que exista uniformidad en los diagnósticos aplicados a cada paciente), presencia de patología extrarrenal y antecedentes familiares.
La segunda ventana incluye los parámetros antropométricos y analíticos: peso, talla, superficie corporal, índice de masa corporal (IMC), perímetro cefálico (en menores de 3 años), BUN, urea, creatinina, GFR estimado según la fórmula de Schwartz, GFR estimado según la fórmula de la cistatina, aclaramiento de creatinina en orina de 24 horas, TA, hematocrito (Hto), Hb, ferritina, índice de saturación de la transferrina (IST), calcio, fósforo, PTH y 25 (OH)-Vitamina D.
La tercera ventana registra los tratamientos que está recibiendo cada paciente: estatinas, captores del fósforo, vitamina D, 1,25 (OH)-vitamina D, hierro, eritropoyetina, bicarbonato sódico, resinas de intercambio, cloruro sódico, hormona de crecimiento, ácido fólico, alopurinol, sonda nasogástrica/gastrostomía, suplementos nutricionales, fluorhidrocortisona, hipotensores y antiproteinúricos.
En la cuarta ventana se refleja el motivo y/o el destino de los pacientes que abandonan la base de datos: ERC terminal, pérdida en el seguimiento, traslado a otro centro, traslado al servicio de nefrología de adultos, fallecimiento, recuperación de función renal y nueva pérdida de función renal tras haberla recuperado.
Por último, debemos comentar que, teniendo en cuenta la corta trayectoria del Proyecto REPIR II, en este estudio sólo se refleja los datos de incidencia y prevalencia de los pacientes que se encontraban registrados a finales de 2008.
RESULTADOS
Con fecha de 31 de diciembre de 2008 habían incluido pacientes 37 centros, con un total de 605 pacientes registrados. De ellos, 74 (12%) fueron diagnosticados de ERC durante el año 2008. La edad media de todos los pacientes en el momento del diagnóstico era de 3,9 ± 5 años y en el momento de realizar la última valoración de 9,2 ± 6 años. El 59, el 13, el 22 y el 6% de los pacientes tenían una edad al diagnóstico de < 2, 3-5, 6-12 y 13-18 años, respectivamente. Sin embargo, en la última valoración para los mismos grupos de edad, el porcentaje era del 18, del 18, del 34 y del 31%, respectivamente. La diferencia entre la edad media en la última valoración y en el momento del diagnóstico es elevada (± 5 años), lo que indica que un número considerable de pacientes registrados tienen ya una evolución prolongada de varios años. El 66% de los pacientes (400 casos) pertenecían al sexo masculino y el resto al femenino (205 casos; 34%). El cociente hombre/mujer era de 1,95. El 88% de los pacientes eran de raza caucásica, el 6% de raza hispana, el 3% eran árabes, el 1% de raza negra y un 2% pertenecían a otras razas.
Durante el año 2008, sobre una población total española, en el momento del estudio, de 46.157.822 millones de habitantes y una población igual o menor de 18 años de 11.296.170 millones, la incidencia y la prevalencia de la ERC no terminal era de 8,66 y de 71,06 ppm de habitantes menores de 18 años, respectivamente.
Nefropatía primaria
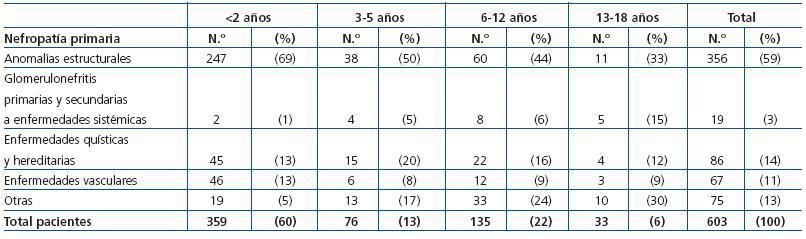
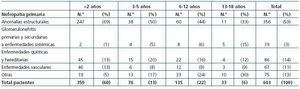
Las anomalías estructurales constituían la nefropatía primaria más frecuente (356 pacientes; 59%). Había 19 casos (3%) que tenían una glomerulopatía, 86 (14%) con una enfermedad quística o hereditaria, 67 (11%) con una enfermedad vascular y 75 (12%) con otras nefropatías. En la tabla 1 se exponen las nefropatías primarias en relación con la edad de los pacientes. Destaca que en todas las edades se mantenía el predominio de las anomalías estructurales y que el número de glomerulopatías era muy reducido. El 76% de las anomalías estructurales se producían en los hombres. Las glomerulopatías fueron más frecuentes en las mujeres (58%). El resto de las nefropatías se distribuían por igual en ambos sexos.
Función renal
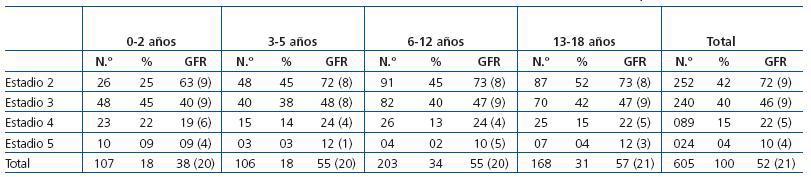
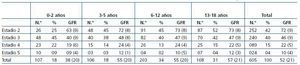
En la tabla 2 se refleja la función renal en el momento de la última valoración durante el año 2008, de forma conjunta en todos los pacientes y distribuyéndolos por cada grupo de edad y en función del estadio de la enfermedad. El valor medio del GFR de todos los pacientes era de 52 ± 2 ml/min/1,73 m2. El 82% de todos los pacientes se encontraban en estadios 2 o 3, es decir, la ERC de los pacientes registrados hasta el momento era leve-moderada.
Anemia
El valor medio del Hto, Hb, ferritina e IST cuando se valoraba a todos los pacientes conjuntamente era de 37,5%, 13 ± 2 g/dl, 91 ± 109 ng/ml y 25 ± 14%, respectivamente. Había un 30% de pacientes que presentaban anemia. A medida que progresaba la enfermedad aumentaba el porcentaje de anémicos siendo del 14, del 33, del 58 y del 54%, en los estadios 2, 3, 4 y 5, respectivamente. La presencia de anemia en los distintos grupos de edad era irregular y ocurría en el 31, el 19, el 26 y el 39% de los niños de <2, 3-5, 6-12 y 13-18 años, respectivamente.
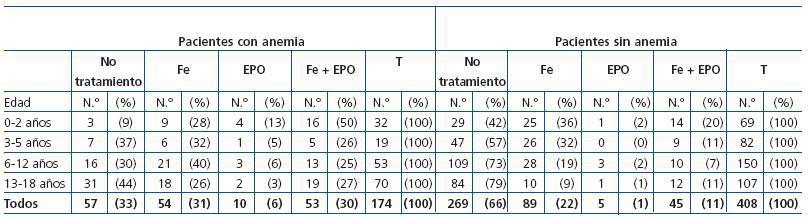
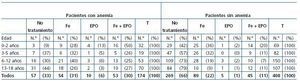
En la tabla 3 se exponen los pacientes anémicos y no anémicos en función de la edad y del tratamiento recibido. Había un 33% (57 pacientes) de anémicos que no recibían ningún tipo de tratamiento y un 67% (117 pacientes) tratados de forma insuficiente con hierro y/o eritropoyetina. En los pacientes no anémicos había un 34% de ellos (139 pacientes) que recibían algún tipo de tratamiento.
Hipertensión arterial
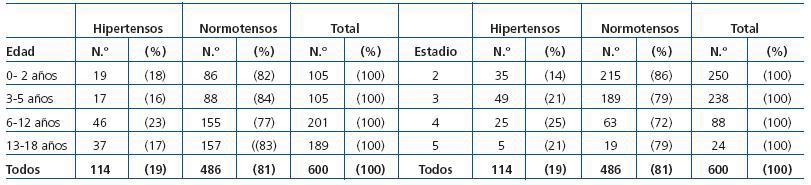
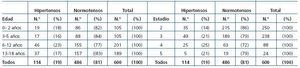
En la tabla 4 se expone la prevalencia de la HTA en los pacientes registrados en relación con los grupos de edad y con el estadio de la enfermedad. Cabe destacar que el porcentaje global de pacientes con HTA era del 19% y su presencia no guardaba relación ni con la edad ni con el estadio. El 63% de las glomerulopatías, el 31% de las enfermedades quísticas y hereditarias, el 20% de las enfermedades vasculares y el 16% del grupo de pacientes con otras enfermedades tenían HTA. El grupo etiológico con menor número de pacientes con HTA era el de las anomalías estructurales (14%).
Había un 6% de pacientes con HTA (7/114) que no recibían ningún tipo de tratamiento hipotensor. Los fármacos más utilizados en los pacientes que recibían tratamiento eran los IECA y/o los ARA II, que recibían el 71% de los pacientes tratados. El 59% recibían un solo fármaco, el 33% 2 fármacos y el 8% tres o más, con una media de 1,52 fármacos/paciente.
Metabolismo fosfocálcico
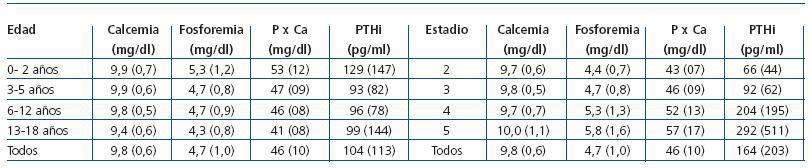
El valor medio de la calcemia, fosforemia, producto Ca x P y de la PTHi en todos los pacientes valorados de forma conjunta era de 9,8 ± 0,6 mg/dl, 4,7 ± 1,0 mg/dl, 46 ± 10 mg/dl y 104 ± 113 ng/ml, respectivamente.
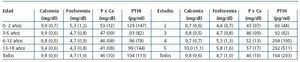
En la tabla 5 se observa que cuando la valoración se realiza en función de la edad la calcemia no sufre modificaciones significativas. La fosforemia y el producto Ca x P presentan un ligero descenso con la edad. La PTHi se mantiene sin diferencias importantes en todas las edades salvo en el grupo de 0-2 años, en el que se encuentra más elevada.
No ocurre lo mismo cuando la valoración de estos parámetros se realiza en función del estadio. En la tabla 5 se aprecia que mientras la calcemia se mantiene prácticamente normal y similar en todos los estadios, la fosforemia, el producto Ca x P y la PTHi ascienden de forma significativa a medida que aumenta la gravedad de la enfermedad. El 17% de los pacientes cumplían las recomendaciones K/DOQI sobre el metabolismo fosfocálcico, manteniendo estos cuatro parámetros dentro de los intervalos aconsejados. El 35% cumplían tres, el 34% dos, el 8% uno y el 1%, ninguna recomendación.
Crecimiento
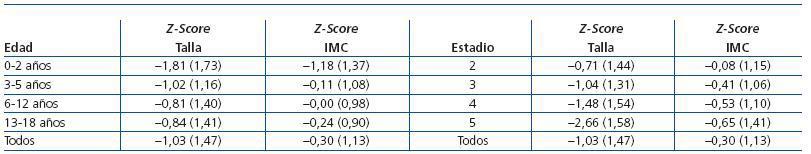
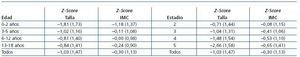
El valor medio global del Z-Score de la talla, en todos los pacientes en la última valoración era de —1,03 ± 2. El déficit de crecimiento guardaba una relación inversa con la edad de los pacientes. En la tabla 6 se aprecia que el grupo de edad con peor crecimiento era el de 0-2 años. Por otro lado, cuanto más avanzaba la enfermedad peor era le crecimiento, siendo los pacientes que se encontraban en el estadio 5 los que peor crecían.
Sin embargo, al realizar un análisis de regresión logística multivariante en el que se analizaron diversos factores (edad, sexo, raza, nefropatía primaria, estadio de la ERC, presencia de anemia, presencia de acidemia, valor de la PTHi, valor del producto Ca x P), sólo la edad predecía de forma significativa a los pacientes con talla baja. Los menores de 2 años tienen una probabilidad un 40% mayor de tener una talla baja (OR = 1,40; p <0,01).
Había 136 pacientes (25%) que tenían un Z-Score de la talla de —1,88 o peor. Dentro de este grupo, cabe destacar que el 82% de ellos no recibían tratamiento con hormona de crecimiento.
Había un 7% (42 pacientes) que estaban desnutridos, con un Z-Score del IMC de —1,88 o peor y la mayoría de ellos también se encontraban en el grupo de edad de 0-2 años. Es decir¿los niños menores de 2 años eran los que presentaban un peor crecimiento y entre quienes se encontraban el mayor número de pacientes desnutridos.
DISCUSIÓN
Éste es el primer registro que realiza un análisis prospectivo sobre la incidencia, prevalencia, etiología y comorbilidad de la ERC en la población pediátrica del estado español.
La historia natural de la enfermedad renal es variable y a veces impredecible. Sin embargo, en la edad pediátrica, generalmente se produce una progresión continua del deterioro, que lleva a menudo a la ERCT. La progresión de la enfermedad renal es mayor durante los dos períodos de rápido crecimiento que son la primera infancia y la pubertad en los que el brusco aumento de la masa corporal produce un incremento de demanda de filtración de las nefronas restantes. Los cambios hormonales durante la pubertad contribuyen al rápido deterioro del filtrado glomerular, y también pueden influir factores genéticos, familiares o étnicos. Por último, existen otros factores asociados con la progresión de la ERC que también están presente en la edad adulta: HTA, proteinuria, obesidad, dislipemia, proteinuria, anemia o alteraciones en el metabolismo fosfocálcico17.
En el año 2008, la incidencia de la ERC no terminal en nuestro medio era de 8,66 ppm de habitantes menores 18 años y la prevalencia de 71,06, cifras que se encuentran muy próximas a las referidas en el registro italiano en el año 2003 (12,1 y 74,07 ppm <18 años de incidencia y prevalencia, respectivamente)10. Sin embargo, teniendo en cuenta la corta trayectoria del REPIR II, estos datos son provisionales y probablemente, en los próximos años, sufran variaciones que podrían llegar a ser importantes.
Como en todas las series pediátricas, la patología estructural, y por tanto congénita, es la primera causa de ERC, alcanzando el 59% en nuestra serie, el 56% en el registro americano y 67,5% en el italiano. Este hecho motiva que la edad en el momento del diagnóstico sea en la mayoría de los casos antes de los 6 años (un 72% en nuestro registro) que la ERC sea más prevalente en los hombres (un 66% de nuestros pacientes). El hecho de que la diferencia entre la edad media a la última valoración durante el año 2008 y la edad en el momento del diagnóstico de la ERC sea elevada (± 5 años) indica que un número considerable de los pacientes registrados en nuestra base de datos tienen ya una evolución prolongada de varios años. Por otro lado, dadas las características de la población española, se entiende fácilmente que hayamos constatado un claro predominio de la raza caucásica en nuestra serie (88%).
El porcentaje de glomerulopatías como causa de ERC no terminal reflejado en la tabla 1 es muy reducido (3%) y contrasta con el que ocurre en la ERCT que puede llegar al 20%. Ello se debe a que la evolución de la enfermedad glomerular es mucho más rápida que la de las displasias renales, muchas de las cuales alcanzan la ERCT en la edad adulta18.
El valor medio del GFR de nuestros pacientes es de 52 ± 2 ml/min/1,73 m2, con un 82% de ellos en estadios 2 y 3, mientras que en el NAPRTCS y en el ITALKID es de 39 y de 42 ml/min/1,73 m2, respectivamente. Es decir, los pacientes de nuestro registro presentan una ERC más leve que la de los otros dos registros (tabla 2). Ello puede estar en relación, al menos en parte, con que los pacientes pediátricos con ERC en nuestro medio son remitidos más precozmente (desde el estadio 1) desde atención primaria a los servicios de nefrología pediátrica.
La información de la que se dispone en la bibliografía médica acerca de la comorbilidad asociada con la ERC es muy reducida y sólo el NAPRTCS ofrece anualmente datos sobre ella. En este estudio hemos analizado la prevalencia de la anemia y de la HTA, así como el nivel de control de las alteraciones del metabolismo calcio-fósforo y del crecimiento que se producen en estos pacientes9,16,19.
La anemia es una complicación común en la ERC avanzada y se asocia con un aumento de la morbilidad y del riesgo de mortalidad18,20,21. La prevalencia de la anemia en nuestros pacientes es del 30%. Este porcentaje se incrementa con la gravedad de la ERC, de tal manera que en los estadios 4 y 5 prediálisis, es del 58 y del 54%, respectivamente. Hemos constatado que nuestros pacientes anémicos están siendo tratados de forma incorrecta, ya que el 33% de ellos no reciben ningún tipo de tratamiento y el resto lo reciben de forma insuficiente (tabla 3).
La HTA es un conocido factor de riesgo cardiovascular y de progresión de la ERC en adultos, y aunque no existen datos prospectivos en pediatría22,23, es lógico pensar que también lo es en los niños. En nuestra serie sólo el 19% de nuestros pacientes presentan HTA, porcentaje muy inferior al del registro americano, en el que se refiere una prevalencia de HTA del 48%9. Aunque este dato tiene que ser confirmado en los próximos años, uno de los factores que podrían explicarlo sería que, en nuestros pacientes, la etiología más frecuente es la enfermedad estructural, que no suele cursar con HTA y que la mayoría de los niños tenían una enfermedad renal leve-moderada. Por otro lado, en este momento no podemos descartar que estemos infradiagnosticando los casos de HTA, ya que existen indicios de que no ha habido unanimidad entre los distintos centros participantes a la hora de definirla (tabla 4). Únicamente hemos encontrado relación entre la prevalencia de la HTA y la etiología de la ERC, de tal manera que el 63% de los niños con una glomerulopatía tenían HTA. No se ha podido demostrar relación alguna ni con la edad ni con el estadio de la ERC. El 94% de los pacientes con hipertensión recibían tratamiento hipotensor y de ellos el 71% recibían tratamiento con IECA y/o ARA II.
Las anomalías del metabolismo mineral óseo son un hallazgo universal a medida que progresa la ERC. En los pacientes pediátricos tiene además un efecto deletéreo en el crecimiento24,25. Aunque en nuestros pacientes los valores medios de la calcemia, fosforemia, producto Ca x P y PTHi, valorados de forma conjunta, estaban dentro de los límites de las recomendaciones de las Guías K/DOQI26-28, cuando analizamos los mismos parámetros teniendo en cuenta la edad y el estadio, sólo el 17% cumplían las cuatro recomendaciones, mientras que la mayoría cumplían sólo tres (35%) o dos (34%) recomendaciones. Hemos constatado, igual que otros autores, que las recomendaciones de las Guías K/DOQI en el control de las alteraciones del metabolismo Ca-P son difíciles de cumplir (tabla 5).
El retraso en el crecimiento es un problema común en los niños con ERC y se asocia con una morbimortalidad significativa18. La talla final alcanzada en los pacientes con inicio de la ERC en la edad pediátrica es uno de los factores más importantes para su rehabilitación18,29-31. El valor medio global del Z-Score de la talla en la última valoración de nuestros pacientes era de —1,03 ± 2. Había 136 pacientes (25%) que tenían un Z-Score de la talla <1,88, dato que contrasta con los del registro americano, en el que el número de pacientes con un crecimiento deficitario era mayor (36%). Por otro lado, hemos constatado que el déficit de crecimiento guardaba una relación inversa con la edad y una relación directa con la gravedad de la ERC, presentando un peor crecimiento los pacientes de menor edad (grupo de 0-2 años) y los que se encontraban en estadio 5 prediálisis (tabla 6). Sin embargo, al realizar un análisis de regresión logística multivariante solamente la edad predecía de forma significativa a los pacientes con talla baja. Los menores de 2 años tienen una probabilidad un 40% mayor de tener una talla baja (OR = 1,40; p <0,01).
El porcentaje de malnutrición (Z-Score de IMC ≤1,88) en nuestra serie era del 7%, la mayoría en el grupo de edad de 0-2 años. Es decir, los niños <2 años son los que presentaban un peor crecimiento y entre quienes se encontraba el mayor número de pacientes desnutridos.
En conclusión, en este trabajo presentamos los primeros datos del Registro Español de ERC no terminal en la edad pediátrica, REPIR II referentes al año 2008, siendo el primer estudio que realiza un análisis prospectivo sobre la incidencia, prevalencia, etiología y comorbilidad de la ERC en la población pediátrica del estado español. Teniendo en cuenta la corta trayectoria de este registro los datos presentados son provisionales, pudiendo sufrir cambios importantes en los próximos años.
AGRADECIMIENTOS
Esta base de datos está financiada por Pfizer. Queremos agradecer a Francisco Poyato Camacho, Medical Advisor en dicho laboratorio, su apoyo incondicional a este proyecto, sin el cual no hubiera sido posible llevarlo a cabo. Queremos extender nuestro agradecimiento a todos los pediatras y nefrólogos pediátricos que, con la aportación de los datos de sus pacientes, han hecho posible que comencemos a conocer de forma más objetiva las características de la ERC infantil en nuestro país.
Tabla 1. Nefropatía primaria en el momento del diagnóstico
Tabla 2. Estadio de la ERC en el momento de la última valoración en relación con la edad de los pacientes
Tabla 3. Presencia de anemia en el momento de la última valoración, en relación con la edad y el tratamiento recibido
Tabla 4. Frecuencia de la HTA en el momento de la última valoración, en relación con la edad y la gravedad de la ERC
Tabla 5. Metabolismo fosfocálcico: valores medios y desviación estándar de los distintos parámetros en el momento de la última valoración, en relación con la edad y la gravedad de la ERC
Tabla 6. Crecimiento de los pacientes en el momento de la última valoración, en relación con la edad y la gravedad