La elección de la modalidad de diálisis más apropiada para los pacientes que pierden un injerto renal es una pregunta no resuelta. La mayoría de pacientes reinicia tratamiento sustitutivo con hemodiálisis (HD). Hay varias razones para ello:
1. En la mayor parte de los programas, predomina la HD sobre la diálisis peritoneal (DP).
2. La urgencia para el inicio del tratamiento obliga a la HD.
3. El temor a las complicaciones infecciosas por la necesidad de mantener cierto grado de inmunosupresión para evitar fenómenos inmunes y preservar la función residual en el caso de la DP.
Muchos pacientes que pierden su injerto se podrían beneficiar de la diálisis peritoneal, manteniendo un estilo de vida más parecido al que tenían en trasplante, preservando el árbol vascular en casos de niños y jóvenes, y como alternativa si no hay acceso vascular.
La mortalidad en los pacientes que regresan a diálisis tras el fallo crónico del injerto respecto a la de pacientes que inician diálisis como primer tratamiento sustitutivo parece ser mayor. Sin embargo, no hay diferencias de mortalidad entre los pacientes que inician HD o DP.
Los estudios que comparan la tasa de peritonitis en DP tras la pérdida de un injerto y sin injerto renal previo no obtienen resultados homogéneos. La supervivencia de la técnica DP tras perder un injerto es similar a la de la DP inicial.
Al comparar la supervivencia de la técnica entre la HD y la DP en estos pacientes, estudios retrospectivos y sesgados encontrados sugieren que ambas técnicas presentan un pronóstico superponible.
Con todo ello, debemos concluir que la elección de la modalidad de diálisis tras la pérdida de un injerto debe seguir riterios similares a los que se aplican en pacientes que inician diálisis como primer tratamiento sustitutivo.
The choice of the most of dialysis modality after renal graft loss is an unanswered question. Most patients start hemodialysis (HD) in this situation, because of several reasons:
1. In most dialysis programs HD predominates clearly over Peritoneal Dialysis (PD).
2. The star of dialysis in emergency situations makes the physician use HD
3. The fear of infections in case of maintenance of immunosupression to avoid immune response and to keep residual renal function in case of PD.
A lot of patients could undergo PD in order to maintain the previous style of life, as an alternative in case of absence of vascular access and to avoid vascular accesses in children.
Mortality seems to be greater in patients with graft loss than in those who start dialysis for the first time, although the comparison between both groups is methodologically difficult. However, there is no difference in mortality between patients who start HD and those who start PD.
Studies comparing the rate of peritonitis in PD patients in both groups find controversial results. The analysis of the few, retrospective and biased studies which look for differences in patient survival in HD and DP suggests that prognosis of both groups is similar.
The choice of dialysis modality must be similar to those patients which begin dialysis for the first time.
INTRODUCCIÓN
La característica común a todos los aspectos relevantes para la decisión de la modalidad de diálisis aconsejable tras la pérdida de un injerto renal es la práctica ausencia de evidencia suficiente para tomar decisiones en uno u otro sentido. Así, no existe en ninguno de ellos evidencia de nivel superior al C al basarse en estudios de cohortes o de casos y controles; y si tenemos en cuenta que el escaso número de pacientes incluidos en estos estudios proporciona a éstos poca potencia estadística, en la práctica debemos tener en cuenta que en este capítulo se darán recomendaciones de nivel de evidencia D, es decir, basadas en la experiencia más que en la evidencia.
El grupo de pacientes que regresa a diálisis tras la pérdida del injerto renal tiene un riesgo mayor de mortalidad y hay que abordarlo como un grupo especial. No hay evidencia de que la técnica de diálisis tenga un impacto especial en este riesgo, y tanto la HD como la DP son opciones válidas como tratamiento renal sustitutivo en este grupo.
El manejo adecuado de la inmunosupresión y las mejores técnicas de diálisis (tanto DP como HD) hacen posible que no desechemos a priori una u otra.
El abordaje de la enfermedad crónica avanzada debe ser multidisciplinar, incluyendo aspectos educativos e información de las modalidades de la terapia renal sustitutiva, de forma complementaria y no competitiva. En la literatura del trasplante renal, pocos estudios evalúan el impacto bidireccional entre modalidad de diálisis y supervivencia del paciente. La mayor experiencia de los grupos en ambas técnicas, el abundante número de pacientes que precisan un segundo o más injertos a lo largo de su vida y la necesidad de individualizar los tratamientos nos ayudarán en el futuro a definir la mejor terapia para cada individuo.
COMPARACIÓN ENTRE LA HEMODIÁLISIS Y LA DIÁLISIS PERITONEAL EN LA MORBIMORTALIDAD DE LOS PACIENTES QUE REGRESAN A DIÁLISIS TRAS LA PÉRDIDA DEL INJERTO
Se describe una alta mortalidad en los pacientes que regresan a diálisis tras el fallo crónico del injerto renal. Analizando datos del USRDS, Ojo A et al.1 comunicaron una alta mortalidad en este grupo a los cinco años (35% para no diabéticos y 50% para diabéticos), resultados similares a los mostrados por Meir-Kriesche HU et al.2
Destacamos dos estudios recientes3,4 que sugieren que la mortalidad de este grupo es mayor que la de pacientes que inician diálisis por primera vez, incluso al comparar grupos de igual situación en lista de espera para trasplante.
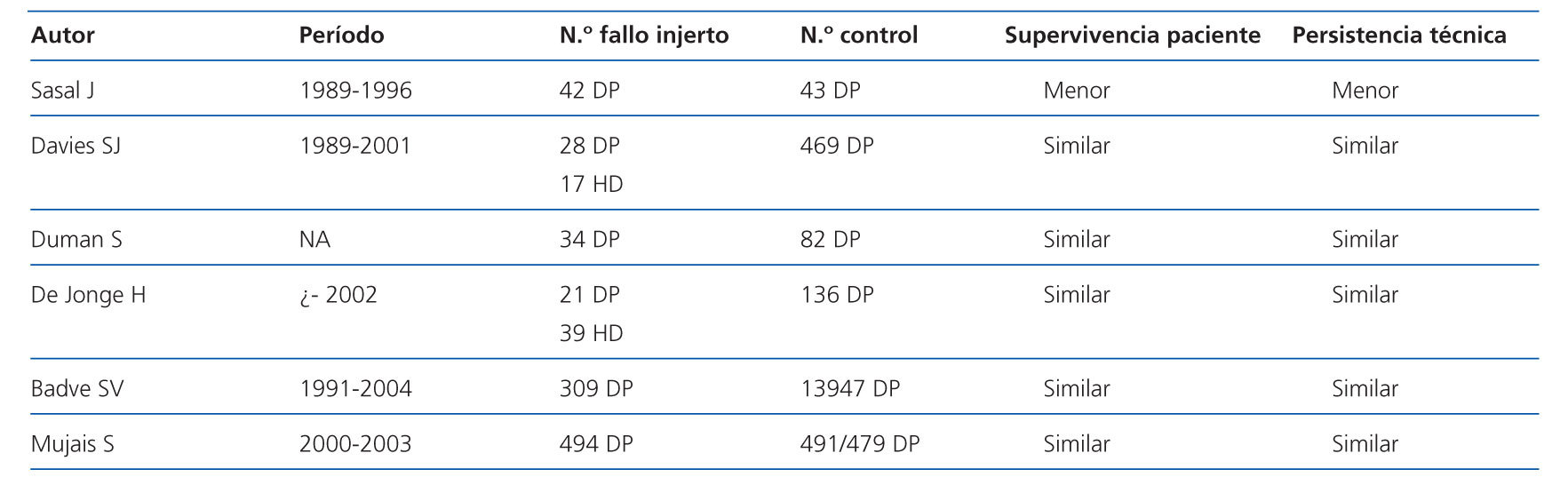
No hay diferencias en la supervivencia de los pacientes que inician DP o HD tras perder el injerto. Los escasos estudios que comparan ambos grupos encuentran similar supervivencia (tabla 1)7,10,12. Davies SJ estudia 45 pacientes con fallo del injerto que inician diálisis, 28 en DP y 17 en HD, no encontrando diferente supervivencia entre la DP y la HD7. De Jonge H compara 21 pacientes que inician DP postrasplante y 39 pacientes que iniciaron HD, sin encontrar diferencias significativas en la mortalidad10. Badve SV publicó los resultados del estudio del registro australiano. De 11.979 pacientes que iniciaron DP (1991-2004), 309 pacientes lo hicieron tras fallo del injerto. El análisis multivariante no mostró que la técnica de diálisis fuera una variable independiente de mortalidad12. El pronóstico respecto a supervivencia de pacientes que comienzan DP tras fallo del injerto es al menos superponible a la de los que inician HD. Ahora bien, todos estos estudios son retrospectivos y presentan varios sesgos, principalmente de selección, y carecen de información clínica importante (como la concerniente a la inmunosupresión o el riesgo vascular).
Respecto a la técnica de diálisis, en los escasos estudios que comparan los pacientes que vuelven a DP desde el trasplante a los que inician DP de novo, no hay diferencias de mortalidad, fundamentalmente porque la población que vuelve a DP desde el trasplante fallido es una población más seleccionada en estos estudios. Únicamente Sasal J et al. encuentran una mayor mortalidad en los pacientes con injerto renal, en una cohorte de 42 pacientes comparada con una cohorte seleccionada aleatoriamente de 43 pacientes que inician DP de novo5.
En un análisis retrospectivo realizado en los hospitales del País Vasco y La Rioja, estudiamos 154 pacientes que regresaron a diálisis tras la pérdida del injerto. El 73,7% en HD y el 18,5% en DP. El resto se trasplantó (4,2%) o falleció (3,6%). La supervivencia en este segundo período de diálisis fue mayor en DP (p <0,003), probablemente asociado a una menor edad media de estos pacientes respecto a los que iniciaban HD (42 vs. 54 años) (p <0,001).
Hay que tener en cuenta que en nuestro programa el reparto de tratamiento renal sustitutivo tras la pérdida de función renal de riñones nativos es del 73% para HD y del 27% para DP en este grupo estudiado. El grado de concordancia entre modalidad de diálisis previa y secundaria fue del 90% para HD y del 49% para DP.
En nuestra experiencia, la adecuada selección de los pacientes, teniendo en cuenta la edad, el estímulo para mantener una vida autónoma, la ausencia de patología grave concomitante y la ausencia de fenómenos inflamatorios desde el injerto que favorezcan la minimización de la inmunosupresión, nos animan a indicar la DP sin menoscabo de inicio o traslado a HD si las circunstancias lo aconsejan.
Como argumento adicional, los pacientes que inician DP lo hacen con más precocidad por la propia necesidad de la técnica (colocación del catéter, entrenamiento e inicio del tratamiento propiamente dicho). Esto lleva a un mayor cuidado de todos los factores no relacionados con la inmunosupresión y a un mejor estado clínico prediálisis.
DIFERENCIAS EN LA SUPERVIVENCIA DE TÉCNICA ENTRE HEMODIÁLISIS Y DIÁLISIS PERITONEAL
No existen diferencias significativas en la duración de la técnica entre la HD y la DP en los pacientes que regresan tras el trasplante (tabla 1).
Davies SJ et al. estudian 45 pacientes con fallo del injerto que inician diálisis, 28 en DP y 17 en HD, no encontrando diferente supervivencia entre ambas técnicas7.
De Jonge H et al. comparan 21 pacientes que inician DP postrasplante y 39 pacientes que inician HD. La duración de la técnica tiende a ser mayor en HD, y el retrasplante más frecuente en DP.10
Badve SV et al. publicaron los resultados del estudio del registro australiano. De 11.979 pacientes que inician DP (1991-2004), 309 pacientes lo hicieron tras fallo del injerto. El análisis multivariante no mostró que la técnica de diálisis fuera una variable independiente de mortalidad12.
En los 154 pacientes estudiados de nuestra serie (junio de 2003-octubre de 2007), el fallo de la técnica es superponide retrasplante fue mayor en pacientes en DP. Aunque estamos pendientes de analizar la velocidad de pérdida de función residual en pacientes en DP, la aparición y el desarrollo de técnicas de diálisis automática nocturna en parte ha paliado este problema; si bien sigue siendo más frecuente el paso de DP a HD. Como curiosidad, tenemos un caso de regreso a DP automática tras embolización del injerto por problemas inflamatorios.
En resumen, pensamos que la evidencia no concluye a favor de una de las técnicas.
PERITONITIS EN DIÁLISIS PERITONEAL CON INJERTO FALLIDO
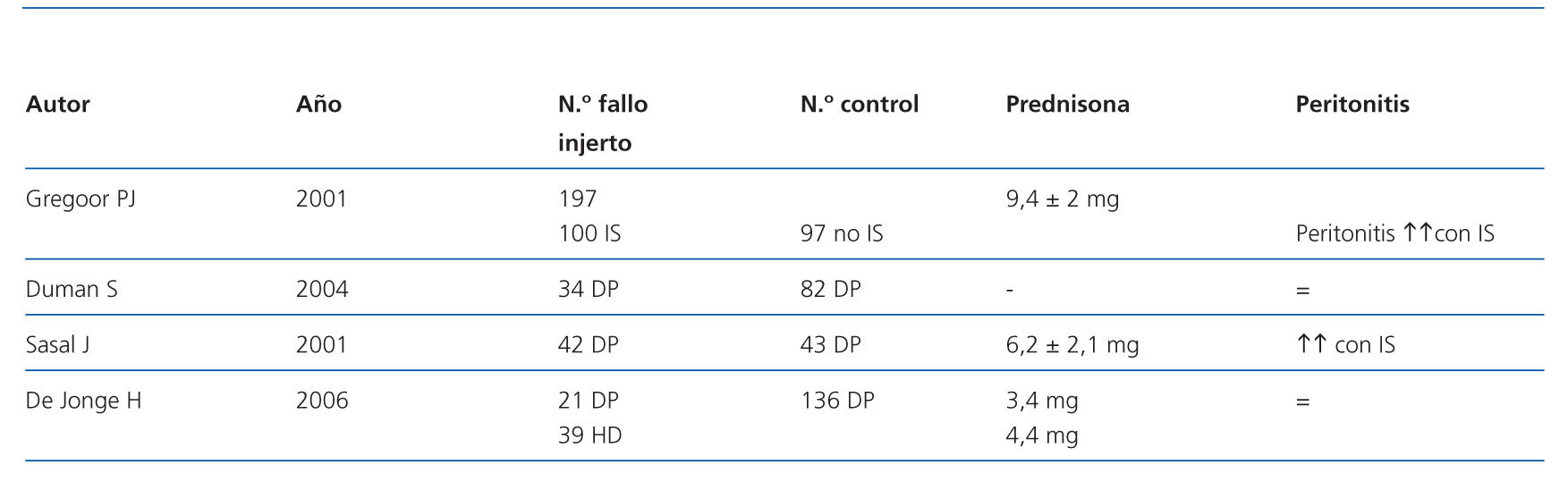
La peritonitis puede condicionar un aumento de mortalidad del paciente y de fallo de la técnica (tabla 2). Hay pocos estudios enfocados a este aspecto tan importante:
- Gregoor PJ et al. evalúan la morbilidad y mortalidad en 177 pacientes que recibieron 197 injertos con fallo crónico posterior. Comparando los grupos con y sin inmunosupresión (100/97), encontraron más mortalidad por infecciones graves y mortalidad cardiovascular en cualquier modalidad de diálisis. La dosis de prednisona era de 9,4 mg/día de media. No se diferencia HD o DP11.
- Sasal J et al. encuentran mayor mortalidad y mayor número de peritonitis (todas por gramnegativos) en los pacientes en DP por fallo del injerto. De éstos, 39/42 tomaban prednisona5.
- De Jonge H et al. no observaron un mayor número de peritonitis en los pacientes DP y fallo del injerto. El 86% de los pacientes tomaban dosis bajas de prednisona (3,4 mg/día), que se retiraba en 9-12 meses10.
- Duman S et al. no encuentran diferencias en la tasa de peritonitis en los dos grupos en DP con o sin fallo del injerto. Sólo 4 de 34 pacientes con injerto llevaban prednisona8.
La inmunosupresión en dosis elevadas puede condicionar un aumento de las complicaciones infecciosas. Parece que la inmunosupresión en dosis bajas podría ser bien tolerada, con tasa escasa de infecciones, evitando fenómenos inmunes y permitiendo el mantenimiento de la función renal residual tan importante en DP.
En nuestra experiencia, no hemos tenido un mayor número de peritonitis en DP de novo o tras pérdida de injerto. Asimismo, el germen causal ha sido principalmente el estafilococo y no ha habido ni infección ni fallecimiento por censo de inmunosupresión ha sido rápida para anticalcineurínicos (<1 mes). Indicamos una dosis de prednisona (si la tenían previamente) de 2,5 mg en 2-3 meses y suspensión en 6-8 meses. Mantuvimos dosis pequeñas de MMF (250-500 mg/día) durante el descenso de los corticoides y suspensión en el mismo tiempo. Puntualizamos que si individualmente algún paciente presentó problemas inflamatorios y precisó dosis elevadas de inmunosupresión, seguimos las indicaciones de embolización o nefrectomía del injerto. Como curiosidad, indicar que tenemos a un paciente en DP automática e hiperinmunizado que nunca tuvo fenómenos inflamatorios ni peritonitis.
ASPECTOS A CONSIDERAR AL SELECCIONAR LA MODALIDAD DE TRATAMIENTO SUSTITUTIVO TRAS LA PÉRDIDA DE UN INJERTO
La falta de evidencia impide establecer conclusiones o recomendaciones firmes en relación con la elección de la técnica, pero la experiencia y los pocos estudios disponibles permiten considerar ambas técnicas de diálisis como válidas tras el fallo del injerto. No obstante, hay ciertos aspectos de las circunstancias clínicas de estos pacientes que deberemos tener en consideración y que enumeramos a continuación:
1. Indicaciones generales de la modalidad. El planteamiento a priori, al igual que en los pacientes que inician diálisis por primera vez, debe tener en cuenta las actuales indicaciones de cada modalidad13, que en el caso de la HD serían la voluntad del paciente, la presencia de daño abdominal importante y la incapacidad de autotratamiento; y en el caso de la DP, la imposibilidad de acceso vascular interno y la presencia de cardiopatía grave. La inmensa mayoría del resto de indicaciones o contraindicaciones son relativas. En caso de duda, la elección lógica debería ser la DP, dada la mayor dependencia y aprovechamiento de ésta de la función renal residual. Por otro lado, el paciente potencial candidato a un nuevo trasplante debe ser informado de sus circunstancias y posibilidades, tanto en el caso del trasplante de donante cadáver como de donante vivo, si es posible y procede. También en este aspecto se deben individualizar las indicaciones.
2. Mantenimiento del injerto. La anulación de su función, tratada en otro capítulo de estas guías, sea mediante embolización o mediante nefrectomía, dificultará la DP por la dependencia de ésta en la función renal residual para conseguir una diálisis adecuada. Sin embargo, las técnicas actuales para conseguir una ultrafiltración y diálisis adecuada a priori no contraindicarían la DP.
3. Mantenimiento de la inmunosupresión. Este tema también se trata en otro capítulo de estas guías. En lo diremos que el ritmo de reducción de la inmunosupresión debería ser más lento en pacientes en DP para facilitar el mantenimiento de la función renal residual, y más rápido en los pacientes en HD a través de acceso vascular percutáneo, en los que el riesgo de infección es mayor, sin obtener apenas beneficio del mantenimiento de función renal residual. En cualquier caso, la aparición de fenómenos sugestivos de reacción inmunológica en relación con el injerto puede llevar al aumento temporal de la dosis de inmunosupresores, lo cual va en contra de modalidades que utilicen un catéter como acceso de diálisis.
4. Seguimiento integrado del paciente. Cuando las maniobras terapéuticas para detener la progresión de la nefropatía crónica del injerto están agotadas y la función del mismo está muy deteriorada, es importante la coordinación entre las consultas de trasplante y las de prediálisis para conseguir los resultados adecuados, tanto en lo que se refiere a la elección de la modalidad de tratamiento y la información que debe recibir el paciente como al adecuado manejo de la inmunosupresión y la medicación característica de esta fase de la insuficiencia renal.
Tabla 1. Estudios que comparan supervivencia del paciente y de la técnica. Los controles son pacientes con inicio de tratamiento renal sustitutivo de novo
Tabla 2. Estudios que analizan el porcentaje de peritonitis en pacientes con pérdida de injerto y diálisis peritoneal. Los controles son pacientes con inicio de tratamiento renal sustitutivo de novo