En México y en el resto del mundo existe incremento de frecuencia de enfermedad renal crónica (ERC) que progresa a insuficiencia renal crónica terminal (IRCT) y que requiere terapias de reemplazo renal como diálisis peritoneal (DP)1,2. En IRCT la morbimortalidad es debida principalmente a enfermedad cardiovascular (ECV)3,4. La cardiomiopatía urémica (CMU) resulta de alteraciones en la estructura y función cardiaca en pacientes con ERC3–5. La CMU predice mortalidad por presencia de alteraciones detectadas desde el inicio de DP4,5 y se caracteriza por hipertrofia ventricular izquierda (HVI), dilatación ventricular izquierda y disfunción cardiaca tanto sistólica como diastólica5. La ecocardiografía detecta hallazgos relacionados con la CMU3,4,6 que impactan en el pronóstico de pacientes con IRCT que inician DP6. La prueba de equilibrio peritoneal (PEP)7 valora la función peritoneal, permite clasificar a pacientes como diferentes tipos de transportadores y tiene valor pronóstico en pacientes en DP8,9. El objetivo del estudio fue describir hallazgos ecocardiográficos relacionados con la CMU al iniciar DPCA, además de correlacionar dichos hallazgos con el tipo de transporte peritoneal (TP).
Estudio transversal realizado de enero de 2013 a agosto de 2014. Incluimos a pacientes con IRCT de cualquier etiología, entre 16 y 75 años, con DPCA durante un mínimo de un mes, con ecocardiograma transtorácico y PEP. Excluimos a portadores de cardiopatía previamente diagnosticada, a aquellos con descompensación aguda de cualquier enfermedad cardiaca, con catéter peritoneal disfuncional, con peritonitis en las 6semanas previas a realizar PEP, con falla de ultrafiltración o lesión renal aguda. Se realizó ecocardiograma transtorácico para determinar la fracción de eyección (FEVI) y la fracción de acortamiento del ventrículo izquierdo (FacVI). Definimos disfunción sistólica (DS) a valores de FEVI <52% en hombres y de <54% en mujeres, con o sin FacVI <25%. Determinamos la masa del ventrículo izquierdo (MVI) para definir hipertrofia ventricular izquierda (HVI) con MVI de >224 g en hombres y >162 g en mujeres. Para determinar el patrón de HVI, se calculó el espesor relativo con valores de <0,42 para HVI excéntrica y >0,42 para HVI concéntrica. Clasificamos como disfunción diastólica (DD) de acuerdo con el patrón de llenado del ventrículo izquierdo. Las dimensiones y funcionalidad cardiacas se calcularon de acuerdo con las recomendaciones de la Sociedad Americana de Ecocardiografía10. Se realizó estadística descriptiva, la prueba de Kruskall-Wallis para evaluar diferencias entre hallazgos bioquímicos y ecocardiográficos en relación con los meses de uso de DP, asi como correlación de Pearson para determinar la relación entre hallazgos ecocardiográficos y TP.
Se evaluó a 50 pacientes, 30 (60%) hombres, con mediana de edad de 24 años (16-70) y tiempo en DPCA de 2 meses (1-6); con etiología idiopática de ERC en el 68%, con TP principalmente de promedio alto en el 38% de la serie. Bioquímicamente, destacaron anemia e hipoalbuminemia moderadas, así como glucosa alterada en ayuno. Hubo HVI en el 72%, patrón geométrico de HVI de tipo concéntrico en el 53%, derrame pericárdico en el 32% e hipertensión arterial pulmonar en el 60%. Existió DD en el 100% de los pacientes, principalmente con patrón de tipo i o de relajación prolongada en el 54% de la población. El 50% presentaron DS, manifestada principalmente con disminución de FEVI. Existieron calcificaciones valvulares (CV) en el 30%; en el 18% en válvula aórtica y en el 12% en mitral (tabla 1). En la tabla 2 se observa que no existió diferencia (p=ns) entre los diferentes hallazgos relacionados con CMU en relación con el tiempo en DP, ni tampoco hubo diferencias en las comparaciones intra- ni intergrupos entre el TP y las variables analizadas (p=ns). De igual manera, tampoco existió correlación entre el TP y variables bioquímicas ni tampoco hallazgos ecocardiográficos relacionados con CMU (p=ns).
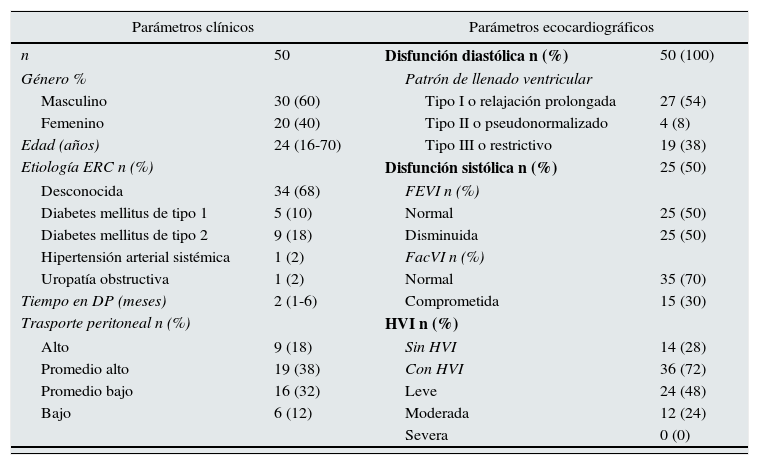
Características demográficas clínicas, bioquímicas y ecocardiográficas
| Parámetros clínicos | Parámetros ecocardiográficos | ||
|---|---|---|---|
| n | 50 | Disfunción diastólica n (%) | 50 (100) |
| Género % | Patrón de llenado ventricular | ||
| Masculino | 30 (60) | Tipo I o relajación prolongada | 27 (54) |
| Femenino | 20 (40) | Tipo II o pseudonormalizado | 4 (8) |
| Edad (años) | 24 (16-70) | Tipo III o restrictivo | 19 (38) |
| Etiología ERC n (%) | Disfunción sistólica n (%) | 25 (50) | |
| Desconocida | 34 (68) | FEVI n (%) | |
| Diabetes mellitus de tipo 1 | 5 (10) | Normal | 25 (50) |
| Diabetes mellitus de tipo 2 | 9 (18) | Disminuida | 25 (50) |
| Hipertensión arterial sistémica | 1 (2) | FacVI n (%) | |
| Uropatía obstructiva | 1 (2) | Normal | 35 (70) |
| Tiempo en DP (meses) | 2 (1-6) | Comprometida | 15 (30) |
| Trasporte peritoneal n (%) | HVI n (%) | ||
| Alto | 9 (18) | Sin HVI | 14 (28) |
| Promedio alto | 19 (38) | Con HVI | 36 (72) |
| Promedio bajo | 16 (32) | Leve | 24 (48) |
| Bajo | 6 (12) | Moderada | 12 (24) |
| Severa | 0 (0) | ||
| Parámetros bioquímicos | |||
|---|---|---|---|
| Hemoglobina (g/l) | 8,76±1,4 | ||
| Patrones geométricos HVI n (%) | |||
| Creatinina (mg/dl) | 10,2±3,9 | ||
| Urea (mg/dl) | 90,9±18,8 | ||
| Glucosa (mg/dl) | 108±28,7 | HVI excéntrica | 17 (47) |
| Potasio (mmol/l) | 4,8±0,67 | HVI concéntrica | 19 (53) |
| Sodio (mmol/l) | 133,1±2,61 | ||
| Albúmina (g/l) | 2,9±0,64 | ||
| Fósforo (mg/dl) | 4,81±1,6 | ||
Se muestran las variables evaluadas de los pacientes incluidos, se describen los parámetros bioquímicos y la distribución de las frecuencias del tipo de TP de la población estudiada, además, se muestran los parámetros ecocardiográficos de la serie. Resultados expresados en media±desviacion estandar y/o mediana y rango según se requiera (variables cuantitativas) o números y porcentajes (variables cualitativas).
DP: diálisis peritoneal; ERC: enfermedad renal crónica; FacVI: fracción de acortamiento ventricular izquierdo; FEVI: fracción de eyección ventricular izquierda; HVI: hipertrofia ventricular izquierda; n: número de pacientes.
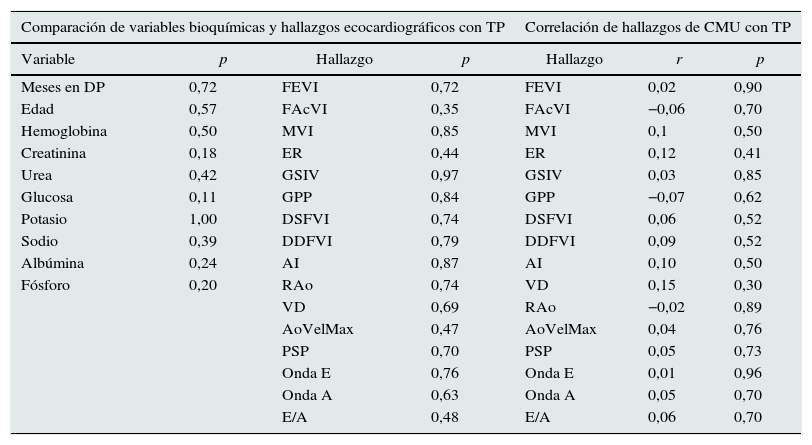
Análisis comparativo y de correlación de variables bioquímicas, hallazgos ecocardiográficos de CMU con TP
| Comparación de variables bioquímicas y hallazgos ecocardiográficos con TP | Correlación de hallazgos de CMU con TP | |||||
|---|---|---|---|---|---|---|
| Variable | p | Hallazgo | p | Hallazgo | r | p |
| Meses en DP | 0,72 | FEVI | 0,72 | FEVI | 0,02 | 0,90 |
| Edad | 0,57 | FAcVI | 0,35 | FAcVI | −0,06 | 0,70 |
| Hemoglobina | 0,50 | MVI | 0,85 | MVI | 0,1 | 0,50 |
| Creatinina | 0,18 | ER | 0,44 | ER | 0,12 | 0,41 |
| Urea | 0,42 | GSIV | 0,97 | GSIV | 0,03 | 0,85 |
| Glucosa | 0,11 | GPP | 0,84 | GPP | −0,07 | 0,62 |
| Potasio | 1,00 | DSFVI | 0,74 | DSFVI | 0,06 | 0,52 |
| Sodio | 0,39 | DDFVI | 0,79 | DDFVI | 0,09 | 0,52 |
| Albúmina | 0,24 | AI | 0,87 | AI | 0,10 | 0,50 |
| Fósforo | 0,20 | RAo | 0,74 | VD | 0,15 | 0,30 |
| VD | 0,69 | RAo | −0,02 | 0,89 | ||
| AoVelMax | 0,47 | AoVelMax | 0,04 | 0,76 | ||
| PSP | 0,70 | PSP | 0,05 | 0,73 | ||
| Onda E | 0,76 | Onda E | 0,01 | 0,96 | ||
| Onda A | 0,63 | Onda A | 0,05 | 0,70 | ||
| E/A | 0,48 | E/A | 0,06 | 0,70 | ||
Se muestra comparación (prueba Kruskall-Wallis) sin observar ningún dato de significación entre TP y datos bioquímicos y hallazgos relacionados con CMU al iniciar diálisis. Se muestran los valores de correlación (r de Pearson), donde no se observó ningún dato de significación entre TP y los hallazgos relacionados con CMU al iniciar la diálisis.
AI: aurícula izquierda; AoVelMax: velocidad máxima de aorta; DDFVI: diámetro diastólico final de ventrículo izquierdo; DSFVI: diámetro sistólico final de ventrículo izquierdo; E/A: relación onda E/onda A; ER: espesor relativo; FacVI: fracción de acortamiento de ventrículo izquierdo; FEVI: fracción de eyección de ventrículo izquierdo; GPP: grosor de pared posterior; GSIV: grosor de septum interventricular; MVI: masa de ventrículo izquierdo; PSP: presión sistólica pulmonar; RAo: raíz aórtica; VD: ventrículo derecho.
Describimos importantes hallazgos para CMU presentes en una población joven y sin seguridad social, con evidente diagnóstico de ERC, de etiología desconocida, desde su ingreso al programa de DP. Detectamos, además, hipoalbuminemia y anemia, importantes factores conocidos para ECV4. Es importante resaltar que dichas alteraciones bioquímicas y ecocardiográficas no fueron diferentes en relación con los meses de uso de DP en los pacientes evaluados. Existió disfunción ventricular izquierda con DD en toda la muestra, principalmente de tipo relajación prolongada. La mitad presentó DS con frecuente HVI, principal manifestación descrita en la CMU5. De manera adicional, aunque no descrito en la CMU, hubo CV en un tercio de la serie, principalmente en aorta. A pesar de que en esta serie predominó el TP de tipo promedio alto, no existió correlación alguna al iniciar DP ni con variables bioquímicas ni tampoco con hallazgos ecocardiográficos relacionados con CMU.
En conclusión, desde el ingreso de pacientes con IRCT a DP, se observa presencia de CMU con predominio de DD, frecuente HVI principalmente de tipo concéntrico y función sistólica afectada. Dichas alteraciones no difieren con relación al tiempo de uso de DP. Existen factores importantes descritos como de riesgo para ECV como anemia, hipoalbuminemia y CV. Todas estas alteraciones repercuten en el pronóstico de pacientes con IRCT que inician DP. Sin embargo, se requieren estudios longitudinales para conocer la evolución de hallazgos relacionados con CMU en pacientes con DP.
FinanciamientoEl estudio fue financiado por el Hospital Civil de Guadalajara Dr. Juan I. Menchaca.
Conflicto de interesesNo existen conflictos de interés.