Después de una contextualización en los marcos genéricos de la nanotecnología y la nanomedicina, se exponen las 2connotaciones nanotecnológicas de la Nefrología. La potencial faceta negativa de la nanonefrología es el aclaramiento renal de las nanopartículas usadas con fines nanomédicos o ingeridas en los nanoalimentos, cada vez más abundantes. El impacto positivo de la nanotecnología en la Nefrología se centra en el desarrollo de nanodiagnósticos renales para estudios básicos de la función renal, diagnóstico precoz del fallo renal agudo, seguimiento fiable y simple de la enfermedad renal crónica o la mejora de las imágenes de resonancia magnética nuclear. Las nanoterapias renales con fármacos es un tema de importancia que tiene 2connotaciones: la protección de fármacos y agentes nefrotóxicos (ej. antibióticos, retrovirales, medios de contraste, etc.) y el desarrollo de nuevos medicamentos para enfermedades renales. La nanoteragnosis renal es una línea prometedora poco desarrollada. Se explicita también el impacto de los soportes nanoestructurados en la regeneración tisular renal. El artículo finaliza con un breve análisis de las perspectivas de la nanonefrología.
After contextualising the generic frameworks of nanotechnology and nanomedicine, the 2disciplines are discussed in the field of Nephrology. The potential downside to nanonephrology is the renal clearance of nanoparticles, the use of which is ever-increasing both for nanomedicinal purposes and in nanofoods. The positive impact of nanotechnology in Nephrology is centred on the development of renal nanodiagnostics for basic renal function studies, the early diagnosis of acute kidney injury, reliable and simple follow-up of chronic kidney disease and the improvement of magnetic resonance imaging. Renal drug nanotherapies comprise an important and dual-faceted area: The protection of drugs and nephrotoxic agents (e.g. antibiotics, antiretrovirals, contrast media, etc.) on the one hand, and the development of new kidney disease medications on the other. Renal ‘nanotheranostics’ is a promising but little-studied area. The impact of nanostructured supports on renal tissue regeneration is also discussed. The article concludes with a brief analysis of the various nanonephrology perspectives.
El estado actual y perspectivas de la nanonefrología es la temática abordada en este artículo. Su título puede parecer pretencioso si se supone que las nanoherramientas van a cambiar las esencias, los pilares de la Nefrología (estudio de la función renal y prevenir/tratar/curar enfermedades del riñón). En realidad, el adjetivo «nueva» se refiere a la incorporación de las tendencias científico-técnicas como la miniaturización, automatización, informatización, nanotecnología, etc., que la han revolucionado técnicamente. En cada década de la segunda mitad del siglo xx se han conseguido logros inimaginables. La irrupción de la nanotecnología en la Nefrología en el siglo xxi ha supuesto el cambio más relevante en su evolución desde el siglo xix.
Cualquier cambio significativo y profundo en una disciplina científica o especialidad médica genera, en general, inquietud, desconfianza y el conservadurismo más férreo. Solo las mentes abiertas, ávidas de innovación, reciben con los brazos abiertos las novedades «revolucionarias». Este es el caso de la nanonefrología, que cambiará en una o 2décadas los servicios de Nefrología en los hospitales. Una aproximación similar ocurrirá cuando la explotación del big data —la denominada minería de datos— sea asequible a muchos profesionales, como los médicos.
Como introducción al tema, se comentan sucintamente a continuación los marcos genéricos donde se encuadra la nanonefrología.
NanotecnologíaEsta nueva tecnología se refiere a los eventos y tamaños que ocurren en la denominada escala nanométrica (de 1 a 100nm), aunque su carácter rompedor no es cuestión del tamaño, ya que algunos materiales cambian radicalmente de propiedades al pasar de tamaño micro a nano (ej. el oro amarillo es verde, azul, rojo a tamaño nanométrico debido al efecto denominado plasmón superficial). La nanotecnología aporta valores añadidos sustanciales en una amplia variedad de áreas tales como la salud, la energía, el hogar, la mecánica, la arquitectura, los sensores, el arte, la agroalimentación, el deporte, la toxicología, el sexo, entre otras. La nanotecnología es, pues, una tecnología trasformadora y revolucionaria con un impacto semejante a la máquina de vapor (siglos xviii y xix), la electricidad (siglo xx) y la informática (siglos xx-xxi)1. En el siglo xxi se han publicado cientos de miles de artículos científicos, se han registrado miles de patentes, creado más de 2.000 empresas start-up de base nanotecnológica y han aparecido 42 revistas nuevas con el prefijo «nano» en su título. Un resumen actual de la nanociencia y la nanotecnología puede encontrarse en el libro de Kumar y Kumbhat2 publicado en 2016.
NanomedicinaEs la vertiente nanotecnológica de mayor impacto económico y repercusión social3. Organizaciones prestigiosas tales como la OMS (ONU) y el NIH (EE. UU.) la consideran como una revolución en las Ciencias de la Salud.
Su objetivo esencial es el desarrollo de nanoherramientas para el diagnóstico, prevención y tratamiento de enfermedades tan relevantes como el cáncer, la diabetes, las cardiovasculares y las neurodegenerativas, en sus estados poco avanzados.
El carácter multidisciplinar de la nanomedicina es innegable. No solo se trata de la obvia combinación de medicina y nanotecnología, sino que otras áreas como la química, la bioquímica, la biología molecular, la genética, así como la física y la ingeniería son esenciales. Es curioso hacer constar lo difícil que es diferenciar con nitidez la nanotecnología de la biotecnología en este contexto.
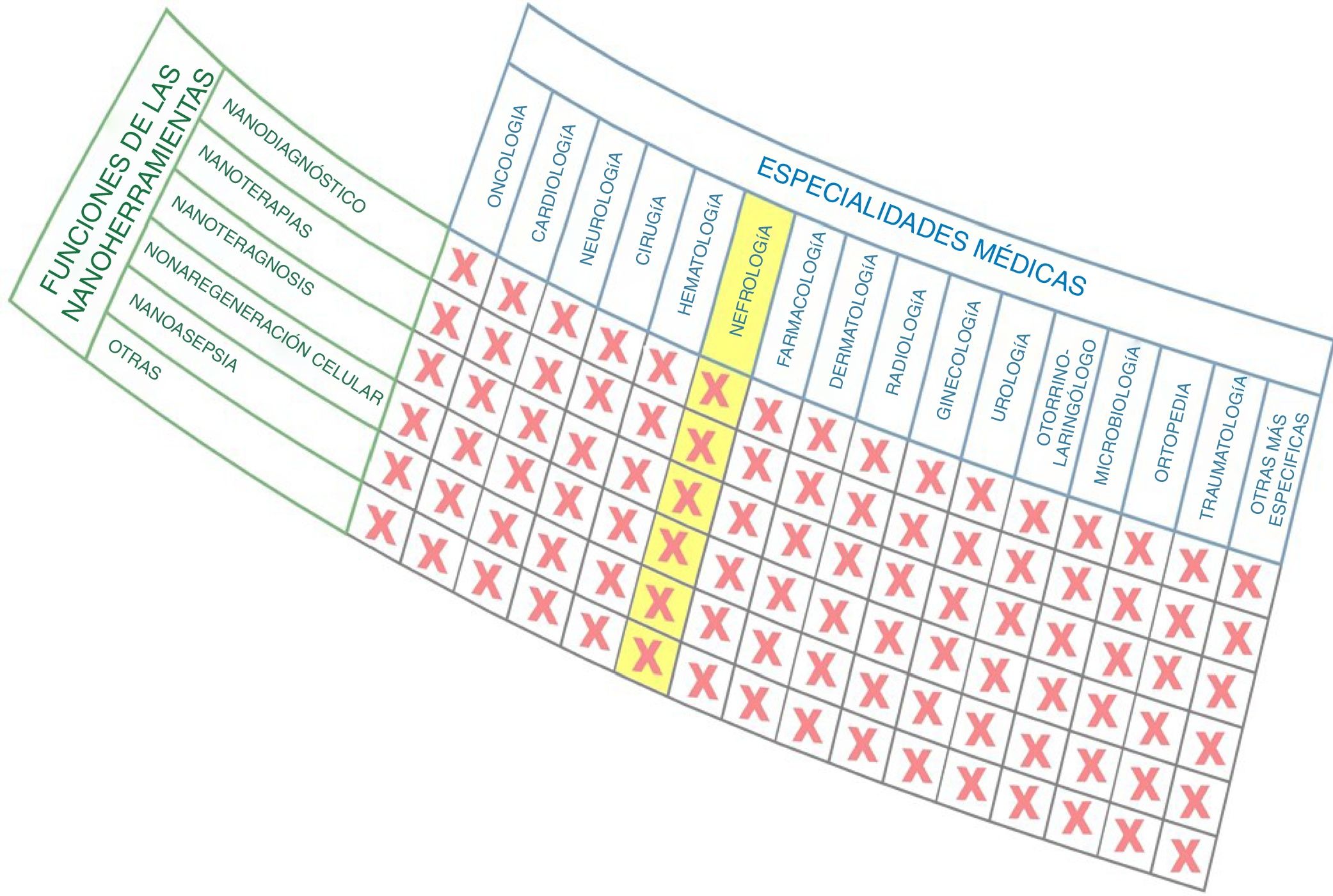
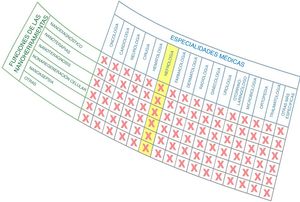
Las posibles clasificaciones para sistematizar la nanomedicina son 2, tal como se puede observar en la figura 1. Por una parte, se puede considerar dividida por especialidades médicas (ej. nanooncología, nanodiabetes, etc.) o bien por las funciones que realizan las nanoherramientas en Medicina: nanodiagnósticos, nanoterapias, nanoteragnosis, nanoasepsia, etc. Obviamente, existe una correspondencia entre ellas. Para la sistematización y descripción de la nanomedicina se considera más útil usar el criterio de las funciones de las nanoherramientas, que son trasversales a todas las especialidades médicas: la otra opción implicaría la descripción artificial de compartimentos estancos. Por ello, se considera conveniente describir el impacto en cada especialidad médica dividiéndola en las funciones que pueden desarrollar las nanoherramientas, tal como se realiza en este artículo para la nanonefrología.
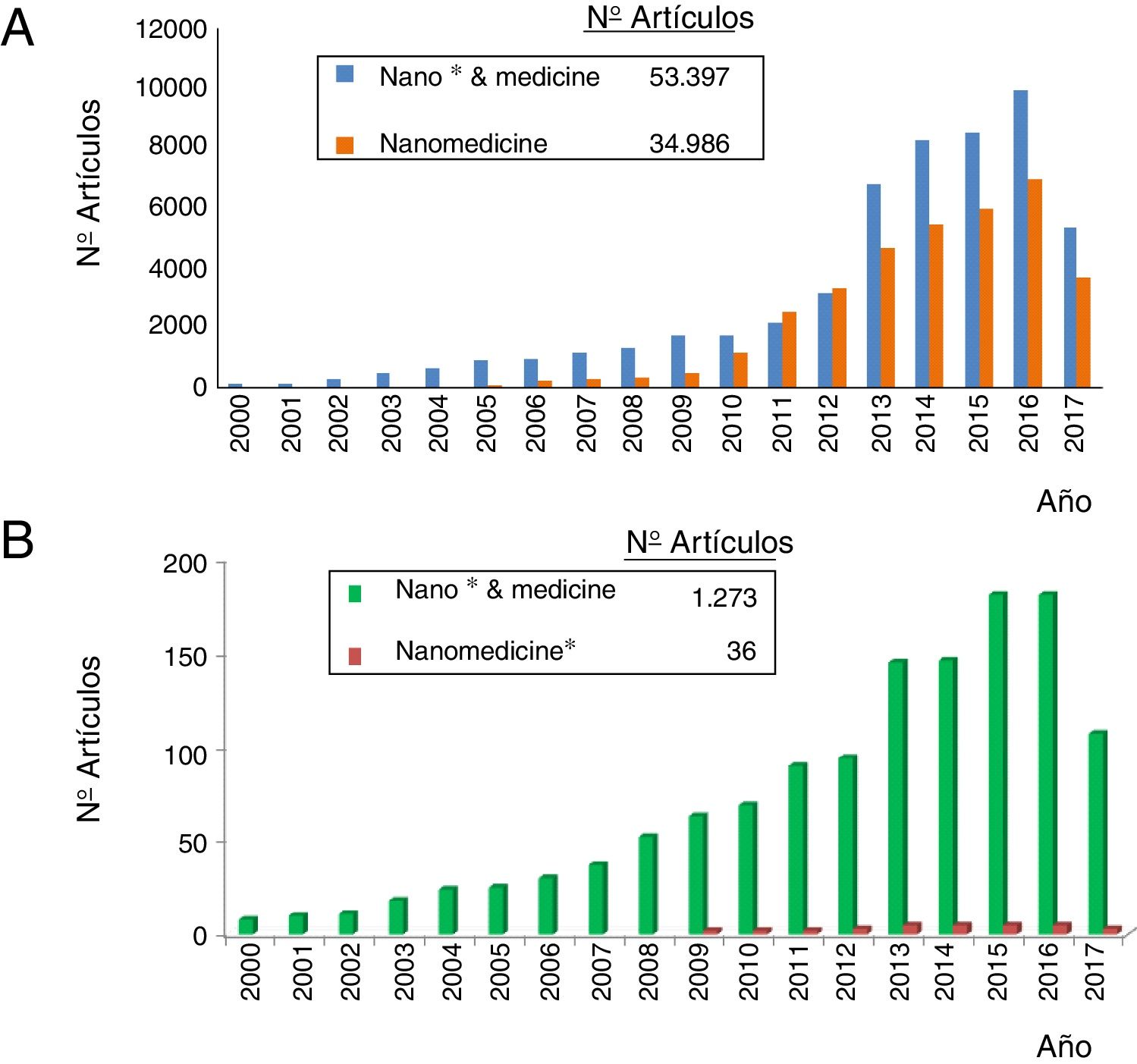
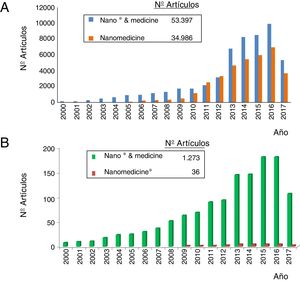
El crecimiento exponencial e incluso lineal desde 2013 de los artículos publicados en nanomedicina se expone en la figura 2A. Hay, pues, más de 50.000 artículos publicados sobre la temática. Obsérvese que, antes del siglo xxi, prácticamente no existían artículos. Se establece la diferencia entre 2búsquedas en la base internacional de datos científicos de la WOS del ISI: artículos que tienen conjuntamente los prefijos «nano» y «medicine» (color azul) y los que tienen el término «nanomedicine» (color rojo). Se constata que más del 70% de los artículos usan este término, lo que implica que está ya en vías de consolidación definitiva en la literatura científica. Otra prueba del afianzamiento de la nanomedicina es su consideración como objeto de divulgación en un libro separado de la colección sobre «Fronteras de la Ciencia» patrocinada por National Geographic, de reciente aparición en los kioscos españoles.
La representación del número de artículos publicados en nanonefrología durante el siglo xxi se muestra en la figura 2B. De esta gráfica se deduce que: 1) El número de artículos en esta especialidad es solo del 2,5% del total de los artículos de nanomedicina; 2) el crecimiento de los artículos en nanonefrología es también exponencial, con un triple escalón bianual y 3) el término nanonefrología está muy lejos de consolidarse todavía (solo se usa en un 3% de los artículos).
Aclaramiento renal de nanopartículasSe trata de una potencial connotación negativa de la nanonefrología. En ausencia de aclaramiento renal o biodegradación en compuestos inertes, las nanopartículas utilizadas con fines diagnósticos o terapéuticos según su naturaleza pueden acumularse en el organismo e inducir toxicidad (muchas de las nanopartículas contienen metales pesados o agentes fluorescentes, por ejemplo). Es pues, un «cuello de botella» el empleo de nanoherramientas para enfermedades en el contexto de la nanomedicina. El artículo de Choi et al.4 publicado en 2007 con más de 2.400 citas es considerado un hito en el tópico. Después se han publicado muchos artículos específicos para nanopartículas determinadas durante 10 años. Como botón de muestra, en 2017ha aparecido un artículo sobre el aclaramiento renal de nanopartículas de metales nobles5.
Las características de las nanopartículas que influyen en su aclaramiento renal son muy variadas y con connotaciones mutuas: naturaleza, forma, cristalinidad, tamaño hidrodinámico, estabilidad y, sobre todo, la actividad superficial (grupos reactivos y cargas). Por ello, la nanoencapsulación es una estrategia muy prometedora en nanomedicina, ya que el recubrimiento (ej. PEG, cisteína, dendrómetros, liposomas, etc.) de un medicamento nefrotóxico (ej. retrovirales, agentes quimioterápicos, antiinflamatorios, etc.) permite que durante su aclaramiento renal no provoque daño. Existe una regla general bastante aceptada, con sus excepciones: existe un aclaramiento aceptable cuando el diámetro hidrodinámico de las nanopartículas es inferior a 5-15nm, que mejora si son nanopartículas bioquímicas (ej. biopolímeros) y orgánicas (ej. liposomas y dendrímetros). Como ejemplo, tras la inyección intravenosa de quantum dots marcados con Tc99m, aquellos con un diámetro hidrodinámico pequeño (4,36nm) se aclaran con una vida media de 48 min, mientras que los de diámetro hidrodinámico mayor (8,65nm) presentan una vida media de 20 h5. A modo de comparación, el tamaño hidrodinámico de la inulina es 3nm.
La presencia de nanopartículas en el organismo humano puede deberse a:
Incorporación directa, voluntaria y, por tanto, controlada de nanopartículas debido al empleo de nanoherramientas con fines terapéuticos (ej. nanotubos de carbono), diagnósticos (ej. quantum dots para bioimágenes), teragnósticos (ej. nanopartículas de oro), de asepsia (ej. nanopartículas de plata) en el ámbito de la nanomedicina.
Incorporación involuntaria y no controlada de nanopartículas por una amplia variedad de causas: contaminación de aguas y aire, ingestión de nanoalimentos, contacto con productos de base tecnológica (ej. cosméticos), etc.
Los mecanismos de eliminación renal de las nanopartículas son muy variados, pero, en general, son de 2tipos: directos, a través de la filtración glomerular, e indirectos, cuando se eliminan productos de biodegradación de las nanopartículas en el organismo. Esta segunda vía de eliminación, hepática, está diseñada para captar y eliminar aquellas con tamaño entre 10 y 20nm de diámetro hidrodinámico (como, por ejemplo, los virus), pero es un proceso mucho más lento que la vía renal.
Nanodiagnósticos renalesEsta es la primera aplicación del uso de nanoherramientas que contribuyen a mejorar la Nefrología que se describe en este artículo. Los nanodiagnósticos renales han incrementado nítidamente la capacidad de monitorizar enfermedades renales incluso en sus primeros estadios, así como de facilitar con nitidez un estudio más profundo y fiable de la función renal.
Estudios nanotecnológicos de la función renalLos estudios in vitro (simulaciones artificiales de sistemas biológicos), ex vivo (experimentos en tejidos o células extraídas de un organismo vivo) e in vivo (experimentos en animales y humanos) de la función renal son mucho más eficientes si tienen base nanotecnológica. Los resultados y conocimientos (resultados tratados, contextualizados, discutidos y que permitan la toma de decisiones) adquiridos son la plataforma para los avances de la Nefrología en todas sus facetas. La evolución deseable de estos estudios es que sea desde in vitro hasta in vivo para materializarse, si hay éxito, en fármacos, sistemas y tratamientos asequibles a los enfermos en la clásica secuencia I+D+T.
Una de las aportaciones más relevantes en este contexto la ha desarrollado el Instituto Wyss de la Universidad de Harvard bajo la dirección del profesor Donald Ingber. Se combina micro- con nanotecnología en una aproximación genérica denominada organs-on-chips (OOC)6,7 aplicables al estudio de diversas enfermedades, entre ellas, la renal. Los OOC son plataformas de polímeros transparentes con microcanales en su seno para introducir y evacuar líquidos a la plataforma central que contiene una tira de 4mm de ancho y 3-5cm de largo de un soporte (scaffold) nanotecnológico en el que se retienen y crecen las células vivas. Esta plataforma está siendo observada continuamente por un microscopio óptico de fluorescencia, lo que permite obtener imágenes de alta resolución en tiempo real e in situ cuando pasan por las células diferentes agentes (ej. tóxicos, medicamentos, etc.). Así se realizan estudios ex vivo más eficientes para el descubrimiento de medicamentos para inducir/combatir daños renales, para determinar la nefrotoxicidad de otros medicamentos, para identificar biomarcadores, para estudiar los mecanismos moleculares, etc., sin necesidad de la experimentación animal. Esta plataforma obtuvo el Premio Nacional de Diseño Industrial en EE. UU. en 2015.
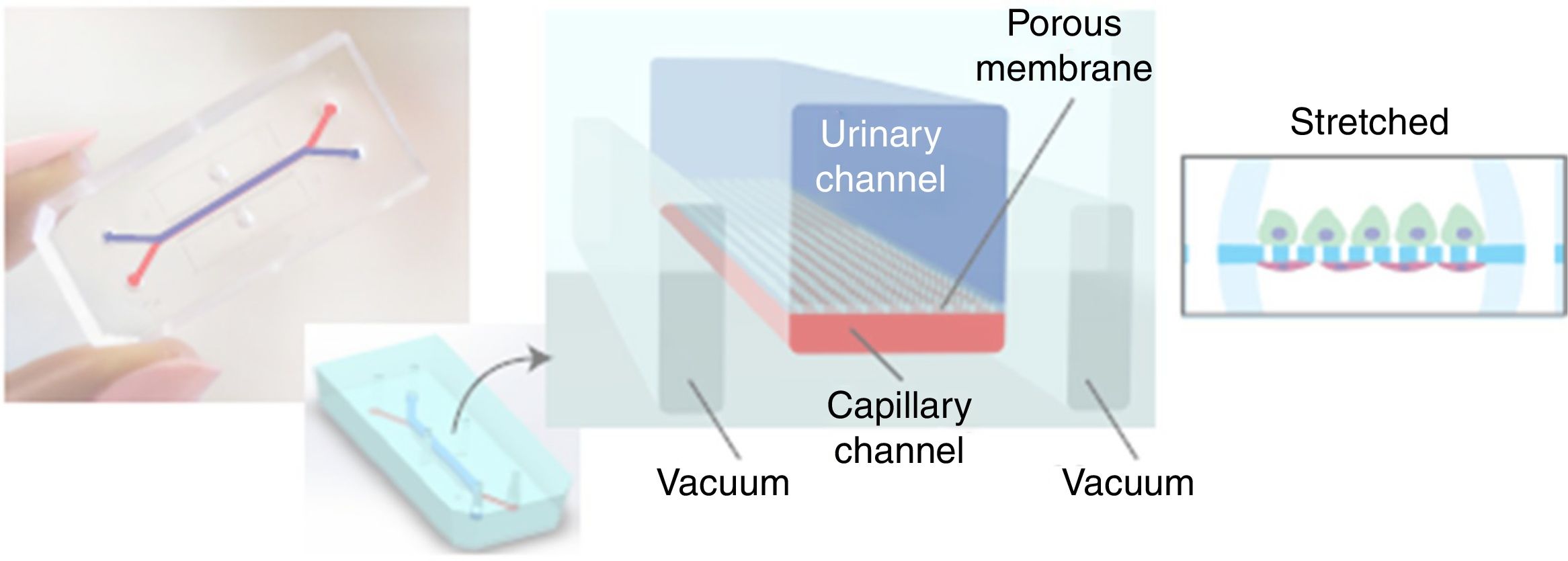
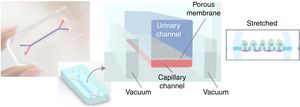
El mismo equipo médico de la Universidad de Harvard acaba de dar a conocer en junio de hace un año año la creación ex vivo de un glomérulo renal en una aproximación más específica que la anterior. En la figura 3 se muestra un esquema de este glomérulo en un chip8. El seguimiento se realiza también con un microscopio óptico de fluorescencia. Se basa en el mismo chip microfluídico (OOC) con microcanales que replican el compartimento urinario (en azul) y capilar (en rojo) del glomérulo. La membrana basal glomerular es reproducida usando una membrana nanoporosa con la proteína laminina, que es parte de la matriz extracelular. La membrana de polidimetisiloxano no es rígida y debe ser tensionada (estirada) mediante un sistema de vacío que funciona cíclicamente. El glomérulo «humano» incorpora células derivadas de cultivo primario de células endoteliales humanas y células madre pluripotenciales inducidas para su transformación en podocitos. Las imágenes en tiempo real obtenidas son espectaculares y muestran la capacidad fisiológica de filtración de inulina y albúmina y la posibilidad de crear un modelo in vitro de podocitopatía mediante nefrotoxicidad por adriamicina.
Replica fotográfica y esquemática en un organ-on-a-chip microfluídico de los compartimientos urinario (color azul) y capilar (color rojo) del glomérulo renal. Una membrana flexible de silicona nanoporosa separa ambos compartimentos. El montaje de vacío cíclico es necesario para que la membrana artificial glomerular se vuelva rígida.
Fuente: Musah et al.8, con permiso de Macmillan Publishers Ltd., 2017.
Se trata de aplicar la nanotecnología y sus herramientas para mejorar nítidamente los resultados de los diagnósticos renales habituales en la actualidad. Se exponen aquí algunos ejemplos representativos.
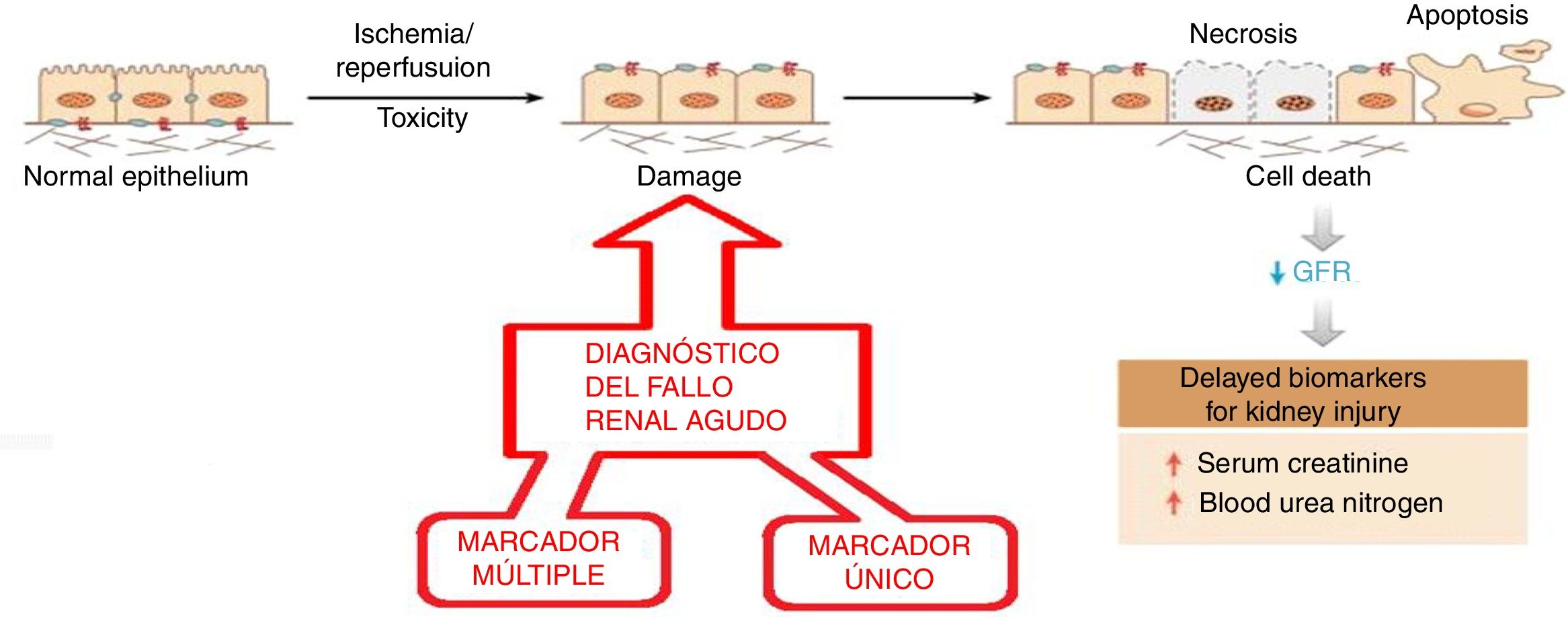
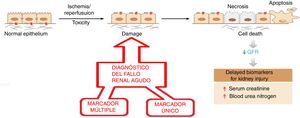
El diagnóstico precoz del fallo renal agudo es siempre un reto en Nefrología. Tal como puede verse en la figura 4, el epitelio normal se daña por agentes tóxicos o isquemia/reperfusión. Es preciso un indicador eficiente para poner de manifiesto el inicio de estos daños para aplicar urgentemente la terapia adecuada. Si no se actúa, se produce necrosis, apoptosis y muerte celular. La caída en picado del aclaramiento renal se pone de manifiesto con el espectacular incremento de los indicadores nitrogenados ordinarios: concentraciones de creatinina en suero y de urea en sangre que certifican el daño tisular. Como se observa en la figura 4, existen 2enfoques para el diagnóstico. La estrategia del marcador múltiple9 consiste en medir la proporción relativa entre sí de 14 biomarcadores en orina con un sistema fluorimétrico basado en una combinación de microfluídica y nanotecnología y el tratamiento quimiométrico de los datos; el diagnóstico es binario y tiene una fiabilidad del 99% (no se producen falsos negativos). La estrategia del marcador único10 se basa en un nanorreactivo (inmunosensor basado en un nanoanticuerpo extaído del camello) que detecta la lipocalina asociada a una neutrofil-gelatinasa, que es un marcador precoz del fallo renal agudo; el nanorreactivo se inmoviliza sobre un electrodo de titanio para una detección basada en la espectroelectroquímica; el procedimiento es simple, rápido, selectivo (respecto a otras macromoléculas en la orina) y ha demostrado una gran precisión y exactitud.
Evolución del fallo renal agudo desde epitelios no dañados. Se señala el momento de aplicación de 2 tipos de nanomarcadores (simple y múltiple) para el diagnóstico precoz.
Fuente: Adaptado de la Vaidya et al.9, con permiso de HHS PublicAcess.
La detección o el seguimiento de la enfermedad renal crónica (ERC) se hace rutinariamente con los marcadores nitrogenados ordinarios en sangre mediante análisis clínicos. La nanotecnología ofrece soluciones ingeniosas para abordar este tipo de diagnóstico. Tal es el caso de la diferenciación simple de los diferentes estados de la ERC (desde individuos sanos hasta los que presentan insuficiencia renal crónica avanzada) mediante el análisis directo del aliento11. Este diagnóstico se fundamenta en que el estado renal cambia la proporción entre sí de más de 40 compuestos orgánicos volátiles. Se utilizan para ello nanotubos de carbono recubiertos como sensores en el instrumento denominado «nariz electrónica», asequible comercialmente. Mediante el empleo de la metodología quimiométrica de análisis de componentes principales para examinar los resultados de más de 1.000 individuos, se demuestra una capacidad de discriminación entre estados del 95% y que las diferencias de humedad del aliento no influyen significativamente.
La morfología del glomérulo renal se determina cuantitativamente con la prueba diagnóstica de análisis de imágenes por resonancia magnética nuclear empleando como marcador el gadolinio. La nanotecnología aporta en este contexto un nanomarcador denominado nanoferritina, que se enlaza prioritariamente a la membrana glomerular12 cuando se inyecta una disolución intravenosa de una suspensión del nanomarcador. Así pues, se consigue una alta selectividad renal, la reducción de la toxicidad del gadolinio y los resultados conseguidos (número y tamaño de las nefronas, volumen renal, velocidad de filtración, etc.) para definir los factores que contribuyen a la ERC son altamente fiables.
Uno de los nanomateriales más importantes en la actualidad por su aplicabilidad en medicina es el grafeno. Su aplicación como biosensor, al unirse a redes de nanopartículas de oro, ha permitido crear un sensor portátil de glucosa, temperatura, humedad y pH en el sudor de pacientes diabéticos. Este sistema es capaz además de administrar por vía subcutánea fármacos como metformina a través de microagujas poliméricas de grafeno activadas térmicamente13.
Recientemente se ha desarrollado un biosensor basado en un compuesto de MoS2-grafeno que permite medir la concentración de hormona paratiroidea en suero de pacientes con enfermedad renal, de forma lineal en el rango ente 10 y 1.000 ng/ml y validado frente a un inmunoanálisis comercial de uso clínico14. Por otra parte, el grafeno puede tener efecto citotóxico directo e inducir necrosis y apoptosis celular15, pero su utilización como óxido de grafeno en forma de hojas bidimensionales ha mostrado ser inerte para el riñón y es filtrable por el capilar glomerular en modelos animales. No induce lesión a nivel podocitario, endotelial ni en la barrera de filtración glomerular16.
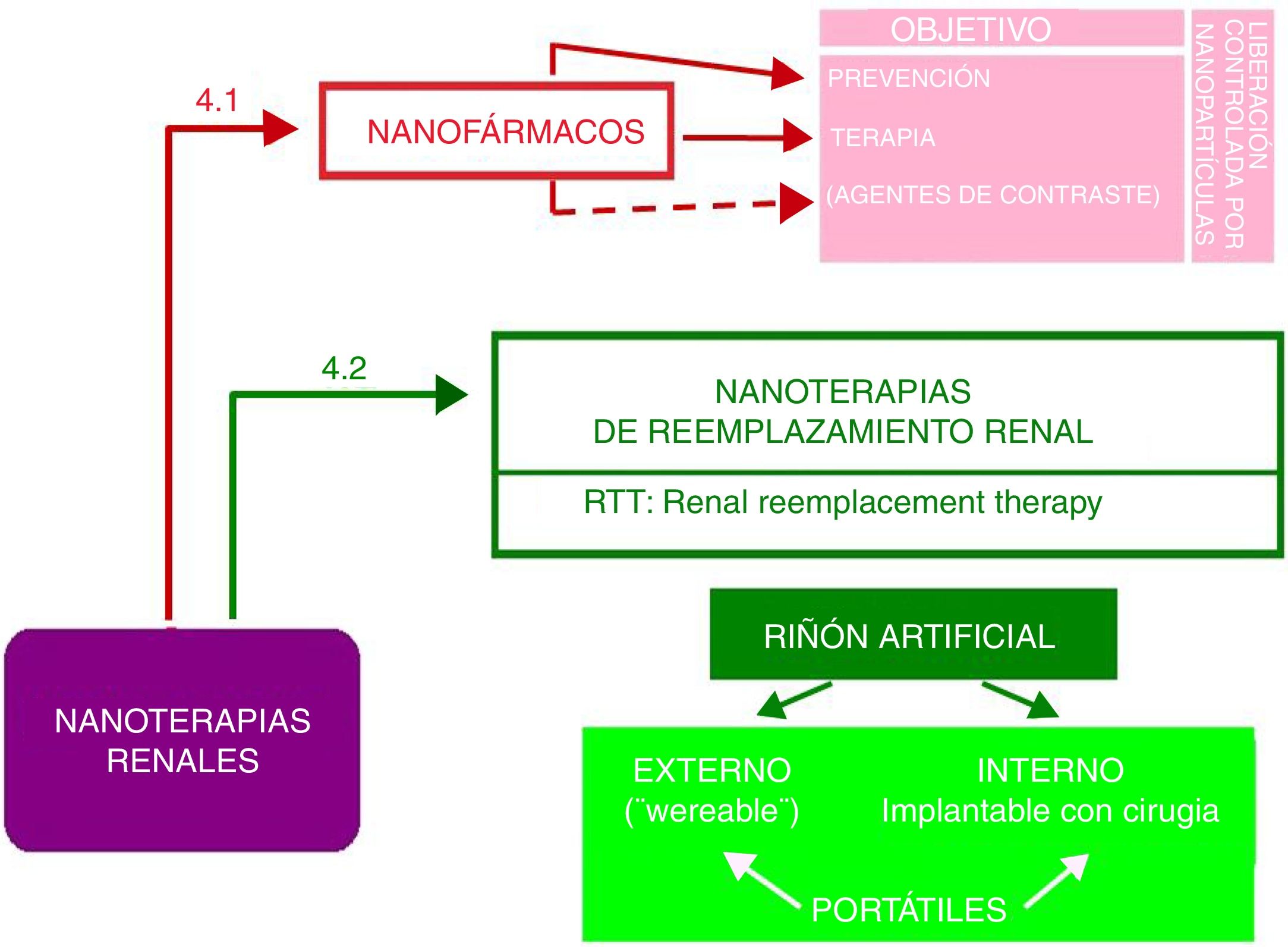
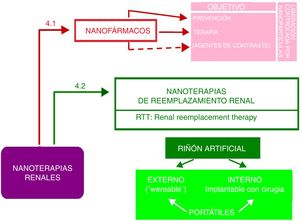
Nanoterapias renalesLa nanotecnología ha posibilitado mejoras importantes en las terapias para prevenir y tratar enfermedades del riñón. Es la rama de la nanonefrología con más referencias bibliográficas. Deben distinguirse 2tipos muy distintos de nanoterapias entre sí, como se muestra en la figura 5, que servirá de guía para este apartado.
Según se muestra en la figura 5, los nanofármacos para el riñón pueden tener 2objetivos: prevenir y tratar enfermedades renales. Algunos autores17 incluyen también los medios de contraste de imagen como nanofármacos, aunque los autores de este artículo los consideran en el apartado de diagnóstico (ej. nanoferritina en resonancia magnética nuclear renal12). Otra posibilidad trasversal es que estos fármacos se liberen de forma controlada encapsulados en nanopartículas, como liposomas, dendrímeros, polietilenglicol, etc. Esta temática de la nanonefrología que es tan prometedora no ha recibido suficiente atención por parte de los investigadores y es un reto abordarla urgentemente. Se exponen 2ejemplos representativos de nanofármacos para la protección renal y para el tratamiento de enfermedades renales.
La protección del riñón por nanoencapsulación de medicamentos nefrotóxicos, tales como agentes de contraste, antibióticos, retrovirales e antiinflamatorios ampliamente usados por pacientes, pero vetados para enfermos renales, es una de las temáticas más prometedoras de la nanomedicina. Un ejemplo característico desarrollado por Serrano et al.18 es la nanoencapsulación (con un polímero derivado del citosano) de la anfotericina B, con la que se consigue la administración oral del antifúngico, con una biodisponibilidad del 24% y una eficacia similar a la de la anfotericina liposomal administrada parenteralmente, pero reduciendo la exposición renal del fármaco y, con ello, su nefrotoxicidad. Además, esta novedosa nanopartícula previene la degradación de la anfotericina B por el medio ácido del estómago. Se ha demostrado la eficacia de esta nanoencapsulación en el tratamiento de leismaniosis, aspergilosis y candidiasis en modelos animales. El daño renal (ej. inflamación, fibrosis, muerte celular, etc.) puede ser tratado de forma eficiente con nanomedicamentos19,20, aunque no se ha demostrado plenamente hasta ahora. Es necesaria una investigación más extensa y profunda para que estos fármacos con base nanotecnológica cumplan 2objetivos: liberación contralada desde la nanopartícula y tener como órgano-diana el riñón (GTT: glomerular tubular targeting). Es prometedor el empleo de nanopartículas poliméricas hidrofílicas que faciliten el transporte selectivo al interior del riñón. Una reciente y excelente revisión sobre este tópico demuestra la importancia de la nanomedicina en el tratamiento de tumores y enfermedades renales21.
Nanotecnologías para el reemplazo renalEl mayor impacto de la nanotecnología en la Nefrología es el desarrollo de un riñón artificial implantable por cirugía que minimice el trasplante renal de donantes de cadáver o entre vivos y reduzca o elimine la diálisis; ello supone un punto de inflexión en el desarrollo de los hemodializadores. Los macrodializadores del considerado «padre» de la hemodiálisis (Kolhf, 1943) han ido incorporando tendencias científico-técnicas como la miniaturización, automatización e informatización y, al principio del siglo xxi, son indudablemente más pequeños y muchomás eficientes, más biocompatibles y más autocontrolables; incluso se ha facilitado su diseño para usarse en el domicilio de los pacientes.
La descripción de los riñones artificiales portátiles en la literatura es muy difusa y poco transparente. Se encuentran muchos artículos divulgativos cortos, sin detalles técnicos, y videos con más intención de propaganda que de divulgación científica. La causa de esta situación es que existen patentes que impiden una descripción transparente. Muchos aspectos quedan oscuros (ej. duración de un riñón artificial implantado por cirugía).
Según puede verse en la figura 5, el riñón artificial, que siempre es «portátil», puede ser externo o interno respecto al organismo al que se incorpora.
Al riñón artificial externo, se le denomina en inglés «weareable», que equivaldría a «ponible» o de «quita y pon» en castellano. Son cinturones que incorporan todos los elementos para realizar hemodiálisis. Requieren, lógicamente, un acceso vascular doble para sortear el riñón dañado. Muchos autores coinciden que es una posibilidad de poco recorrido, aunque uno de sus últimos modelos ha sido aprobado por la FDA de EE. UU. Durante 12-14 h realiza la función de un dializador ordinario en 3-4 h22.
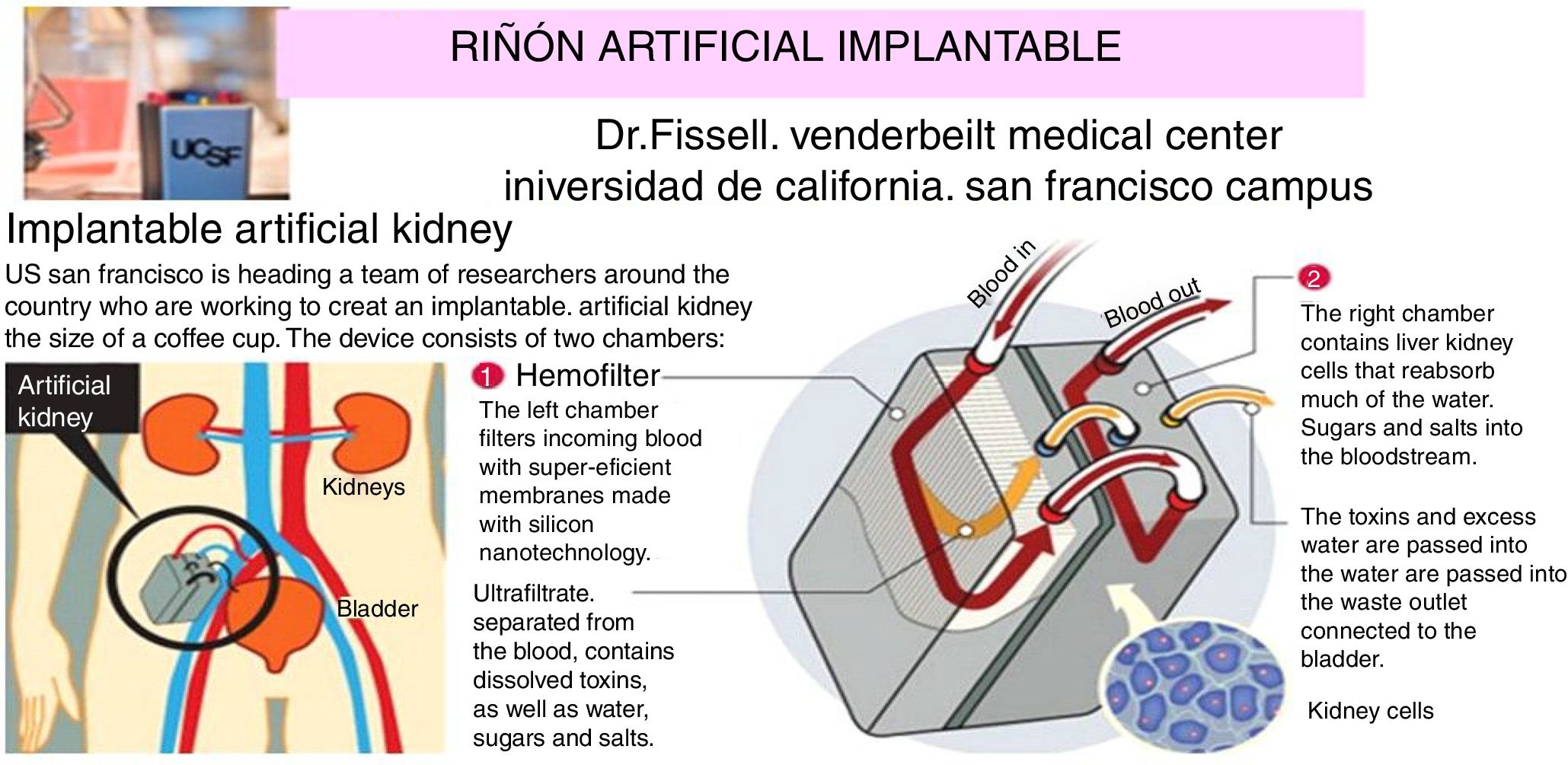
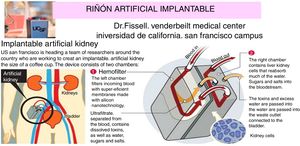
El riñón artificial interno es el que se implanta mediante cirugía, es decir, como si fuera un riñón natural donado. En la figura 6 se muestra esquemáticamente el riñón artificial que ya está en ensayos en humanos (2017-2018) en el Centro Médico Venderbeit de la Universidad de California (Campus de San Francisco [UCSC])23,24 bajo la dirección del Dr. Fissell. El riñón artificial tiene 2compartimentos: 1) compartimento del filtro de sílice nanoporoso que tiene: un input (entrada de la corriente sanguínea, en rojo), y 2outputs (el de la sangre filtrada y el del ultrafiltrado, en naranja) que contiene toxinas, sales, agua, azúcares, etc. La membrana nanotecnológica de sílice filtra muy eficientemente las sustancias que pasan al ultrafiltrado; y 2) compartimento-biorreactor con células renales vivas que tiene: 2inputs (el de corriente sanguínea filtrada y el del ultrafiltrado que procede del anterior compartimento) y 2outputs (el de la sangre tratada a las células renales que han reabsorbido los azúcares, sales y parte del agua, el de la «orina» conectado a la vejiga que contiene las toxinas y el exceso de agua) y un output (toxinas, exceso de agua), que va a la vejiga.
Riñón artificial implantable con cirugía en desarrollo en la Universidad de California.
Fuente: Universidad de California, Campus de San Francisco23,24. Para detalles, ver texto.
En vías de desarrollo se encuentra el riñón-en-un-chip implantable25, que es diferente a los que se diseñan para estudios renales ya comentados en el apartado de nanodiagnósticos renales. El mismo equipo de la Universidad de California-San Francisco ha combinado la micro- y la nanotecnología (con el mismo enfoque que el modelo macro anterior: combinación de filtro nanotecnológico y células renales vivas (VO Inside). Para replicar el funcionamiento de un riñón se necesitan 15 microchips nanotecnológicos que se apilan en un compartimento plástico de tamaño 5veces inferior respecto al macroriñón artificial anterior. Esta tecnología está en sus primeras etapas de configuración, lejos todavía de los ensayos en animales y humanos. La miniaturización es muy prometedora, dado que permitirá el implante quirúrgico y la portabilidad del riñón artificial de forma simple y cómoda.
Nanoteragnosis renalesLa combinación on time, in situ e in vivo de terapias y diagnósticos (y viceversa) se denomina teragnosis. Se desarrolló a finales del siglo xx. La irrupción de la nanotecnología ha originado la nanoteragnosis26-28, que es una de las líneas más prometedoras de la nanomedicina. Las nanopartículas inorgánicas (ej. de oro, de sílice mesoporosa, etc.), orgánicas, (ej. dendrímeros, liposomas, nanotubos de carbono, etc.) o biológicas (ej. biopolímeros) hacen de nanotransportadores, en su interior o en su superficie, de los demás componentes: agentes terapéuticos, agentes diagnósticos, agentes orientadores y agentes antiagregantes/repulsores de otras (macro)moléculas en el torrente sanguíneo.
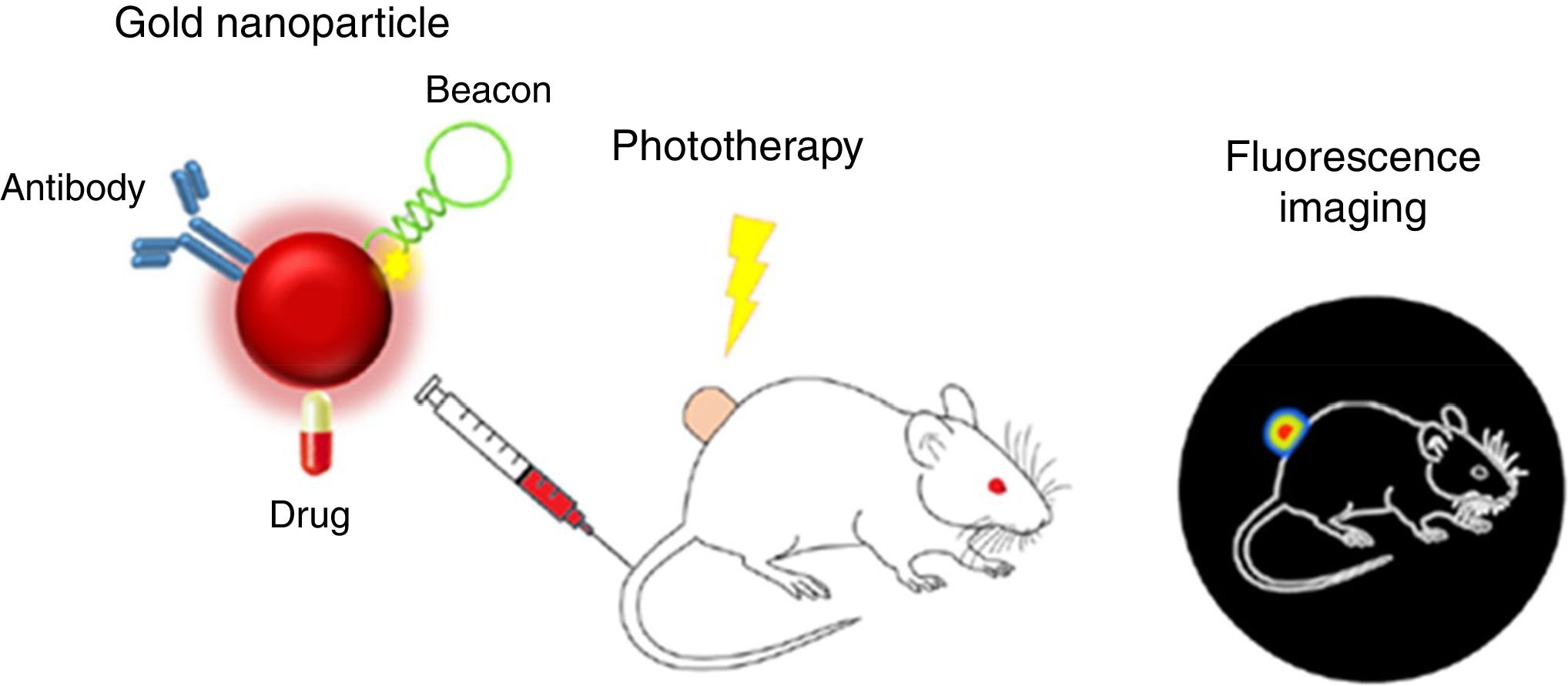
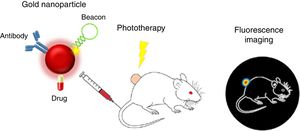
Han sido escasas las propuestas nanoteragnósticas para enfermedades renales, lo que implica una gran oportunidad de I+D+T, toda vez que, como se ha indicado, los nanomedicamentos específicos para el riñón necesitan un mayor desarrollo. Un espectacular ejemplo de nanoteragnosis para cáncer renal29 se basa en el empleo de nanopartículas de oro (de color rojo por su tamaño de 15nm) como nanocarriers, que además convierten la energía lumínica de un láser en térmica e inhiben la florescencia de fluoróforos en su superficie. El orientador direccional es un anticuerpo que enlaza con los antígenos del tumor renal y «ancla» a la nanopartícula teragnóstica. Las horquillas de ADN que tienen acoplados fluoróforos actúan de nanofaros: cuando llegan al tumor renal se separan y se emite una intensa fluorescencia. El agente terapéutico es un quimioterápico típico (como el 5-fluorouracilo). En la figura 7 se representa el agente nanoteragnóstico y cómo su suspensión se inyecta en el animal por vía intravenosa. Cuando llega al tumor renal se ancla y se genera fluorescencia por desprendimiento de las horquillas de ADN. El efecto quimioterápico del fármaco es potenciado por un rayo láser externo dirigido a la zona fluorescente, ya que eleva la temperatura del tumor a 45°C. Es un ejemplo espectacular de la combinación de 3terapias: la génica, la térmica y la química.
Nanoteragnosis para el cáncer renal de un ratón.Fuente: Pedrosa et al.29. Para detalles, ver texto.
Una de las primeras líneas trasversales de la nanomedicina (ver fig. 1) fue la nanorregeneración tisular y celular mediante el empleo de soportes (scaffolds) de estructura nanotecnológica orgánica (ej. nanotubos de carbono, nanocelulosa y derivados) o inorgánicos (ej. quantum dots, sílice mesoporosa) o biológicos (ej. empleo de tejido renal limpio como tal30) en lugar de los habituales. Las ventajas de los scaffolds nanotecnológicos31 son: A) alta citocompatibilidad; B) mimetizar la matriz nativa extracelular; C) promover la adhesión de células y su proliferación y D) mejorar las propiedades (mecánicas, eléctricas, magnéticas, catalíticas, ópticas) de los soportes microestructurados convencionales. Su comercialización ha comenzado ya. Una interesante revisión sobre nanotecnología aplicada a ingeniería tisular ilustra ejemplos concretos sobre este punto32.
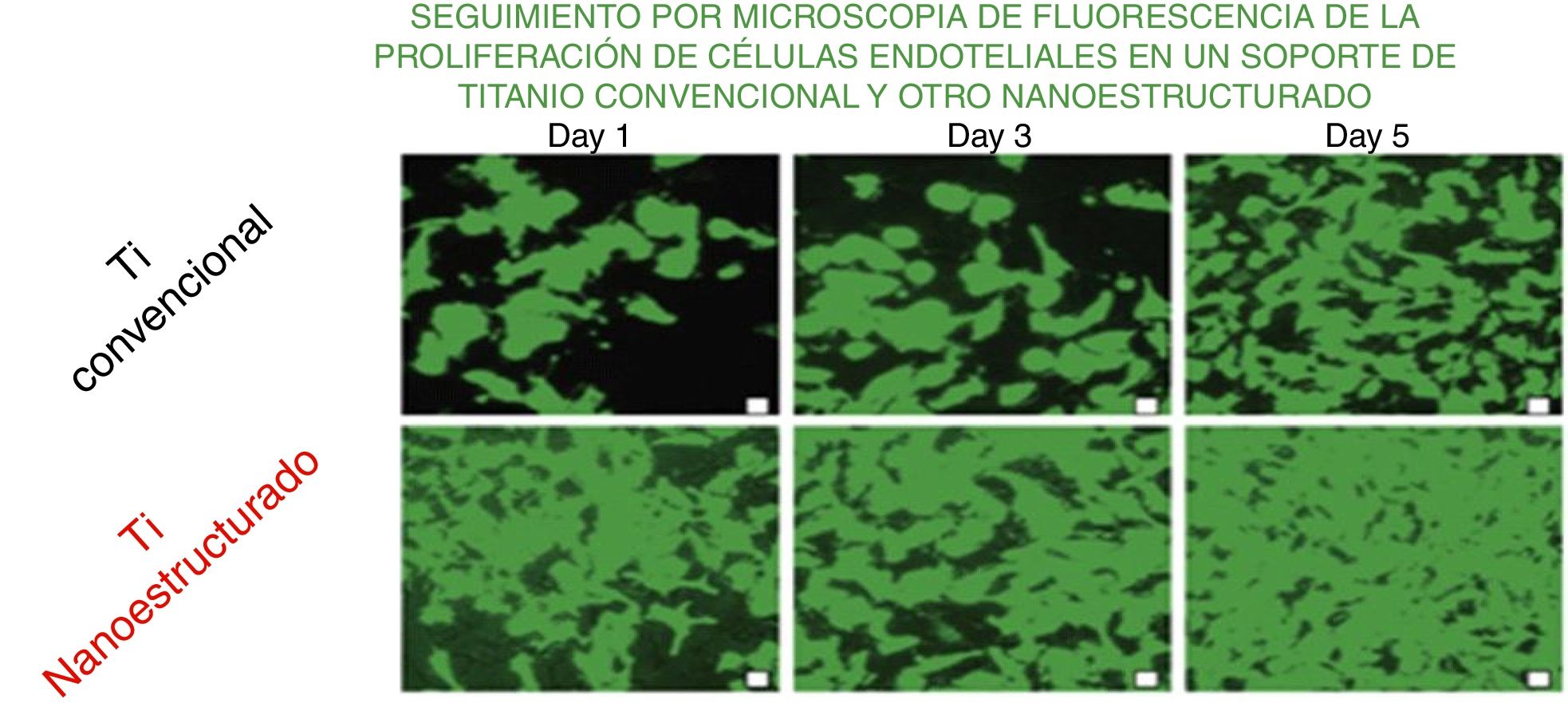
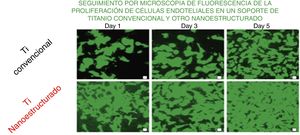
Un ejemplo relacionado con el ámbito renal es el crecimiento de las células epiteliales, que son claves en los capilares del glomérulo33. En la figura 8 se representa el seguimiento por microscopia óptica de fluorescencia de la proliferación de estas células en soportes convencionales y nanoestructurados durante 5 días. Se observa que el crecimiento es cada vez mucho mayor si se usa el soporte nanoestructurado.
Comparación del crecimiento de células endoteliales en soportes convencional y nanoestructurado.
Fuente: Adaptado de Zhang y Webster33 con permiso de Elsevier Ltd., 2008.
En este contexto cabe mencionar que el interés por las células madre se ha revitalizado gracias a la nanotecnología en la denominada stem cell nanotechnology34, que tiene importantes connotaciones: 1) aislamiento de células madre mediante nanopartículas magnéticas; 2) nanotubos de carbono modificados para introducir genes en las células madre; 3) soportes de nanotubos de carbono para la proliferación y diferenciación de células madre y 4) nanopartículas (ej. quatum dots) para análisis de imágenes muy fiables de las células madre.
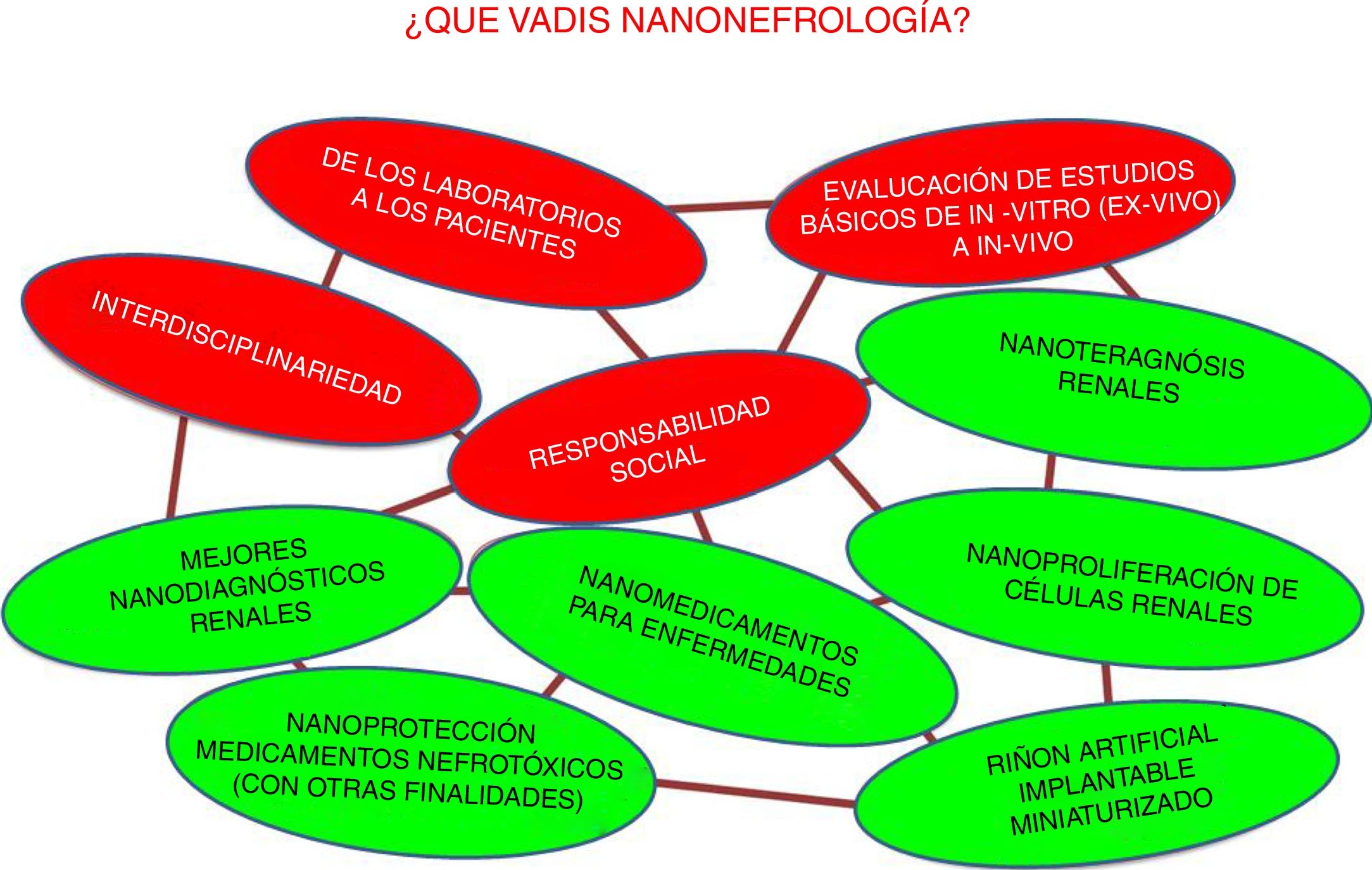
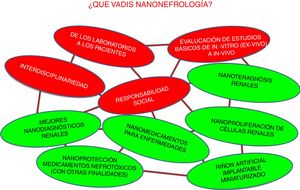
¿Quo vadis nanonefrología?Las tendencias que pueden vislumbrarse o desearse para la nanonefrología se muestran esquematizadas en la figura 9. En realidad, se trata de una red, ya que existe una relación entre sí. Por colores se distingue entre las genéricas y las específicas.
Las 4tendencias genéricas de la nanonefrología coinciden en gran manera con las de la nanomedicina (fig. 9 en rojo) y son:
- 1.
Dar continuidad a la secuencia I+D+T para que los desarrollos de investigación básica lleguen a los enfermos. En este contexto, es recomendable la lectura del artículo de Ionannides de 2016 con el título «Why most clinical research is not useful?»35 que analiza las causas del desvío de los objetivos que debe tener la investigación clínica, lo que ocurre en otras disciplinas, como la química36, por igual. La mala praxis de la evaluación científica vigente (sobrevaloración del número de artículos publicados) junto con el extraordinario beneficio económico de las editoriales científicas37 propician un ambiente en ciencia y tecnología en el que la publicación predomina sobre la utilidad, y que debería erradicarse.
- 2.
Como consecuencia de lo anterior, debería reforzarse la evolución traslacional de los estudios nanonefrológicos desde la investigación in vitro (o ex vivo) a in vivo, lo cual implicaría un valor añadido a la publicación.
- 3.
En la interdisciplinariedad (las interfaces científico-técnicas) se encuentran los grandes avances para que los desarrollos nanonefrológicos lleguen a los enfermos renales. Esta característica es innata en la nanomedicina.
- 4.
Al igual que la nanomedicina, la nanonefrología ofrece aportaciones muy valiosas, ordinariamente asociadas a cambios que pueden suponer billones de euros. Por ello, es imprescindible abordar su responsabilidad social en coherencia con las tendencias genéricas en ciencia y tecnología38. Ello implica considerar sistemáticamente temas tales como trasparencia, comportamiento ético, rendición de cuentas, cumplimiento de la legalidad vigente, etc.; todas ellas orientadas a satisfacer con prioridad las necesidades de los enfermos, que son las partes interesadas (stakeholders) más relevantes sobre los intereses de médicos, hospitales, empresas y gobiernos.
Las tendencias específicas de la nanonefrología se basan en las genéricas y suponen la materialización de las líneas iniciadas descritas en este artículo. Las más relevantes, también mostradas en la figura 9, son:
- •
Riñón artificial implantable por cirugía miniaturizado y de larga duración.
- •
Mejora nítida de los diagnósticos renales mediante la nanotecnología.
- •
Nanoprotección renal de medicamentos nefrotóxicos tales como algunos antibióticos, retrovirales, medios de contraste para análisis de imágenes (TAC, resonancia magnética nuclear).
- •
Medicamentos de base nanotecnológica específicos para enfermedades renales tales como cáncer, fibrosis, infecciones, etc.
- •
Desarrollo de procesos nanoteragnósticos renales.
- •
Nanorregeneración eficiente de células renales y
- •
Otras que surgirán en un futuro inmediato.
Este artículo no tiene como finalidad ser una revisión sobre la nanonefrología, de la que se han publicado más de 1.300 artículos a finales de 2017. Los autores han seleccionado el material más representativo para ofrecer un overview que muestre un state-of-the-artand prospects genérico con ejemplos para ilustrarlos.
La nanonefrología está todavía en sus primeros estadios de aprovechamiento de las nanoherramientas para mejorar nítidamente los diagnósticos, las terapias y las teragnosis renales, así como para potenciar el estudio de la función renal.
La orientación de este artículo no es tratar de «vender» la nanonefrología como la panacea de la Nefrología. La intención real de los autores es solo abrir una ventana a una potencial tecnología que puede revolucionar la Nefrología actual. En realidad, los autores se dirigen a los jóvenes nefrólogos para que se incorporen plenamente a la innovación con una mínima garantía de éxito tanto en sus publicaciones como en la mejora real de la Nefrología.
El enorme potencial de la aplicación médica de la nanotecnología en el diagnóstico y la terapia se completa con el desarrollo paralelo de las «ómicas» —proteómica, peptidómica, transcriptómica, genómica y metabolómica—, cuya aplicación genera una ingente cantidad de información que es imposible procesar con los medios ordinarios de gestión de datos. Así nace el big data y la necesidad de explotar esa exorbitante montaña de datos que se generan diariamente en medicina, tanto en la investigación como en los registros clínicos basados en historias de salud digitales39. Se calcula que la información biomédica disponible se va a duplicar cada 18-24 meses durante los próximos años. La necesidad de disponer y gestionar adecuadamente estos datos ha provocado el nacimiento de 2nuevos términos: la minería de datos y el machine learning. El primero es un campo de la estadística y las ciencias de la computación que trata de descubrir patrones en grandes volúmenes de datos40. Para ello, se utiliza la inteligencia artificial y el aprendizaje automático. El machine learning es una rama de la inteligencia artificial en la que los ordenadores desarrollan algoritmos de aprendizaje automático a partir de bases de datos —con millones datos— sin necesidad de ser programados. La regresión lineal o la regresión logística pasan a ser superadas por las redes neuronales, los vectores (support vectors machines) y árboles de decisión (random tree, random forest). Estos nuevos sistemas de análisis de datos ya se están aplicando en el campo de la Nefrología41. Uno de los retos de la explotación del big data es precisamente mantener la confidencialidad de los datos personales en un entorno seguro pero a la vez accesible para integrar la información y poder explotarlos de manera eficiente y productiva.
En conclusión, la nanotecnología es una nueva vía técnica que va a contribuir al desarrollo de la «nueva» Nefrología. El futuro pasará por la integración de los nanodiagnósticos, nanoterapias, las «ómicas» y la explotación adecuada de los ingentes datos que generarán estas técnicas.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses en relación con el texto.
Miguel Valcárcel desea hacer constar su agradecimiento a la Sociedad Andaluza de Nefrología (SAN) y a la Sociedad Española de Nefrología (SEN) por la confianza depositada en un químico y nanotecnólogo para impartir charlas sobre la temática de este artículo durante 2017 en Córdoba (abril) y Burgos (octubre), respectivamente.