Los pacientes con insuficiencia renal son un grupo de alto riesgo nutricional. En los pacientes con insuficiencia renal aguda (IRA) el aporte energético debe ser de 30-40 kcal/kg de peso corporal, con un aporte proteico de 0,8-1 g/kg de peso ideal, que aumenta al normalizarse el filtrado glomerular. Con respecto al potasio es preciso limitar la ingesta 30-50 mEq/ día y de sodio a 20-40 mEq/ día en fase oligúrica, reemplazando las pérdidas en la fase diurética. Con respecto a los pacientes con insuficiencia renal crónica (IRC), se debe recomendar una dieta controlada en proteínas (0,75-1 g/kg/día) en estos pacientes. Las dietas bajas en proteínas (<0,6 g/kg/día) no están justificadas ya que la mejoría en el filtrado glomerular es mínima y la repercusión sobre la situación nutricional lo desaconseja (evidencia A). En los pacientes en hemodiálisis los requerimientos calóricos son de 35 Kcal/kg/día en situación basal. El objetivo proteico es alcanzar un aporte de 1,2-1,4 g/Kg día de proteínas. La necesidad de agua depende de la diuresis residual, a lo que se puede añadir 500-800 mL al día. El aporte de sodio debe limitarse a 60-100 meq al día, debiendo reducirse al mínimo el aporte de agua y sodio en pacientes anúricos. El aporte de potasio no suele sobrepasar 1 meq/kg/día. Los pacientes en diálisis peritoneal tienen una serie de peculiaridades en cuanto a los requerimientos. El aporte de proteínas es mayor, aproximadamente de 1,5 g/Kg/día. Las calorías procedentes de los hidratos de carbono, que son aproximadamente el 60% del total deben incluir la glucosa que aporta el líquido dializador. Otra diferencia fundamental es la mayor liberalización de la dieta de estos pacientes, al realizarse diálisis diaria. La ingesta de potasio se puede aumentar a 2000-3000 mg/día. Las perdidas de vitaminas hidrosolubles son menos llamativas
Patients with kidney failure are a high nutritional risk group. Patients with acute kidney failure need and energy intake of 30-40 kcal/kg and a protein intake of 0,8-1 g/kg of ideal weight, that it is increased with glomerular filtration improvement. Potassium must be limitated to 30-50 mEq/day and sodium to 20-40 mEq/day in oliguric phase, and must be replaced the losses in diuretic phase. Specific recommendations have been designed to some nutrients. A diet with 0.75-1 g/kg/day of proteins must be recommended in patients with chronic kidney failure (CDF). Low protein diets (<0.6 g/kg/day) are not justified, due to a possible malnutrition might be developed (A). In patients with haemodialysis, energy requirements are 35 Kcal/kg/day. Protein recommendations are 1.2-1.4 g/Kg/day. Water recommendations depend of residual diuresis. 500-800 ml must be added to residual diuresis. Sodium must limitated to 60-100 meq/day, with a depth reduction of water and sodium in anuric patients. Potassium must be under 1 meq/kg/day. Patients with peritoneal dialysis had different dietary recommendations. Protein recommendations are higher than previous (1.5 g/Kg/day). Energy recommendations from carbohydrates must be included glucose of dialyser liquid (60% of total amount). Diet has low restrictions due to the daily sessions of peritoneal dialysis, for example potassium intakes can reach 2000-3000 mg/day. Hidrosoluble vitamin losses are lower than patients with haemodialysis.
INTRODUCCIÓN
La función renal juega un papel en la regulación del equilibrio ácido-base, balance hidroeléctrico, metabolismo fosfocálcico y balance nitrogenado. Por ello, la insuficiencia renal aguda (IRA) o crónica (IRC) afectan de una manera especial la situación metabólica nutricional de los pacientes1,2.
Los pacientes con IRC presentan una alta prevalencia de malnutrición calórico-proteica, con alteración del compartimiento graso y proteico, así como una profunda alteración de las proteínas séricas. Diferentes estudios han demostrado la relación entre el mantenimiento de un buen estado nutricional con una menor morbilidad en estos pacientes3-4, recomendándose, aún existiendo una buena situación nutricional, monitorizarlos cada 6 meses si su edad es inferior a 50 años y cada 3 meses en mayores de 50 años. Desde hace décadas se han utilizado dietas restrictivas en proteínas para aliviar los síntomas urémicos, que además han probado su capacidad de disminuir la progresión de la pérdida de la función renal. El desarrollo de la hemodiálisis y la diálisis peritoneal ha supuesto un aumento en la supervivencia de estos pacientes con una clara mejoría de la calidad de vida, estos avances hacen que los requerimientos nutricionales sean específicos en función del tratamiento recibido5.
Revisaremos sucesivamente los problemas nutricionales de los pacientes con IRA o IRC así como las herramientas utilizadas en su valoración, así como las recomendaciones dietéticas de soporte nutricional avanzado que existen en la literatura.
DESNUTRICIÓN y VALORACIÓN NUTRICIONAL EN LA INSUFICIENCIA RENAL
En la IRA se presenta un estado hipercatabólico que produce un aumento en el consumo de glucosa. Si no existe un aporte dietético adecuado, una vez agotados los depósitos de glucógeno hepático, comienza una fase de neoglucogénesis3,6. La obtención de las nuevas moléculas de glucosa a partir de las proteínas viscerales y del músculo esquelético, produce una situación metabólica desfavorable. Por otra parte, la proteólisis produce una acidosis metabólica, que a su vez favorece el catabolismo proteico, dando lugar a una pérdida cada vez mayor de masa muscular y al empeoramiento del estado nutricional del paciente. Además, el acúmulo en sangre de productos nitrogenados genera anorexia y náuseas, manteniendo la situación de catabolismo al no permitir una ingesta adecuada. En resumen es importante mantener un aporte energético adecuado, con un buen aporte de hidratos de carbono para mantener el balance nitrogenado.
En el caso de los pacientes con insuficiencia renal crónica, la malnutrición calórico-proteica7 se produce por el propio fracaso de la función renal, al producirse un aumento de factores neuroendocrinos y de citoquinas. Esta alteración hormonal produce hipertrigliceridemia y una alteración del metabolismo hidrocarbonado, con resistencia a la insulina que puede finalizar en un cuadro de diabetes. El aumento de productos nitrogenados y las alteraciones iónicas produce trastornos gastrointestinales que reducen la ingesta, con náuseas y vómitos. Por otra parte, los tratamientos que reciben estos pacientes también repercuten sobre la situación nutricional. Una de las recomendaciones dietéticas más extendidas es la restricción proteica en la dieta, la cual reduce la progresión de la nefropatía5. No obstante, esta modificación dietética puede inducir en los pacientes urémicos una disminución de su ingesta calórica por una escasa adhesión a los cambios en los hábitos alimenticios8. La diálisis también puede condicionar la situación nutricional, no debemos olvidar que los pacientes tratados con hemodiálisis tienen un consumo proteico mayor que en la diálisis peritoneal, además existe mayor riesgo de déficit de vitaminas hidrosolubles y de hierro.
Para poder alcanzar una buena ingesta calórica proteica y mantener un adecuado estado nutricional, es por tanto necesario tener unas buenas herramientas su valoración. Clásicamente se han utilizado diferentes parámetros para valorar el estado nutricional de estos pacientes9 y protocolos para evaluar las diferentes herramientas utilizadas10, llegándose a la conclusión de que las más útiles son aquellas que integran parámetros relacionados con diferentes campos de la evaluación nutricional (parámetros subjetivos, antropométricos, bioquímicos, etc.).
Entre estos, los más importantes incluyen los datos derivados de la exploración física utilizando datos antropométricos (peso actual, peso ideal, peso habitual, peso seco, peso ajustado libre de edema, pliegues cutáneos, circunferencia del brazo).
Es importante conocer la definición precisa de los diferentes procedimientos de evaluar el peso corporal, pues lo contrario, puede inducir a error:
1. Peso actual, peso observado en ese momento.
2. Peso ideal, peso que se obtiene de tablas de referencia.
3. Peso habitual, es el peso histórico del paciente.
4. Peso seco: peso que se obtiene postdiálisis.
5. Peso ajustado libre de edema se calcula como (peso seco-(peso ideal-peso seco) x 0,25).
Otro de los parámetros antropométricos más utilizados, es el índice de masa corporal (IMC). Los resultados del estudio realizado con una cohorte de más de casi 10.000 pacientes en USA y Europa11, muestran como la mortalidad descendía significativamente en los pacientes de mayor IMC. En otro trabajo (Dialysis Outcomes and Practice Patterns Study)9 se muestra como un descenso en el IMC mayor de 3,5% se asocia a mayor mortalidad. En nuestro medio también se ha evaluado la importancia de este parámetro en el seguimiento nutricional de estos pacientes12.
Con respecto a los datos bioquímicos, la albúmina se ha utilizado como un parámetro para evaluar la situación calórico-proteica de los pacientes en diálisis13. En el trabajo previamente citado (DOPPS)9 se observa un aumento de la mortalidad de un 1,38% en aquellos pacientes con niveles de albúmina por debajo de 3,5 g/dl. La prealbúmina también se ha mostrado como un marcador predictivo, de mortalidad en pacientes al inicio del tratamiento con diálisis9.
Entre los métodos integrados de valoración nutricional, el más utilizado es el test de Valoración Subjetiva Global (VSG). Se trata de un método sencillo para evaluar y seguir la situación nutricional de los pacientes, con una serie de datos nutricionales, clínicos y antropométricos de fácil obtención y que ha demostrado su utilidad en pacientes con fracaso renal (fig. 1)11.
Podemos utilizar, también, cuestionarios para evaluar la ingesta alimentaria para detectar cuanto se desvía de las recomendaciones que analizaremos posteriormente14 o las de otras dietas, como puede ser la dieta mediterránea15,16. Es necesario repetir estos cuestionarios con cierta periodicidad y en varios días diferentes debido a la propia variabilidad de los resultados obtenidos y a que el nivel de ingesta del paciente se puede ver modificado por múltiples factores intercurrentes.
También podemos utilizar otras técnicas más sofisticadas como son la impedanciometría unifrecuencia o multifrecuencia (incluyendo análisis vectorial), absorciometría con rayos X o análisis de activación de neutrones.
NECESIDADES DIETÉTICAS EN LA INSUFICIENCIA RENAL
Las necesidades energéticas pueden ser calculadas mediante fórmulas utilizadas para la evaluación nutricional de los pacientes en general (sin insuficiencia renal) como la fórmula de Harris-Benedict17 u otras especiales18 (tabla I).
No obstante diversos autores, utilizan aproximaciones para facilitar la práctica diaria, que oscilan alrededor de las 35-40 calorías por kg y día en la nefropatía crónica19. Una vez que hemos realizado el cálculo de los requerimientos energéticos, la distribución de nutrientes20 en la dieta debe ser equilibrada, con un 10-15% de proteínas, 55-70% de carbohidratos y 20- 30% de lípidos. La extendida recomendación de la restricción de proteínas a 0,6-0,8 g/kg/día solo ha demostrado ser beneficiosa en pacientes con IRC que siguen tratamiento conservador (evidencia A) ya que enlentecen la progresión de la nefropatía a su fase terminal21. Sin embargo los pacientes en tratamiento sustitutivo necesitan 1-1,2 g/kg en el caso de la hemodiálisis y de 1-1,5g/kg aquellos en tratamiento con diálisis peritoneal3,19.
Tras calcular el aporte energético y el aporte proteico de nuestro paciente es necesario tener en cuenta el aporte hídrico. Debemos realizar un cálculo del balance hídrico, teniendo mucha importancia la diuresis que conserve el paciente. Habitualmente se aproxima a una ingesta de líquido de 500-600 ml sumados al volumen de diuresis que conserve el paciente.
Las necesidades de minerales y electrolitos vienen marcadas por la situación nutricional del paciente y por el grado de insuficiencia renal. En primer lugar, en los pacientes muy desnutridos las necesidades de minerales pueden estar elevadas debido al anabolismo que presentan cuando se inicia un dieta oral adecuada y/o un procedimiento de soporte nutricional, de tal forma que un aporte excesivo y/o rápido de calorías y proteínas puede dar lugar a un síndrome de realimentación con descenso brusco de potasio, fósforo, y un cuadro severo de insuficiencia cardíaca. En segundo lugar, deberemos tener en cuenta la función renal. Por ejemplo, los pacientes en oligoanuria (diuresis < 500 ml/día) presentan una excreción escasa o nula de sodio, potasio, magnesio o fosfato, debiendo ser restringidos en la dieta. Podemos plantearnos un ajuste más fino de los minerales, midiendo la eliminación de iones y minerales en orina y el aclaramiento de creatinina, sobre todo en pacientes con diuresis conservada, en los que existe gran variabilidad en sus requerimientos. Por otra parte, teniendo en cuenta el déficit en la hidroxilación de la vitamina D en posición 1-hidroxi, es preciso aumentar el aporte de calcio, hasta alcanzar un mínimo de 1 g diario. El incremento de la ingesta de alimentos ricos en vitamina D es complicado al ser estos fuente habitual de proteínas (pescado, lácteos, etc.).
Otro aspecto importante es la acidosis metabólica que presentan los pacientes, por lo que se recomienda la administración de bicarbonato en forma de suplementos orales para mantener pH > 7,2 o un bicarbonato sérico > 17 mEq/L. Una posible medida dietética es recomendar la ingesta de aguas bicarbonatos, aunque la mayor parte de los pacientes precisan bicarbonato oral en diferentes dosis.
Las necesidades de vitaminas también dependen del tratamiento que reciben los pacientes20. Por ejemplo, en los pacientes que siguen recomendaciones dietéticas restrictivas, como medida conservadora de su tratamiento, deben recibir suplementos de vitaminas hidrosolubles y vitamina D activa en forma de 1,25 dihidroxivitamina D. Sin embargo en los pacientes que están en diálisis (peritoneal o hemodiálisis) se recomienda suplementar con vitamina A, D y B12 ya que son fácilmente eliminables en las sesiones de diálisis al estar unidas a proteínas. Por otra parte existen niveles disminuidos del grupo de vitaminas hidrosolubles; vitamina C, ácido fólico y B1, no obstante sólo se ha evidenciado la necesidad de suplementar las dos primeras.
Uno de los minerales que requiere especial atención es el hierro21. Las necesidades de la población general son de 10-15 mg/día, ante un paciente con insuficiencia renal y ferritina < 100 mg/dl se recomienda la suplementación con al menos 60 mg al día de sulfato ferroso. Pudiendo recomendar su ingesta con un zumo de cítrico que favorece la absorción del hierro junto a la vitamina C.
ASPECTOS NUTRICIONALES ESPECIALES EN LA IRA
La IRA produce una gran variedad de alteraciones en el metabolismo intermediario, siendo la situación más grave de ellas, la presencia de un hipercatabolismo severo22,23. Como objetivo nutricional primario en estos pacientes, nos proponemos: acelerar la recuperación de la función renal y preservar la masa magra.
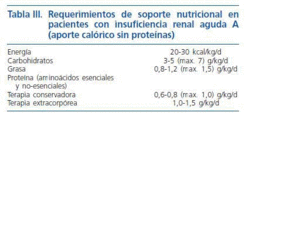
Con respecto al aporte energético (tabla II), los aportes son de 30-40 kcal/kg de peso corporal, con un aporte proteico de 0,8-1 g/kg de peso ideal, que aumenta al normalizarse el filtrado glomerular. Con respecto al potasio es preciso limitar la ingesta 30-50 mEq/ día y de sodio a 20-40 mEq/ día en fase oligúrica, reemplazando las pérdidas en la fase diurética. Para poder llevar a cabo estas recomendaciones de electrolitos podemos calibrar dietas con menús fijos o habitualmente se utilizan tablas para que limiten su ingesta. Por otra parte es necesario recordar que las técnicas de cocción de verduras y legumbres con eliminación del agua de cocción y de aclarado pueden disminuir hasta en un 40% el contenido de potasio de estas, no obstante se produce también una pérdida considerable de vitaminas hidrosolubles. Con respecto al aporte de líquidos se debe reponer el gasto diario más 500 ml.
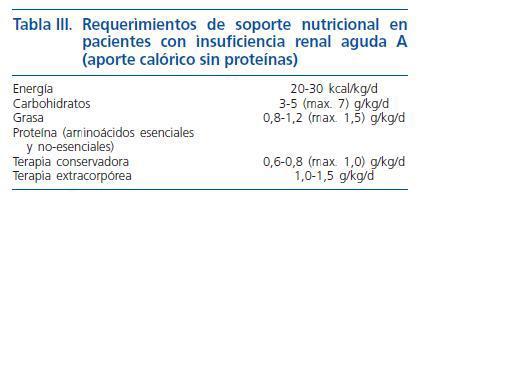
Sin embargo muchos de los pacientes por su situación clínica son incapaces de alcanzar los requerimientos nutricionales arriba señalados, siendo necesario la utilización de soporte nutricional avanzado. Recientemente la Sociedad Europea de Nutrición Enteral y Parenteral (ESPEN)24 ha realizado una guía donde se recogen todos los requerimientos de los pacientes con IRA. Los aportes energéticos no proteicos oscilan entre 20-30 kcal/kg/día, administrando 3-5 g por kg y día de hidratos de carbono y 0,8-1,2 g por kg y día de grasas. El aporte proteico puede oscilar desde 0,6 g por kg y día en pacientes en tratamiento conservador hasta un total de 1,5 g por kg y día en pacientes con tratamiento extracorpóreo.
A pesar de estas recomendaciones, diversos trabajos han mostrado23,25-26 la dificultad de alcanzar una adecuada ingesta proteica con las fórmulas artificiales disponibles en el mercado, siendo más llamativo este problema en el subgrupo de pacientes que requieren diálisis. Como medida alternativa se puede suplementar el aporte nutricional con aminoácidos vía parenteral27, recomendando el aporte de soluciones de aminoácidos estándar para mantener un balance neutro. Se ha demostrado que los aminoácidos no esenciales28 juegan un papel fundamental en determinadas situaciones de estrés en los pacientes con IRA. Sólo en aquellos casos en los que se pretenda evitar la diálisis estaría indicado el uso de soluciones a base de aminoácidos esenciales como única fuente, a dosis de 0,3-0,5 g/kg, y siempre con una duración inferior a tres semanas. Finalmente la Guía de la ESPEN lanza una serie de recomendaciones para este tipo de pacientes:
1. Los requerimientos de macronutrientes no están tan determinados por la IRA como por la severidad de la patología que lo desencadena, el tipo e intensidad de tratamiento extracorpóreo para remplazar la función renal, así como el estado nutricional y las complicaciones asociadas. Evidencia C.
2. Los tratamientos extracorpóreos inducen pérdidas de micronutrientes que requieren ser suplementadas. Evidencia C.
3. Es necesario monitorizar el nivel de micronutrientes para evitar que la suplementación produzca niveles tóxicos. Evidencia C.
4. En Unidades de Cuidados Intensivos, en los pacientes con IRA; los electrolitos que contiene una fórmula enteral que aporta 1.500-2.000 calorías, son generalmente adecuados. No obstante los requerimientos pueden diferir de manera individual, siendo necesaria su monitorización. Se debe tener especial atención en evitar una hipocaliemia y/o hipofosforemia tras iniciar la nutrición enteral (síndrome de realimentación). Evidencia C.
5. En pacientes con IRAy no complicados, deberemos utilizar la nutrición enteral si no se alcanzan los requerimientos con suplementos orales (batidos). Evidencia C.
6. En pacientes con IRA y en unidades de críticos, la nutrición enteral debe ser iniciada de manera precoz (menos de 24 horas). Evidencia C.
7. En pacientes con IRA no complicada, cuando la alimentación oral espontánea es insuficiente deberemos utilizar suplementos orales (batidos) Evidencia C.
8. La sonda nasogástrica debe ser la vía de acceso de elección para la nutrición enteral. El acceso yeyunal se indica en situaciones que cursan con un severo empeoramiento de la motilidad gastrointestinal.
9. En los casos en los cuales no se alcancen los requerimientos nutricionales con el soporte enteral, deberemos utilizar soporte parenteral. Evidencia C.
10. Las fórmulas enterales estándares son las de elección en la mayoría de los casos Evidencia C.
11. En situaciones con IRA y alteraciones hidroelectrolíticas, las fórmulas nutricionales especiales nefrológicas pueden ser útiles. Evidencia C.
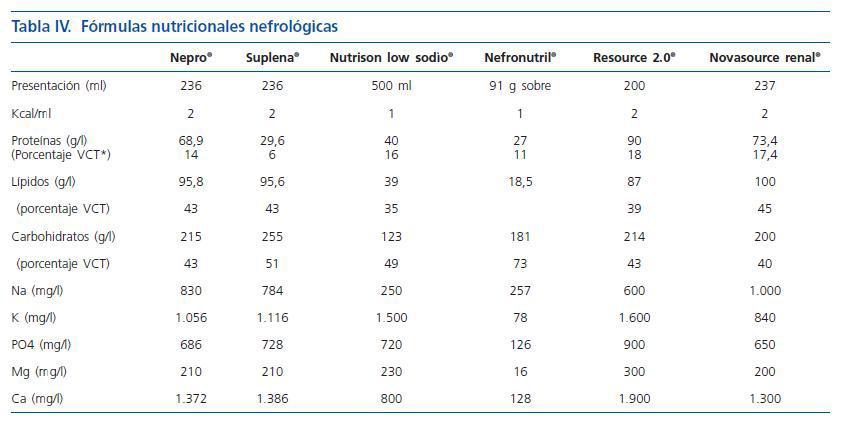
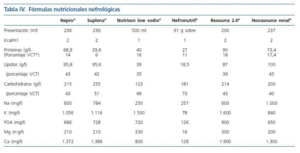
Con respecto a la última recomendación podemos mostrar en la tabla IV, que existen diversos suplementos orales nutricionales que presentan modificaciones en su composición para pacientes con insuficiencia renal aguda.
No obstante estas recomendaciones pueden ser matizadas teniendo en cuenta otra guía publicada en Nutrición Hospitalaria (Órgano Oficial de la Sociedad Española de Nutrición Enteral y Parenteral)26:
1. Los pacientes con IRA deben recibir un aporte de glucosa de 3-5 g/kg/día, es decir similar a otras situaciones clínicas. Evidencia C.
2. La infusión de grasa debe limitarse a 1 g/kg/día, suspendiendo el aporte de lípidos si se alcanzan niveles de triglicéridos por encima de 300 mg/dl. Evidencia C.
3. El aporte proteico debe adecuarse a la situación clínica y a la situación catabólica valorada por la aparición de nitrógeno uréico. La aparición del nitrógeno uréico es la suma del nitrógeno ureico urinario más el nitrógeno ureido en líquido dialítico más el cambio en el «pool» de urea orgánica. Evidencia B.
4. No deben utilizarse fórmulas de aminoácidos compuestas exclusivamente por mezcla de aminoácidos esenciales (Evidencia A).
5. El aporte de aminoácidos como tirosina, histidina, taurina y aminoácidos ramificados debería realizarse en cantidades superiores a las recomendadas para otros pacientes. Evidencia C.
6. Se recomienda el empleo de glutamina (Evidencia B).
7. El aporte proteico deber ser aumentado en pacientes con IRA sometidos a hemodiálisis (Evidencia C).
8. Es importante la valoración del aporte de vitamina A, C y D (Evidencia A). Para la vitamina C se sugiere un mínimo de 60-100 mg/día. También se recomiendan aportes mínimos de piridoxina (5-10 mg) y ácido fólico (1 mg/día).
9. La utilización de dietas estándares de nutrición enteral no plantea problemas si los pacientes están siendo tratados con técnicas de depuración (Evidencia B).
10. Las dietas enterales adaptadas a la insuficiencia renal podrían estar indicadas si los pacientes se encuentran en situación de fracaso multiorgánico y esta siendo tratado con técnicas de depuración (Evidencia C).
11. Las técnicas de depuración se podría emplear para el aporte de nutrientes Evidencia C.
ASPECTOS NUTRICIONALES ESPECIALES EN LA IRC
Ante un paciente con IRC los objetivos nutricionales son: alcanzar un estado nutricional adecuado, ayudar a controlar la azoemia y sus efectos para mejorar la calidad de vida, y retrasar la progresión de la insuficiencia renal.
Con respecto al primer punto, son diversas las series que muestran el mejor pronóstico vital que presentan estos pacientes cuando están bien nutridos19,28-31. Con respecto al retraso de la progresión en la pérdida de la función renal, también existen recomendaciones generales al respecto incluso con un Evidencia A17, donde las dietas con restricción en proteínas y fósforo en la mayoría de los estudios retrasan la caída del filtrado glomerular y la progresión a nefropatía terminal en los pacientes con insuficiencia renal en general, y en particular diabéticos tipo 1, en estos últimos de forma independiente al control glucémico16. De este modo la guía CARI (Caring for Australasians with renal impairment) recomienda32:
1. Se debe prescribir una dieta controlada en proteínas (0,75-1 g/kg/día) en todos los pacientes con IRC. Las dietas bajas en proteínas (< 0,6 g/kg/día) no están justificadas ya que la mejoría en el filtrado glomerular es mínima y la repercusión sobre la situación nutricional lo desaconseja (Evidencia A).
2. En los niños, la reducción de la ingesta de proteínas hasta los niveles mínimos recomendados por la Organización Mundial de la Salud (0,8-1,1 g/kg/día dependiendo de la edad del paciente) no ha mostrado disminuir la progresión de la insuficiencia renal crónica y por tanto no deben ser recomendadas.
Específicamente en el grupo de pacientes diabéticos, las guías de la Asociación Americana de Diabetes (ADA)33 recomiendan con una evidencia B la reducción de la ingesta de proteínas a 0,8-1 g/kg/día en pacientes con diabetes y estadios iniciales de insuficiencia renal crónica y de 0,8 g/kg/día en pacientes en los últimos estadios de insuficiencia renal crónica. El Grupo Colaborativo Cochrane34 demuestra como la reducción ligera de la ingesta de proteínas reduce levemente la progresión de la insuficiencia renal pero sin alcanzar la significación estadística. No obstante, debido a la gran variabilidad interindividual entre los pacientes, puede iniciarse un ensayo terapéutico de restricción proteica durante 6 meses en todos los pacientes, continuando el tratamiento solo en aquellos que respondan favorablemente.
Como podemos ver los interrogantes sobre la verdadera efectividad de este tipo de dietas son grandes, debido a la poca adherencia que existe por parte de los pacientes35, no obstante la utilización de la dieta como una herramienta terapéutica siempre debe ser nuestra primera opción, ya que incluso puede ser útil en el manejo de complicaciones de la IRC como la osteodistrofia36.
A pesar de las recomendaciones dietéticas, algunos pacientes con IRC precisan de soporte nutricional avanzado. Como recomendación general se considera necesario recurrir a soporte nutricional cuando se prevé un período de ayunas de 5-7 días o la ingesta oral no satisface los requerimientos para el paciente. El primer escalón es utilizar suplementos nutricionales orales (tabla III), habiendo demostrado mejorar la evolución de la enfermedad17,37. El tipo de soporte nutricional y los requerimientos, depende del tratamiento que reciba el paciente19,24. Debemos distinguir 2 posibilidades; soporte nutricional en pacientes con IRC en tratamiento conservador-prediálisis y soporte nutricional en pacientes con tratamiento dializador (hemodiálisis y/o en diálisis peritoneal).
Nutrición en paciente con IRC en tratamiento conservador
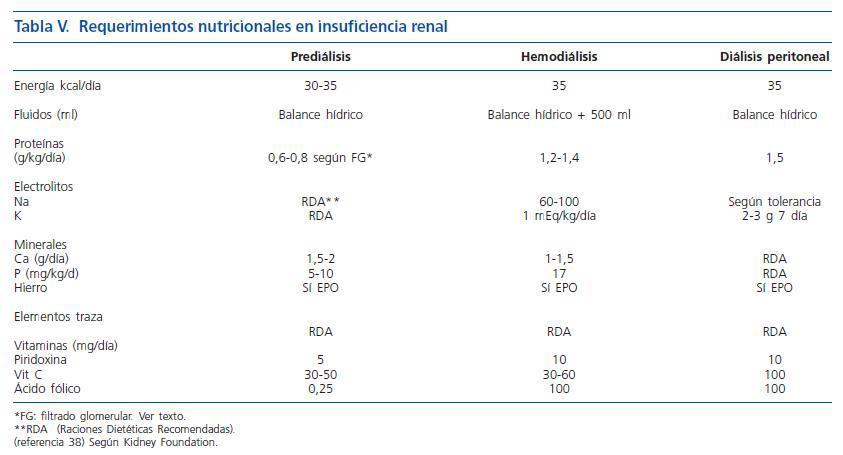
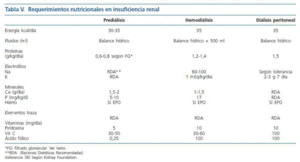
Teniendo en cuenta las recomendaciones de la National Kidney Foundation38 (tabla V), el objetivo es lograr el peso normal para el paciente, recomendándose un aporte de energético de 35 kcal/kg al día, que se ajustará según el estado nutricional del paciente. Con respecto al aporte de proteínas, esta agencia, varía sus objetivos en función de la fase de nefropatía:
a) Función renal superior a 50% (creatinina plasmática inferior a 2 mg/dl o filtrado glomerular > 70 ml/min), se aconseja un aporte de 0,8-1 g/kg/día de proteínas de alto valor biológico y 1 g más por g de proteinuria
b) Función renal entre 20 y 50% (creatinina plasmática de 2 a 5 mg/dl o filtrado glomerular 25-70 ml/min) la ingesta de proteínas se reducirá a 0,6 g/kg/día, cifra que se considera la mínima para un adulto sano. El 60% de la proteína debe ser de alto valor biológico.
c) Función renal inferior al 20% (creatinina plasmática superior a 8 mg/dl o filtrado glomerular < 25 ml/min) la restricción proteica alcanzará los 0,30 g/kg/día.
d) Función renal inferior (filtrado glomerular < 10 ml/ min), el paciente es subsidiario de depuración extrarrenal; sólo si esta no fuera posible se llegaría a una dieta aproteica que se suplementaría con aminoácidos esenciales o sus cetoanálogos.
Con respecto al aporte de hidratos de carbono, deben suponer la principal fuente de energía, en torno al 60% a expensas de hidratos de carbono complejos, dada la restricción de proteínas. Las grasas suponen el 30% del aporte calórico, se reparte en menos del 10% de grasas saturadas, y por encima del 10% de monoinsaturadas. La cantidad de colesterol diaria recomendada es de menos de 300 mg/día. Con respecto a los electrolitos, se debe limitar la ingesta de sodio a 1.000 mg/día, y de potasio a 40-60 mEq/día.
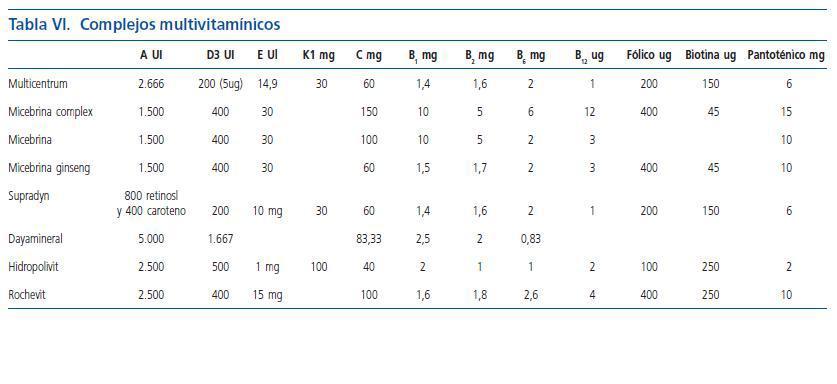
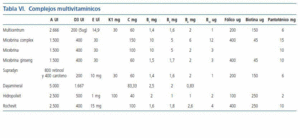
El aporte de minerales y vitaminas en estos pacientes es fundamental, los pacientes presentan un déficit en la absorción de calcio intestinal por déficit de vitamina D3, por lo que debe suplementarse aportes de calcio (1.500-2.000 mg/día). Por el contrario se debe restringir el consumo de fósforo a 5-10 mg/kg/día, limitando el consumo de lácteos, huevos, carne y algunas verduras, puesto que el aumento de fósforo contribuye al hiperparatiroidismo y al deterioro de la función renal. El hierro debe ser aportado en aquellos que reciben tratamiento con eritropoyetina. En estos pacientes se recomienda suplementar las siguientes vitaminas; vitamina B6: 5 mg/ día, vitamina D (1,25 dihidroxivitamina D): 0,25 microgramos/día, vitamina C: 30-50 mg/día. Habitualmente se utilizan complejos multivitamínicos (tabla VI).
La ESPEN también ha realizado una serie de recomendaciones en pacientes, que presentan ciertas peculiaridades:
1. La ingesta energética debe situarse entorno a las 35 kcal/día, en los pacientes con IRC estable y con un peso entorno al 10% del peso ideal (Evidencia A).
2. En los pacientes con obesidad o bajo peso se debe ajustar el aporte energético.
3. Con una evidencia B se recomienda una ingesta de proteínas de 0,55-0,6 g/kg/día (2/3 de alto valor biológico) en pacientes con aclaramiento de creatinina de 25-70 ml/min y de 0,55-0,6 g/kg/día (2/3 de alto valor biológico) o 0,28 y el resto como aminoácidos esenciales.
4. La ingesta de minerales se sitúa en 600-1.000 mg al día de fósforo, 1.500-2.000 mg/día de potasio y 1,8-2,5 g al día de sodio (Evidencia B).
5. La utilización de nutrición enteral por sonda se pauta cuando no se alcancen los requerimientos a pesar de la dieta y suplementos orales (batidos). Evidencia C. Las principales indicaciones de esta modalidad dietética la constituirían los pacientes con IRC y alguna intercurrencia aguda en la cual la ingesta oral, no es posible, aquellos en los cuales no se puede alcanzar las recomendaciones dietéticas utilizando solo la vía ora, siendo de elección en estos casos, el soporte enteral por sonda nocturno, para mantener la ingesta oral durante el día. Por ultimo, los pacientes ancianos con IRC son un grupo de riesgo nutricional elevado.
6. El tipo de fórmula recomendado es una fórmula estándar (Evidencia C).
7. En pacientes que reciban más de 5 días de nutrición enteral, podemos utilizar fórmulas especiales (tabla V) con contenidos modificados de electrolitos. (Evidencia C).
8. Los aminoácidos esenciales y los cetoanálogos, en asociación con fórmulas enterales bajas en proteínas, pueden preservar la función renal. Evidencia B.
Nutrición en paciente con IRC en tratamiento con hemodiálisis y diálisis peritoneal
Los requerimientos calóricos son de 35 kcal/kg/día en situación basal (tabla V). El objetivo proteico es alcanzar un aporte de 1,2-1,4 g/kg día de proteínas (2/3 de alto valor biológico). La necesidad de agua depende de la diuresis residual, a lo que se puede añadir 500-800 mL al día. Si no se logran cubrir las necesidades calórico-proteicas con la dieta normal puede recurrirse a suplementos nutricionales orales e incluso la nutrición parenteral durante la hemodiálisis.
La nutrición parenteral intradiálisis, consiste en administrar una nutrición parenteral, durante el tiempo que dura la sesión de diálisis, aprovechando el alto flujo de la fístula arterio-venosa, permitiendo administrar una solución hiperosmolar, minimizando de este modo la sobrecarga de volumen por la propia hemodiálisis39. El aporte que se realiza es aproximadamente de 16 kcal/kg y 0,08 g de nitrógeno por kg de peso). Apesar de sus ventajas iniciales, presenta una serie de inconvenientes:
1. La administración de una gran cantidad de nutrientes en muy poco tiempo, produce hiperglucemia e hiperlipidemia.
2. Por otra parte el aporte se realiza dos o tres veces por semana, solo durante la sesión de diálisis, de forma que debe ser considerado más como un método de suplementación nutricional, que como un soporte nutricional total.
3. Comparado con otras posibilidades de soporte nutricional, la nutrición parenteral intradiálisis tiene un coste económico alto.
Por tanto, la nutrición parenteral intradiálisis debe ser indicada cuidadosamente, limitandola a los pacientes con malnutrición grave e hipoalbuminemia40 o en situaciones muy especiales41. Los principales criterios para su administración referidos en la literatura38-41 son los siguientes.
• Cifra de creatinina sérica prediálisis < 8 mg/dl durante 3 meses
• Cifra de albúmina sérica prediálisis < 3,4 g/dl durante 3 meses
• Perdida > 10% del peso ideal
• Ingesta proteica < 0,8 g/kg/día y calórica < 25 kcal/kg
• Valoración global subjetiva grado C (malnutrición grave).
La presencia de tres criterios anteriores más la imposibilidad para aumentar la ingesta oral o fracaso de los suplementos orales o rechazo a la nutrición enteral. Como contrapartida, también existen criterios de suspensión de la nutrición parenteral intradiálisis:
• Alcanzar cifra de albúmina sérica prediálisis > 3,8 g/dl durante 3 meses.
• Alcanzar cifra de creatinina sérica prediálisis > 10 mg/dl durante 3 meses.
• Incremento del peso seco.
• Valoración subjetiva global A o B.
• Aumento de la ingesta proteica a > 1 g/kg/día y calórica a > 30 kcal/kg.
La presencia de 3 criterios anteriores más aparición de complicaciones o intolerancia a la nutrición parenteral o la no existencia de mejoría tras 6 meses de nutrición parenteral.
Con respecto a la suplementación de vitaminas y minerales se recomiendan38: vitamina C: 30-60 mg/ día, vitamina B6: 10-20 mg/día, ácido fólico: 1 mg/día y la vitamina B1 se considera opcional. El aporte de sodio debe limitarse a 60-100 meq al día, debiendo reducirse al mínimo el aporte de agua y sodio en pacientes anúricos en hemodiálisis durante los fines de semana para limitar la ganancia interdialítica de peso y prevenir la sobrecarga de volumen. Respecto al potasio, en aquellos los pacientes en acidosis o pacientes sin diuresis, no debe superar 1 meq/kg/día. Con respecto al hierro se debe aportar si recibe eritropoyetina, calcio 1-1,5 g/día.
Las recomendaciones de la ESPEN para este tipo de pacientes24 son similares a las anteriores:
1. En pacientes con patología aguda en un programa de hemodiálisis periódica, los requerimientos nutricionales deben ser similares a los emitidos para el paciente con IRA.
2. El requerimiento de proteínas para los pacientes estables en hemodiálisis son de 1,2-1,4 g/kg/día (> 50% de alto valor biológico) y en los pacientes con diálisis peritoneal de 1,2-1,5 g/kg/día (> 50% de alto valor biológico). Con un aporte energético de 35 kcal/kg/día, teniendo en cuenta en los pacientes con diálisis peritoneal el aporte de glucosa del líquido dializador. Evidencia B.
3. El requerimiento de minerales de pacientes metabolitamente estables es fosfato 800-1.000 mg/día, potasio 2.000-2.500 mg/día, sodio 1,8-2,5 g/día y de fluidos un total de 1.000 ml/día más el volumen urinario. Las sesiones de diálisis producen pérdidas de vitaminas, sobre todo hidrosolubles, recomendándose suplementos; ácido fólico 1 mg/día, piridoxina 10-20 mg/día, vitamina C (30-60 mg/día), la vitamina D se debería suplementar en función de los niveles de calcio, fósforo y hormona paratifoidea. Con respecto a la pérdida de oligoelementos con la hemodiálisis esta es mínima, no obstante en pacientes depleccionados debemos administrar; 15 mg/día de zinc, 50-70 ug/día de selenio (Evidencia B).
4. El soporte nutricional avanzado se debe indicar en pacientes en hemodiálisis desnutridos, definiendo esta desnutrición como un índice de masa corporal < 20 kg/m2, pérdida de peso superior al 10% en 6 meses, albúmina sérica por debajo de 3,5 g/l y prealbúmina menos de 300 mg/l. Evidencia C. Deben ser considerados de especial elección:
a) Pacientes en hemodiálisis con patologías intercurrentes agudas que cursan con catabolismo y el aporte nutricional adecuado no es posible.
b) Pacientes en Hemodiálisis estables que no alcanzan los requerimientos orales recomendados.
c) Pacientes en hemodiálisis inconscientes, por ejemplo con patología neurológica, en residencias.
5. La primera medida de soporte nutricional son los suplementos orales. Evidencia A.
6. Si la dieta y los suplementos orales no son útiles, se debe utilizar el soporte por sonda. Evidencia C.
7. En los pacientes con gastroparesia y que no responden a procinéticos, se debe utilizar de elección una sonda nasoyeyunal. Evidencia C.
8. En pacientes que recibirán durante mucho tiempo el soporte nutricional, debemos utilizar una gastrostomía endoscópica o una yeyunostomía endoscópica. Evidencia C.
9. Para el soporte nutricional mediante suplementos orales se recomiendan fórmulas estándares, si embargo para los pacientes con nutrición por sonda nasogástrica se recomiendan fórmulas específicas (teniendo en cuenta el aporte de fósforo y de potasio). Evidencia C.
Los pacientes con diálisis peritoneal tienen una serie de peculiaridades en cuanto a los requerimientos24,38. El aporte de proteínas es mayor, aproximadamente de 1,5 g/kg/día. Las calorías procedentes de los hidratos de carbono, que son aproximadamente el 60% del total deben incluir la glucosa que aporta el líquido dializador. Existen trabajos que han evaluado el efecto de la utilización de soluciones de diálisis peritoneal basadas en aminoácidos. Los resultados no han conseguido demostrar una mejoría significativa en los niveles de proteínas séricas, aunque existe una tendencia a la mejoría42. No se observan diferencias en la incidencia de peritonitis, la estancia hospitalaria y la mortalidad. Otra diferencia fundamental es la mayor liberalización de la dieta de estos pacientes, al realizarse diálisis diaria. Por ejemplo, la ingesta de potasio se puede aumentar a 2.000-3.000 mg/día. Las pérdidas de vitaminas hidrosolubles son menos llamativas. Se recomienda un aporte de vitamina B6 de 10 mg/día y de vitamina C de 100 mg/día. En caso de recibir tratamiento con eritropoyetina, como en los demás casos, aportar suplementos de hierro.
Tabla 1.
Tabla 2.
Tabla 3.
Tabla 4.
Tabla 5.
Tabla 6.
Figura 1. Test de valoración subjetiva global.