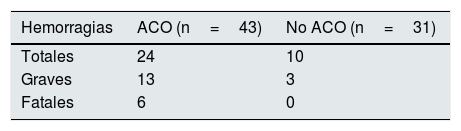La evidencia de la eficacia y seguridad de la anticoagulación oral con dicumarínicos en pacientes en hemodiálisis con fibrilación auricular (FA) es controvertida. El objetivo de nuestro estudio es evaluar las implicaciones a nivel pronóstico a largo plazo de la anticoagulación con dicumarínicos en una cohorte de pacientes con FA no valvular en programa de hemodiálisis debido a insuficiencia renal terminal.
MétodosEstudio observacional retrospectivo con inclusión consecutiva de 74 pacientes en hemodiálisis con FA. El periodo de inclusión fue de enero de 2005 a octubre de 2016. Las variables principales fueron mortalidad por todas las causas, reingresos no programados y sangrados.
ResultadosLa edad media fue de 75±10años; el 66,2% fueron hombres y 43 pacientes (58,1%) recibieron acenocumarol. Durante una mediana de seguimiento de 2,40años (IQR=0,88-4,15), el acenocumarol no demostró beneficio en supervivencia [HR=0,76, IC 95% (0,35-1,66), p=0,494]. Sin embargo, los pacientes anticoagulados presentaron más riesgo de hospitalizaciones cardiovasculares recurrentes [IRR=3,94, IC 95% (1,06-14,69), p=0,041]. Hubo una tendencia a un aumento de hospitalizaciones repetidas de causa isquémica en los pacientes anticoagulados [IRR=5,80, IC 95% (0,86-39,0), p=0,071]. Se observó una tendencia estadística hacia un mayor riesgo de sangrados totales recurrentes en los anticoagulados [IRR=4,43, IC 95% (0,94-20,81), p=0,059].
ConclusionesEn el presente estudio, la anticoagulación oral con acenocumarol en pacientes en hemodiálisis con FA no supuso un aumento de la supervivencia, y sin embargo, se asoció con un mayor riesgo de hospitalizaciones de causa cardiovascular y una tendencia a mayor riesgo de sangrados totales.
Evidence for the efficacy and safety of oral anticoagulation with dicumarines in patients with atrial fibrillation (AF) on hemodialysis is controversial. The aim of our study is to evaluate the long-term prognostic implications of anticoagulation with dicumarines in a cohort of patients with non-valvular AF on a hemodialysis program due to end-stage renal disease.
MethodsRetrospective, observational study with consecutive inclusion of 74 patients with AF on hemodialysis. The inclusion period was from January 2005 to October 2016. The primary variables were all-cause mortality, non-scheduled readmissions and bleeding during follow-up.
ResultsMean age was 75±10 years; 66.2% were men and 43 patients (58.1%) received acenocoumarol. During a median follow-up of 2.40 years (IQR=0.88-4.15), acenocoumarol showed no survival benefit [HR=0.76, 95% CI (0.35-1.66), p=0.494]. However, anticoagulated patients were at increased risk of recurrent cardiovascular hospitalizations [IRR=3.94, 95% CI (1.06-14.69), p=0.041]. There was a trend towards an increase in repeated hospitalizations of ischemic cause in anticoagulated patients [IRR=5.80, 95% CI (0.86-39.0), p=0.071]. There was a statistical trend towards a higher risk of recurrent total bleeding in patients treated with acenocoumarol [IRR=4.43, 95% CI (0.94-20.81), p=0.059].
ConclusionsIn this study, oral anticoagulation with acenocoumarol in patients with AF on hemodialysis did not increase survival. However, it was associated with an increased risk of hospitalizations of cardiovascular causes and a tendency to an increased risk of total bleeding.
Los pacientes en hemodiálisis presentan mayor prevalencia de fibrilación auricular (FA) que la población general1. El score CHA2DS2-VASc ha sido ampliamente validado para decidir la necesidad de anticoagulación en FA no valvular en la población general para prevenir eventos tromboembólicos2. Debido a la prevalencia de insuficiencia cardíaca, hipertensión y diabetes mellitus, la mayoría de los pacientes en hemodiálisis con FA requerirían anticoagulación oral aplicando la escala CHA2DS2-VASc. La evidencia de la eficacia y seguridad de la anticoagulación oral con dicumarínicos en pacientes en hemodiálisis con FA es controvertida3-5.
En este trabajo pretendemos evaluar las implicaciones a nivel pronóstico a largo plazo de la anticoagulación con fármacos antivitamina K en una cohorte de pacientes con FA no valvular en programa de hemodiálisis debido a insuficiencia renal terminal.
MétodosTipo y población de estudioSe trata de un estudio observacional retrospectivo, en el que se han incluido de forma consecutiva a todos los pacientes en programa de hemodiálisis con FA en nuestro centro. Los pacientes con prótesis mecánicas y estenosis mitral significativa fueron excluidos.
El periodo de inclusión fue el comprendido entre enero de 2005 y octubre de 2016. Se incluyeron un total de 74 pacientes en hemodiálisis con FA. La decisión de administrar anticoagulación oral en esta población se basó en el criterio médico del nefrólogo y/o cardiólogo responsable de cada paciente. El fármaco anticoagulante administrado fue acenocumarol en todos los casos.
Fuentes de informaciónLa información clínica se obtuvo mediante revisión de las bases de datos de las historias clínicas electrónicas de las unidades de Nefrología y Cardiología de nuestro hospital; ambas son bases donde se encuentran registrados todos los datos derivados de la asistencia ambulatoria y hospitalaria de nuestros pacientes. Se extrajo información adicional del programa de Alta Hospitalaria, proporcionado por la Conselleria de Sanitat y donde fundamentalmente consultamos datos de episodios asistenciales en Urgencias y hospitalizaciones en otras unidades. Se registraron los international nomalized ratios (INR) y los tiempos en rango terapéutico (TRT) de los pacientes anticoagulados durante el periodo de seguimiento, analizando la base de datos electrónica del Servicio de Hematología.
Objetivos y definicionesLos objetivos primarios fueron: mortalidad por todas las causas, reingresos no programados (por todas las causas y por causas específicas) y sangrados durante el seguimiento.
Definimos hospitalizaciones de causa cardiovascular como aquellas debidas a síndrome coronario agudo, insuficiencia cardíaca, ictus, sangrado e isquemia periférica. Se consideraron hospitalizaciones por causa isquémica las secundarias a isquemia cardíaca, cerebral o periférica. Se definió ictus isquémico como un déficit neurológico de inicio reciente que persistiera 24h y fuera confirmado por técnicas de imagen como tomografía computarizada o resonancia magnética. Se consideraron hemorragias mayores a las hemorragias fatales (con desenlace mortal) y a las que precisaron trasfusión y/u hospitalización. El seguimiento fue censurado en caso de muerte o interrupción de tratamiento anticoagulante durante la evolución (n=8).
Análisis estadísticoLas variables continuas se presentan como media±desviación estándar o mediana [rango intercuartílico (IQR)]. Las variables discretas se muestran como porcentajes. Para minimizar los potenciales sesgos de confusión creamos un índice de propensión (PS). Aquellas variables asociadas con la probabilidad de recibir anticoagulación con acenocumarol (p<0,25 en análisis univariante) fueron incluidas en un modelo de regresión logística, creándose un modelo simplificado final mediante un algoritmo de selección de covariables «hacia atrás». El modelo final incluyó un conjunto de 12 covariables: sexo, FA/flutter paroxístico (sí/no), cardiopatía isquémica (sí/no), enfermedad pulmonar obstructiva crónica (sí/no), arteriopatía periférica (sí/no), ictus previo (sí/no), enfermedad valvular (sí/no), función ventricular izquierda (%), tratamiento con antiagregantes, tratamiento con digoxina, tratamiento con antiarrítmicos, tratamiento con inhibidores de la enzima convertidora de angiotensina o antagonistas del receptor de angiotensina. El área bajo la característica operativa del receptor (ROC) mostró una excelente capacidad discriminativa (0,936) para predecir la probabilidad de recibir anticoagulación. Los scores CHA2DS2-VASc y HASBLED no se asociaron de forma independiente con la probabilidad de recibir acenocumarol.
Para explorar el efecto pronóstico de acenocumarol en nuestra población de estudio, realizamos un modelo multivariante de regresión de Cox y una regresión binomial negativa (NBreg) incluyendo como covariables los cuartiles del PS y el score CHA2DS2-VASc para muerte y hospitalizaciones recurrentes, respectivamente.
Para los eventos hemorrágicos recurrentes se utilizó una regresión binomial negativa y las estimaciones de riesgo se ajustaron por cuartiles del PS y HASBLED score. Las estimaciones de riesgo se muestran como hazard ratios (HR) para muerte e incidence rate ratios (IRR) para eventos recurrentes. Todos los análisis fueron realizados con Stata 14.1.
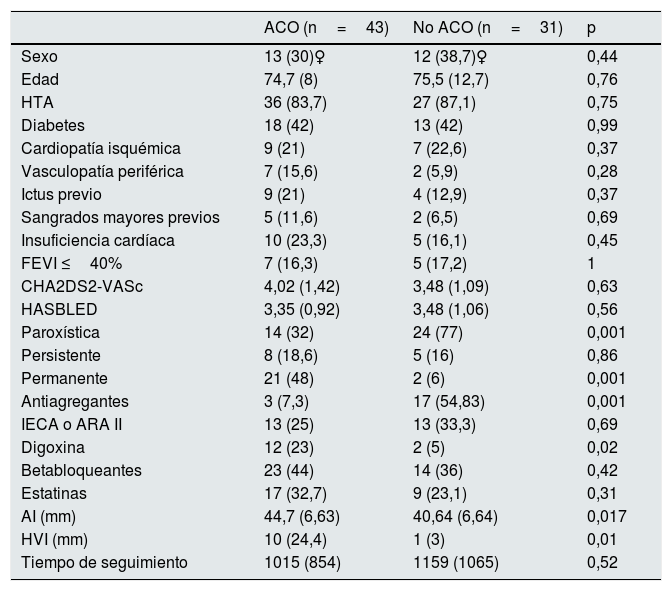
ResultadosLa edad media fue de 75±10años; el 66,2% fueron hombres y 43 pacientes (58,1%) recibieron acenocumarol. La mediana (IQR) estimada de tasa de filtración glomerular, CHA2DS2-VASc y HASBLED fue de 7,3 (5,4-10,2)ml/min/1,73m2, 4 (3-5), 3 (3-4), respectivamente. La tabla 1 muestra las características basales de la muestra.
Características basales de los pacientes con fibrilación auricular y flutter auricular no valvulares incluidos en programa de hemodiálisis anticoagulados frente a los no anticoagulados
| ACO (n=43) | No ACO (n=31) | p | |
|---|---|---|---|
| Sexo | 13 (30)♀ | 12 (38,7)♀ | 0,44 |
| Edad | 74,7 (8) | 75,5 (12,7) | 0,76 |
| HTA | 36 (83,7) | 27 (87,1) | 0,75 |
| Diabetes | 18 (42) | 13 (42) | 0,99 |
| Cardiopatía isquémica | 9 (21) | 7 (22,6) | 0,37 |
| Vasculopatía periférica | 7 (15,6) | 2 (5,9) | 0,28 |
| Ictus previo | 9 (21) | 4 (12,9) | 0,37 |
| Sangrados mayores previos | 5 (11,6) | 2 (6,5) | 0,69 |
| Insuficiencia cardíaca | 10 (23,3) | 5 (16,1) | 0,45 |
| FEVI ≤40% | 7 (16,3) | 5 (17,2) | 1 |
| CHA2DS2-VASc | 4,02 (1,42) | 3,48 (1,09) | 0,63 |
| HASBLED | 3,35 (0,92) | 3,48 (1,06) | 0,56 |
| Paroxística | 14 (32) | 24 (77) | 0,001 |
| Persistente | 8 (18,6) | 5 (16) | 0,86 |
| Permanente | 21 (48) | 2 (6) | 0,001 |
| Antiagregantes | 3 (7,3) | 17 (54,83) | 0,001 |
| IECA o ARA II | 13 (25) | 13 (33,3) | 0,69 |
| Digoxina | 12 (23) | 2 (5) | 0,02 |
| Betabloqueantes | 23 (44) | 14 (36) | 0,42 |
| Estatinas | 17 (32,7) | 9 (23,1) | 0,31 |
| AI (mm) | 44,7 (6,63) | 40,64 (6,64) | 0,017 |
| HVI (mm) | 10 (24,4) | 1 (3) | 0,01 |
| Tiempo de seguimiento | 1015 (854) | 1159 (1065) | 0,52 |
Las variables continuas se expresan en media±desviación estándar. Las variables discretas se expresan en número (%).
ACO: anticoagulación oral; AI: aurícula izquierda; ARA II: antagonistas del receptor de angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; HTA: hipertensión arterial; HVI: hipertrofia ventricular izquierda; IECA: inhibidores de la enzima convertidora de angiotensina.
En los pacientes anticoagulados la FA se presentó como permanente en mayor medida (48% vs. 6%, p≤0,001), presentaban aurículas izquierdas más dilatadas (44,7±6,6mm vs. 40,7±6,6mm, p=0,017) y mayor proporción de hipertrofia ventricular izquierda significativa (≥14mm) (24% vs. 2.9%, p=0,01). Con respecto al tratamiento, el grupo de pacientes no anticoagulados llevaba tratamiento antiagregante en mayor proporción que el grupo de pacientes anticoagulados (54,8% vs. 7,3%, p=0,000). Por el contrario, el tratamiento con digoxina fue más frecuente entre los pacientes anticoagulados (23% vs. 3%, p=0,02). No se observaron otras diferencias respecto al resto de características basales. Los pacientes anticoagulados presentaron una mediana de TRT del 33,3% (IQR=15-48).
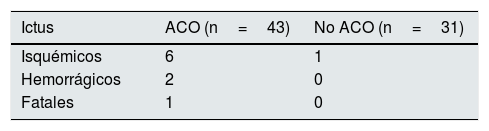
Anticoagulación y eventos clínicos adversosDurante una mediana de seguimiento de 2,40años (IQR=0,88-4,15), 51 pacientes fallecieron (68,9%), se registraron 125 hospitalizaciones por todas las causas en 53 pacientes (71,6%), 65 hospitalizaciones de causa cardiovascular en 32 pacientes (43,2%), 16 hospitalizaciones por ictus o sangrado en 14 pacientes (18,9%) y 26 hospitalizaciones de causa isquémica en 18 pacientes (24,3%). Hubo 9 ictus —2 hemorrágicos y 7 isquémicos—, todos fueron en el grupo de pacientes anticoagulados excepto uno isquémico en un paciente sin anticoagulación; tan solo uno de ellos tuvo desenlace mortal (un ictus hemorrágico en un paciente anticoagulado) (tabla 2).
Respecto a los episodios de sangrado, hubo 34 hemorragias en 24 pacientes (32,4%) y 16 sangrados mayores en 13 pacientes (17,6%). Los pacientes anticoagulados presentaron 24 sangrados, de los cuales 13 fueron graves y 6 fatales. El grupo de pacientes sin anticoagulación tuvo 10 hemorragias, de las cuales 3 fueron graves y ninguna fatal (tabla 3).
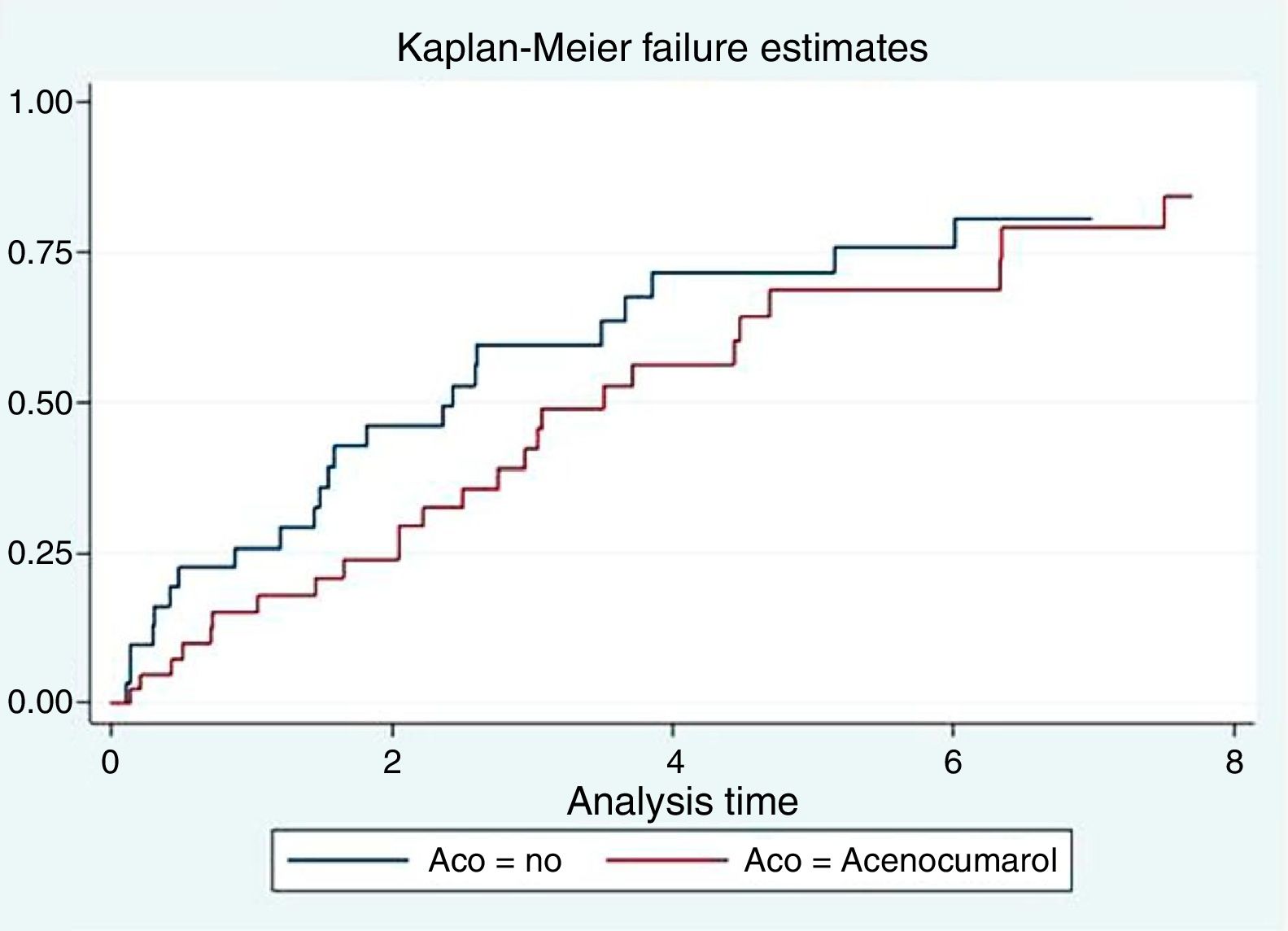
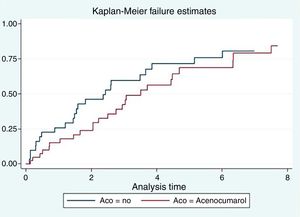
Anticoagulación y mortalidadEn el análisis univariante la anticoagulación con acenocumarol no se asoció con menor mortalidad (2,78 vs. 2,01 por 10 personas-año; p=0,304), como se representa en la curva de Kaplan-Meier (fig. 1). En el análisis multivariado ajustando por PS y CHA2DS2-VASc, la anticoagulación tuvo un efecto neutro sobre la supervivencia [HR=0,76, IC 95% (0,35-1,66), p=0,494].
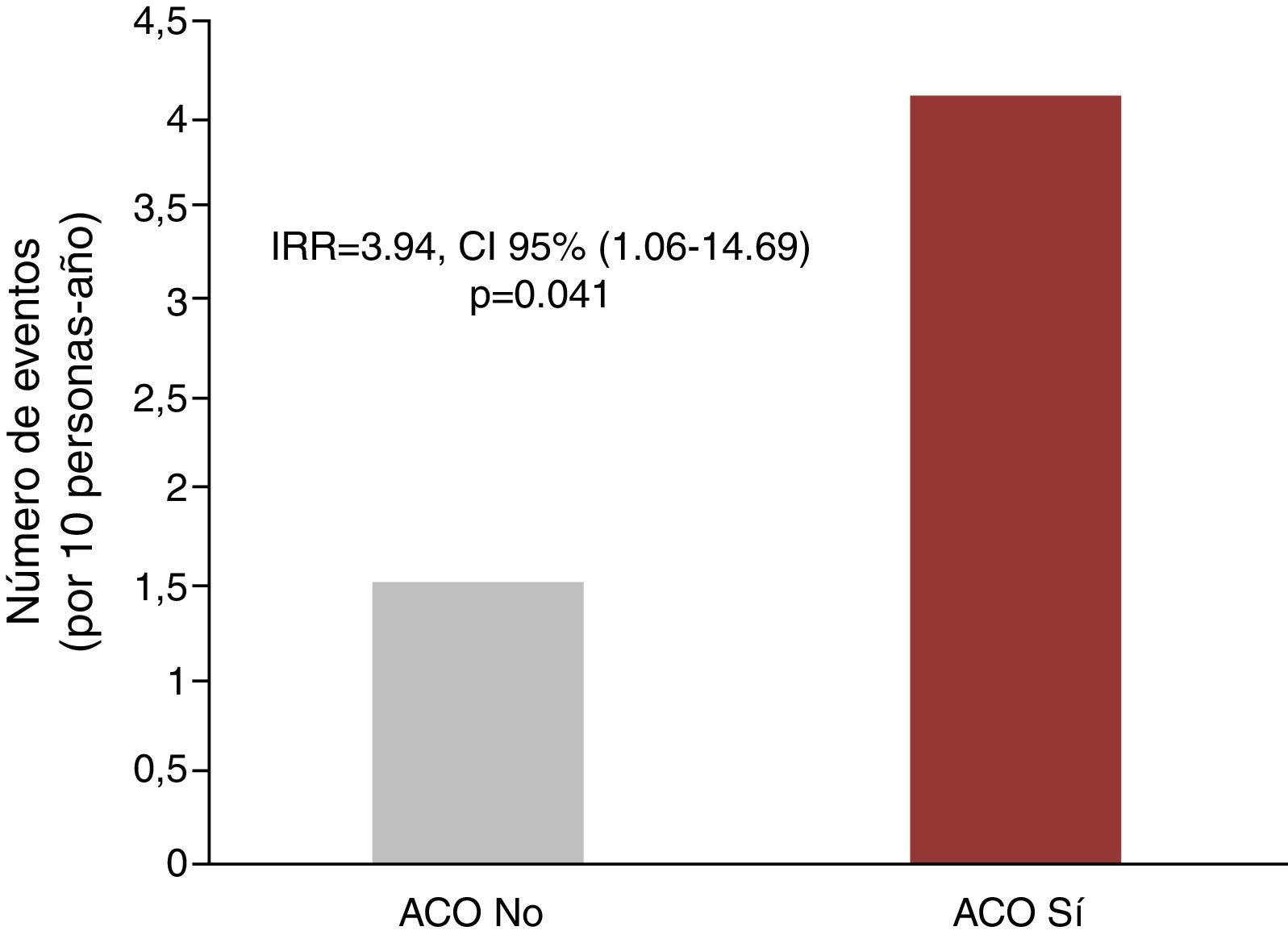
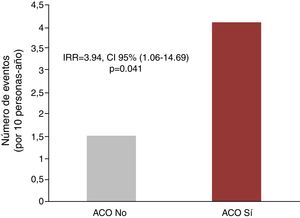
Anticoagulación y hospitalizaciones recurrentesEn el análisis univariado, la anticoagulación se asoció con mayor tasa de hospitalizaciones recurrentes por todas las causas (6,75 vs. 4,39 por 10 personas-año; p=0,022), por causa cardiovascular (4,10 vs. 1,50 por 10 personas-año; p<0,001) y hospitalizaciones de causa isquémica (1,77 vs. 0,43 por 10 personas-año; p=0,003), como se muestra en la figura 2.
En el análisis multivariante, y después de ajustar por PS y CHA2DS2-VASc score, las diferencias encontradas para hospitalización por todas las causas no alcanzaron la significación estadística [IRR=2,13, IC 95% (0,78-5,86), p=0,141]. Sin embargo, para hospitalizaciones cardiovasculares recurrentes, el exceso de riesgo atribuible a la terapia anticoagulante permaneció siendo significativo después del ajuste multivariante [IRR=3,94, IC 95% (1,06-14,69), p=0,041]. Finalmente, también se observó una tendencia a un mayor riesgo de hospitalizaciones repetidas de causa isquémica en los pacientes anticoagulados [IRR=5,80, IC 95% (0,86-39,0), p=0,071].
Anticoagulación y sangrados recurrentesSe encontró una tendencia a mayor frecuencia de hemorragias totales y hemorragias mayores en pacientes anticoagulados [1,93 vs. 1,11 (p=0,113) y 1,05 vs. 0,32 (p=0,051)]. Tras el ajuste multivariante, se observó una tendencia estadística hacia un mayor riesgo de sangrados totales recurrentes en los anticoagulados [IRR=4,43, IC 95% (0,94-20,81), p=0,059]. En cuanto a sangrados mayores, aunque las diferencias fueron ostensibles, estas no llegaron a ser estadísticamente significativas [IRR=13,38, IC 95% (0,47-382,68), p=0,129].
Tiempo en rango terapéutico (TRT) y eventos hemorrágicos en pacientes anticoaguladosNuestros pacientes anticoagulados presentaron una mediana de TRT del 33,3% (IQR=15-48).
Los pacientes anticoagulados que presentaron sangrados mayores tuvieron mayor porcentaje de controles de INR por encima del rango terapéutico que los pacientes anticoagulados sin hemorragias mayores, con una mediana del 19% (IQR=2-26%) frente al 10% (IQR=0-26%), p<0,01.
DiscusiónEl beneficio de la anticoagulación oral en pacientes con FA ha sido demostrado en estudios aleatorizados2, donde la insuficiencia renal terminal ha sido sistemáticamente un criterio de exclusión. No existe evidencia que permita extrapolar este beneficio a los pacientes en hemodiálisis6-8. Por otro lado, como es bien sabido, el riesgo de complicaciones isquémicas y hemorrágicas de estos pacientes es superior al de la población general2,4,6,9.
En nuestro estudio, que evaluó un grupo de pacientes con FA e insuficiencia renal terminal ampliamente representativos de la práctica clínica diaria, observamos que la anticoagulación oral no demostró beneficio en términos de supervivencia. Nuestros resultados concuerdan con un metaanálisis que incluyó 37.349 pacientes de estas características, donde no se observó beneficio en cuanto a mortalidad entre los pacientes anticoagulados4,10-15.
En cuanto a hospitalizaciones recurrentes, el presente estudio mostró un aumento de hospitalizaciones recurrentes de causa cardiovascular, con una tendencia a mayor riesgo de hospitalizaciones de causa isquémica. Estos hallazgos son de especial relevancia dado que en los estudios previos realizados sobre anticoagulación en pacientes con FA y en programa de hemodiálisis no se llevaron a cabo análisis de hospitalizaciones recurrentes.
Con respecto al riesgo hemorrágico, en el presente estudio encontramos un importante incremento del riesgo de sangrados recurrentes, el cual, sin embargo, no llegó a ser estadísticamente significativo probablemente por el reducido tamaño de la muestra. En concordancia con estos resultados, 4 metaanálisis recientes de estudios observacionales sugieren que warfarina no debería utilizarse de rutina en pacientes en hemodiálisis con FA dado que no supone beneficio en mortalidad ni previene ictus de forma significativa pero sí aumenta el riesgo hemorrágico de estos pacientes5,16-18.
La población de nuestro estudio presentó un alto riesgo tromboembólico determinado por la escala CHA2DS2-VASc, con una mediana de 4 (IQR=3-5), por lo que siguiendo las recomendaciones vigentes la mayoría tendrían indicación de anticoagulación oral. A día de hoy, no hay evidencia suficiente para anticoagular a estos pacientes en función de esta escala de riesgo. Por otra parte, se ha de tener en cuenta que la insuficiencia renal ha demostrado ser un factor de riesgo independiente de ictus19,20. El mecanismo de ictus en pacientes en hemodiálisis con FA no está claramente establecido. Probablemente estos pacientes presenten más riesgo de ictus aterotrombótico que embólico5. Por otro lado, hay evidencia de que la warfarina puede asociarse con un aumento de riesgo de calcifilaxia21,22 y calcificación vascular acelerada en pacientes en hemodiálisis23,24.
En cuanto al tratamiento antiagregante, aunque no ha demostrado ser eficaz para la reducción de ictus de origen cardioembólico y embolismos sistémicos25, sí es cierto que resulta eficaz para prevenir los eventos aterotrombóticos, por lo que podría haber actuado como un factor protector en la reducción de eventos isquémicos de este origen en la población de pacientes no anticoagulados, puesto que llevaban tratamiento antiagregante en mayor medida (54,8% vs. 7,3%, p=0,000).
Los pacientes anticoagulados en hemodiálisis presentan con frecuencia INR lábil (TRT por debajo del 60%), como se reporta en los escasos estudios en los que se analiza este parámetro4,13,26. En esta línea, el reciente estudio de Szummer et al.27 demuestra que el TRT es menor en los pacientes con enfermedad renal crónica, y un TRT bajo es de mal pronóstico independientemente de la función renal. De hecho, nuestros pacientes presentaron una mediana de TRT del 33,3% (IQR=15-48). Este hecho podría, de algún modo, estar en relación con los pobres resultados clínicos atribuibles a la anticoagulación con antivitamina K en estos pacientes. En el trabajo de Limdi et al.28, los autores demuestran que la disfunción renal avanzada se asocia con aumento de frecuencia de rangos supraterapéuticos de INR y mayor riesgo de sangrado; de hecho, en nuestro estudio, los pacientes anticoagulados que presentaron sangrados mayores tuvieron mayor porcentaje de controles de INR por encima del rango terapéutico que los pacientes anticoagulados sin hemorragias mayores, con una mediana del 19% (IQR=2-26%) frente al 10% (IQR=0-26%), p<0,01.
Desafortunadamente, no nos es posible hacer un análisis de aquellos que tuvieron un TRT mayor o igual al 60% frente al resto puesto que tan solo hay 2 pacientes que presentan un control óptimo, por lo que no es un número suficiente para establecer una comparación.
A pesar de las limitaciones inherentes al limitado tamaño de la muestra, y dado que en un abordaje metodológico tradicional de tiempo hasta el primer evento las recomendaciones sugieren al menos disponer de un mínimo de 10 eventos por cada covariable incluida en el modelo multivariante29, de manera alternativa decidimos emplear un ajuste mediante un PS, con lo que se pretende construir un modelo que tenga un excelente poder discriminativo, generalmente por encima de 0,85. En nuestro caso, la capacidad discriminativa del modelo fue >0,90, lo que indica un excelente poder discriminativo. El ajuste aquí realizado utilizando un PS (para así intentar minimizar los sesgos de confusión residual propios de los estudios observacionales) se ajusta a lo aceptado tradicionalmente en metodología.
Por otro lado, en un intento por aumentar la potencia del estudio y de describir mejor la historia natural de la enfermedad, decidimos explorar la relación entre la anticoagulación y los eventos repetidos (todos los eventos) durante todo el seguimiento. Con este abordaje, que en los últimos años ha empezado a ser promovido por importantes grupos de investigación30-32, registramos, por ejemplo, 125 hospitalizaciones por todas las causas y 65 hospitalizaciones de causa cardiovascular, lo que sin duda aumenta la potencia del estudio y nos ofrece estimaciones de riesgo más sólidas.
LimitacionesLas limitaciones de nuestro estudio son las inherentes a las de un trabajo observacional retrospectivo en un único centro; sin embargo, la población aquí evaluada constituye un reflejo de la práctica clínica habitual que incluye todos los pacientes con FA en hemodiálisis durante un periodo muy amplio, desde enero de 2005 hasta octubre de 2016, y con un tiempo de seguimiento prolongado [mediana de seguimiento de 2,40años (IQR=0,88-4,15)].
Además, este es un estudio pequeño con potencia limitada para detectar diferencias significativas, sobre todo en aquellos eventos con un número reducido de episodios adversos. Para minimizar los sesgos de confusión empleamos un ajuste mediante un PS. Para aumentar la potencia del estudio realizamos un análisis incluyendo todos los eventos repetidos a lo largo del seguimiento.
En el presente estudio no ha sido posible realizar un análisis de eventos en los pacientes con TRT óptimo puesto que tan solo 2 de los pacientes anticoagulados cumplían dicha condición, lo cual pone de manifiesto la dificultad para el control de la anticoagulación con dicumarínicos en estos pacientes.
ConclusionesEn el presente estudio, la anticoagulación oral con acenocumarol en pacientes en hemodiálisis con FA no supuso un aumento de la supervivencia, y sin embargo, se asoció con un mayor riesgo de hospitalizaciones de causa cardiovascular y una tendencia a mayor riesgo de sangrados totales. Son necesarios nuevos estudios, preferentemente prospectivos y en escenarios más controlados, que desvelen la utilidad de la anticoagulación en estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.