Caso clínico cerrado
Diarrea, anemia, plaquetopenia, hipertensión arterial e insuficiencia renal aguda en mujer joven.
F. Valdés Cañedo1, M. Cao Vilariño1 , F. Arrojo2 y A. Alonso Hernández1
1. Hospital Universitario de A Coruña
2. Hospital Arquitecto Marcide de Ferrol.
Paciente mujer, de 24 años de edad , de profesión militar , sin antecedentes personales de interés excepto un primer embarazo sin complicaciones finalizado con un parto normal 15 meses antes de su ingreso . Su madre, de 55 años , fue diagnosticada a los 52 de enfermedad de Churg- Strauss sin afectación renal y su abuela materna falleció en hemodiálisis crónica por enfermedad renal terminal no filiada . No fuma ni consume alcohol o drogas. Desde hace 11 meses recibe anticonceptivos orales.
Siete días antes de su ingreso, después de un ejercicio físico intenso, presentó astenia, anorexia , náuseas y , tres días más tarde , diarrea sin fiebre con cuatro deposiciones al día, líquidas y sin sangre, de 48 horas de duración. A pesar del cese de la diarrea su estado general no mejora por lo que acude a su hospital de referencia donde se le objetiva oliguria e insuficiencia renal severa , hipertensión arterial , anemia y plaquetopenia . Fue tratada con fluidoterapia IV , trasfundida con una unidad de concentrado de hematíes y remitida a nuestro servicio.
Al ingreso, la paciente estaba consciente y orientada, pálida , sin disnea y tolerando el decúbito. La tensión arterial fue de 170/110 mm de Hg ,la temperatura de 36,5ºC , la frecuencia respiratoria de 12 respiraciones por minuto y la frecuencia del pulso de 70 latidos por minuto. La exploración neurológica fue normal y el fondo de ojo no mostró alteraciones. La auscultación cardiopulmonar y la exploración abdominal fueron normales. Había edemas pretibiales ligeros. No se observaron adenopatías ni tampoco alteraciones en la piel ni en los pulsos periféricos.
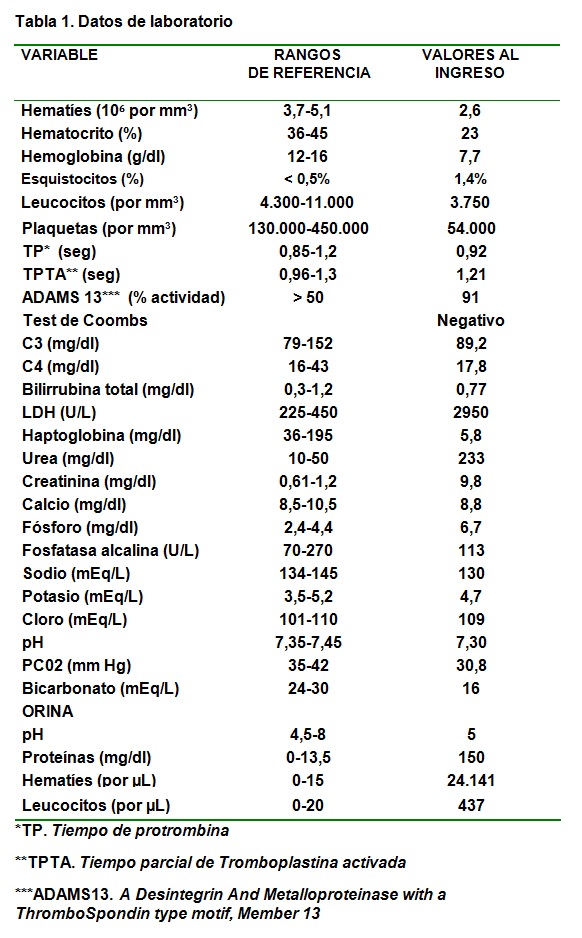
Los datos analíticos iniciales más relevantes para el caso se recogen en la Tabla 1. Posteriormente se comprobó que los ANA , ANCA y la serología para VHB, VHC y VIH eran negativos. El urocultivo fue negativo y el coprocultivo en medio enriquecido con sorbitol , tomado cinco días después del cese de la diarrea, mostró flora saprofítica normal . El electrocardiograma mostró un ritmo sinusal sin alteraciones. La ecografía renal evidenció unos riñones con ecoestructura y tamaño normales (12,3 cms el derecho y 12,5 cms el izquierdo) . El resto de estudios de imagen (RX de tórax, ecografía abdominal y TAC cerebral) fueron normales.
Fue tratada con plasmaféresis e infusión de plasma diarias ,hemodiálisis en días alternos , amlodipino (10 mg/día) , enalapril (40 mg/día) y doxazosina ( 8 mg/día). Después de siete días de tratamiento la situación de la paciente no mejoró. Mantuvo la plaquetopenia y necesitó de la administración de cinco unidades de concentrado de hematíes para controlar la anemia , continuó precisando diálisis y permaneció hipertensa. La tolerancia a la plasmaterapia no fue buena. En todas las sesiones se produjeron reacciones adversas en forma de rash cutáneo y taquipnea a pesar de la premedicación con esteroides y antihistamínicos. Finalmente, fue preciso suspender la sexta sesión por aparición de rash cutáneo y broncoespasmo con la infusión de una pequeña cantidad de plasma. Por todo ello , al séptimo día del ingreso se decidió suspender la plasmaterapia, realizar un procedimiento diagnóstico e iniciar un nuevo tratamiento.
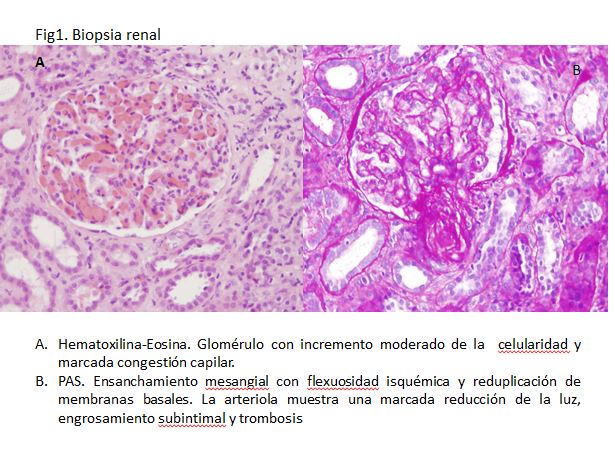
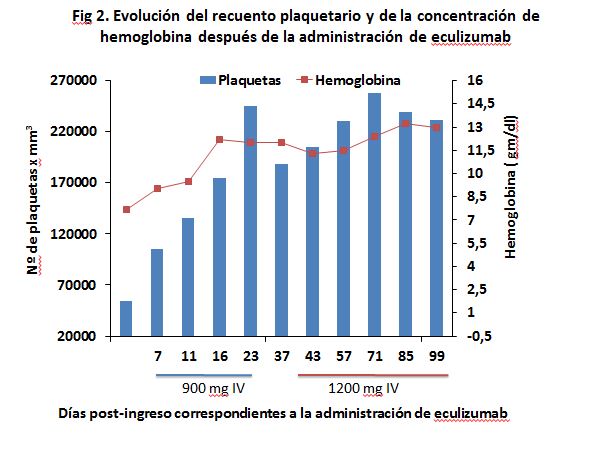
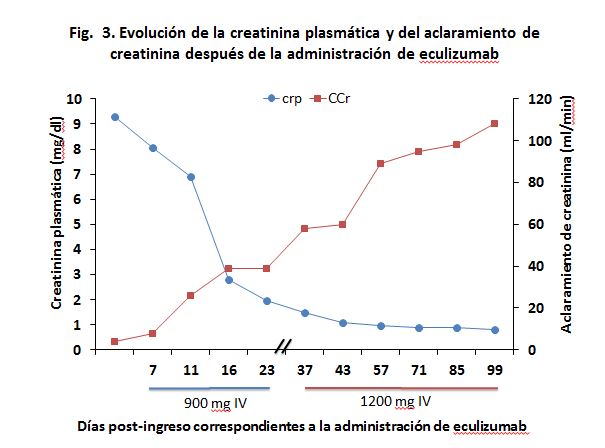
El procedimiento diagnóstico fue una biopsia renal que mostró hallazgos característicos de microangiopatía trombótica (Fig.1). El nuevo tratamiento con eculizumab 900 mg IV los días 7,11 , 16 y 23 del ingreso normalizó la LDH y la haptoglobina con la primera dosis, y las plaquetas y la hemoglobina después de la segunda (Fig.2). La tensión arterial se controló con la segunda dosis y la medicación antihipertensiva se suspendió al alta tras 24 días de ingreso. La función renal mejoró progresivamente, se pudo suspender la diálisis a partir de la segunda dosis y la creatinina plasmática y el aclaramiento de creatinina se normalizaron después de recibir otras seis dosis bisemanales de 1200 mg IV de eculizumab en régimen ambulatorio (Fig.3)
El estudio genético y funcional reveló una mutación heterocigótica en el gen de MCP (membrane cofactor proteína, CD46) con disminución del 55% de la expresión de la proteína en la superficie de los leucocitos (Tabla 2).
El diagnóstico definitivo fue de Síndrome hemolítico urémico atípico (SHUa) mediado por el complemento asociado a uso de anticonceptivos orales.
DEFINICIÓN
El SHUa mediado por el complemento se caracteriza por anemia hemolítica microangiopática (AHM) , trombocitopenia y daño renal agudo que aparecen, cuando hay un factor desencadenante, en individuos con alteraciones genéticas o adquiridas en el sistema del complemento1-4. Estos trastornos permiten la actividad incontrolada de C3 convertasa (C3bBb) de la vía alternativa del complemento en la superficie endotelial y la generación de C5a y C5-9b , que al inducir inflamación ,daño en la membrana celular y activación de la vía de la coagulación causan una microangiopatía trombótica (MAT) 5,4.
PATOGENIA
El 60% de los pacientes con SHUa son portadores de una o mas anomalías genéticas o adquiridas del complemento1, 3 6-8. Las mutaciones genéticas se traducen, o en pérdida de función de proteínas plasmáticas (CFH , CFI)9, 10 o de membrana (MCP, THMD)11, 12 ,que interactúan para disociar a C3bBb o degradar a C3b en la superficie celular , o en ganancia de función de proteínas constituyentes de C3bBb ( C3, CFB)13, 14.
Las mutaciones más frecuentes son las que ocurren en la región C terminal de CFH ( 20-30%) , las de MCP con disminución de función o de expresión de proteína (10-15%) y las de CFI, ( 4-10%) , mientras que las mutaciones de C3 (2-10%) , THBD (3-4%) y CFB (1-4%) son más raras7, 15 . Algunos pacientes con SHUa son portadores de genes híbridos entre el de CFH y los de proteínas relacionadas con el complemento (CFHR1-5)16, 17. Los anticuerpos anti CFH son más frecuente en niños (25-50%) que en adultos (5-10%)18 19 20 y pueden asociarse a delecciones homocigóticas en el gen de CFHR1, CFHR-3 y CFHR4 , aunque también se han descrito en de con mutaciones en CFH, CFI, MCP, CFB o C321 22 23.
La penetrancia , que se estima del 50% entre individuos portadores de anomalías del complemento, se incrementa si coexisten mas de una mutación , si se combinan mutaciones y autoanticuerpos o en presencia de algunos polimorfismos de un único nucleótido o de haplotipos completos de CFH y MCP6.
El complemento podría estar implicado en algunos casos de SHU por Escherichia .Coli productora de toxina shiga (STEC), porque se ha observado que la toxina puede fijarse a CFH interfiriendo con su función reguladora24. Se desconoce si el complemento puede jugar un papel en el SHUa asociado a mutaciones en diaglicerol quinasa (DGKE)25, 26. Estos pacientes presentan daño endotelial con expresión de ICAM-1 y factor tisular mediado por p36 MAPK27, pero se han encontrado casos en los que coexisten mutaciones en DGKE y en C3 o trombomodulina28 y ,recientemente, se ha descrito en una familia consanguínea una mutación en DGKE asociada a consumo de C329. Tampoco se conoce el alcance que puede tener el hallazgo de un estudio en el que la mitad de los pacientes con SHUa compartían mutaciones en el complemento y en genes del sistema de coagulación, principalmente, de plasminógeno30.
MANIFESTACIONES CLÍNICAS Y EVOLUCIÓN
El SHUa es una enfermedad muy rara. En Europa se estiman una incidencia y prevalencia de 0,11 y de 3,3 por millón de habitantes, respectivamente31. Afecta preferentemente a niños y adultos jóvenes, aunque puede manifestarse en cualquier edad, y hacerlo en forma esporádica o familiar15 7.
Suele presentarse, abruptamente, como evento único o como recidiva ,después de un episodio desencadenante como infección, embarazo o exposición a drogas y se manifiesta con AHM , trombocitopenia y daño renal agudo ,frecuentemente, con hipertensión arterial por sobrecarga de volumen o afectación vascular. Otras veces, los pacientes evolucionan con anemia y trombocitopenia con función renal conservada, o con proteinuria, hipertensión y deterioro progresivo de la función renal2, 32, 33.
Las manifestaciones extrarenales dependen del territorio vascular afectado. Son frecuentes las neurológicas que incluyen irritabilidad, confusión, trastornos motores, convulsiones y coma. También son frecuentes las náuseas, los vómitos y la diarrea, y se han descrito casos con hepatitis , pancreatitis y hemorragia intestinal2. Las manifestaciones cardíacas consisten en enfermedad coronaria con infarto , muerte súbita , cardiomiopatía dilatada y estenosis y trombosis de vasos de mediano calibre en fases tardías de la evolución34, 35 . También se han descrito casos con afectación pulmonar32 o cutánea36.
Los datos de laboratorio muestran valores de hemoglobina habitualmente inferiores a 10 gm/dl, elevación de LDH y descenso de haptoglobina en ocasiones hasta niveles indetectables . El test de Coombs será negativo , excepto en los casos de infección por neumococo , y en el examen del frotis en sangre periférica se pueden encontrar esquistocitos en cantidades superiores al 1%, aunque su ausencia no excluye el diagnóstico. La trombocitopenia, cuando se produce, es con frecuencia inferior a 150.000 plaquetas y los estudios de coagulación son normales. El daño renal se objetiva por incremento en los valores de creatinina y por descenso del GFR o por la presencia de proteinuria y hematuria microscópica . En algunos pacientes pueden encontrarse niveles bajos de C3 o C4, aunque su normalidad o la de CFH, CFI, CFB no excluyen la enfermedad.
El análisis genético y funcional del sistema del complemento permite confirmar el diagnóstico y valorar la evolución y el pronóstico . El estudio es imprescindible en los familiares candidatos a donantes vivos para trasplante.
El pronóstico de los pacientes depende del componente del complemento afectado7, 32, 37 y ha mejorado con el uso de plasmaterapia38 y ,sobre todo, de eculizumab. Previamente al uso de Eculizumab se producía insuficiencia renal terminal o muerte en el 50-70% de los casos con mutaciones en CFH, en el 60% de los que las presentaban en C3, en el 50% de los pacientes con mutaciones en CFI, CFB y trombomodulina, en 30-40% de los portadores de anticuerpos anti factor H y en menos del 10% en los pacientes con mutaciones en MCP1, 39, 40.
La recidiva en el trasplante ocurre en más de la mitad de los pacientes con alteraciones de los componentes plasmáticos y es menos frecuente (15-20%) en los pacientes con alteraciones en MCP, porque la proteína se expresa con normalidad en las células del injerto6, 41. La recidiva ensombrece el pronóstico del trasplante, ya que causa pérdida del injerto en el 92% de los casos6 . La mayor edad en la presentación de la enfermedad, un intervalo pequeño entre la entrada en diálisis y el trasplante, el uso de donantes vivos relacionados genéticamente y de anticalcineurínicos se han considerado como factores de riesgo de recidiva en el trasplante42.
DIAGNÓSTICO DIFERENCIAL
El documento de consenso elaborado por el grupo español para el estudio del SHUa ofrece una excelente estrategia para el diagnóstico diferencial de las MAT en pacientes pediátricos y adultos 31 . En los adultos es esencial confirmar la AHMA ,con o sin trombocitopenia, y evaluar el contexto clínico subyacente incluyendo la severidad y la evolución del daño renal.
Siempre hay que descartar las enfermedades autoinmunes, la hipertensión maligna, la preclampsia/ HELP, las infecciones, las neoplasias , los trasplantes de órganos sólidos o hematopoyéticos y el uso de fármacos que puedan inducir daño renal por mecanismos inmunes o por toxicidad dependiente de dosis .Para ello son imprescindibles la historia clínica exhaustiva, el examen físico completo y el uso de las pruebas diagnósticas más sensibles para descartar esos procesos.
Si el daño renal es mínimo o ausente, la púrpura trombocitopénica trombótica (PTT) es la primera opción. Cuando es severo y agudo hay que diferenciar entre PTT y SHU-STEC . Una actividad de ADAMS13 superior al 10% descarta a la PTT mientras que el SHU-STEC se excluye por la ausencia de afectación gastrointestinal y por la negatividad de los cultivos en medio de Mac Conkay para O157:H7, del serotipado específico o de las técnicas de PCR para genes de toxina shiga. La publicación de un caso de SHUa del adulto por déficit de cianocobalamina obliga a considerar este diagnóstico cuando se han descartado el resto de opciones 43.
La biopsia renal rara vez es útil para diferenciar las MAT primarias o secundarias, pero puede utilizarse en casos de evolución atípica o para valorar la indicación de tratamiento continuado con plasmaterapia o eculizumab en pacientes con evolución prolongada ,sin afectación hematológica y con deterioro severo de la función renal.
TRATAMIENTO
El tratamiento convencional consiste en medidas de soporte y en plasmaterapia (plasmaféresis/infusión de plasma) complementada con inmunosupresión en los pacientes con anticuerpos anti CFH. Las medidas de soporte incluyen las transfusiones de hematíes cuando la anemia es severa, y de plaquetas si hay riesgo de sangrado o se realiza alguna intervención, el mantenimiento del volumen intravascular y del soporte nutricional , el control de la hipertensión y el uso de diálisis en caso necesario.
La plasmaterapia aplicada, precozmente , de forma intensiva y prolongada, ha logrado disminuir la mortalidad y alcanzar tasas de remisión hematológica entre 25-88% según la anomalía presente, pero su eficacia respecto a la función renal es más limitada, porque solo la mitad de los pacientes responden con recuperación o mejoría de la función renal38 15 . Además, es ineficaz en los pacientes con alteraciones en MCP, por ser una proteína de membrana y conlleva complicaciones como la necesidad de un catéter de uso prolongado, la depleción de factores de coagulación o las reacciones anafilácticas que dificultan su uso continuado.
Para los pacientes con mutaciones en proteínas plasmáticas , como CFH, se han propuesto como soluciones definitivas el trasplante hepático, o el combinado hepático y renal para los que, además, presentan insuficiencia renal terminal. Del análisis de la veintena de casos reportados hasta la fecha, se deduce que es imprescindible el uso de plasmaterapia o eculizumab en las fases iniciales del trasplante hasta que la función hepática sea operativa y, en cualquier caso, este tipo de trasplante debe realizarse en centros con experiencia acreditada después de un cuidadoso balance individualizado de riesgos y beneficios del procedimiento y frente a la alternativa de tratamiento continuado con eculizumab44-47.
El tratamiento del SHUa ha cambiado con el uso de eculizumab , un anticuerpo IgG4/2 Kappa monoclonal humanizado con alta afinidad por C548. En adultos, a dosis de 900 mg IV semanales durante cuatro semanas y de 1200 mg IV cada dos semanas, posteriormente, bloquea la producción de C5a y de C5-C948, 49 . Fue aprobado por la FDA y la EMEA en 2011 en base la los resultados obtenidos a las 26 semanas de seguimiento en dos estudios observacionales, prospectivos y abiertos, uno con pacientes con SHUa en evolución y refractarios a plasmaterapia ,y otro con pacientes de larga evolución, con daño renal crónico y dependientes de plasmaterapia. Los resultados obtenidos con eculizumab en cuanto a abandono de plasmaterapia , normalización hematológica y mejoría de la función renal , sobre todo con su administración precoz, han sido confirmados en esos estudios a más largo plazo50, 51 , corroborados en otras series , en casos aislados , en una revisión sistemática49 52 y, muy recientemente, en un estudio prospectivo pediatrico53. La eficacia de eculizumab también ha sido demostrada en la profilaxis54-57 y en el rescate de las recidivas en el trasplante renal55, 58-60. Sin embargo, la respuesta a eculizumab puede estar limitada en pacientes portadores de mutaciones en C561.
El bloqueo de la vía terminal del complemento favorece la infección por gérmenes encapsulados. Por eso, es preceptiva la vacunación frente a Neisseria Meningitidis complementada con profilaxis antibiótica durante el efecto ventana o ininterrumpidamente mientras dure el tratamiento62 47. Por otra parte, el tratamiento continuado con eculizumab es muy costoso en términos monetarios49 y , de momento, se desconocen los criterios y el tipo de monitorización necesarios para su discontinuación individualizada. Las Sociedades Científicas y los Grupos de Expertos han elaborado excelentes guías para la optimización de su uso49 31, 47. Sin embargo, es preciso continuar investigando para conseguir una metodología sensible y validada para monitorizar la actividad del complemento63-65 y la discontinuación de eculizumab66, 67, ya que los estudios en estas áreas son escasos y los resultados no son definitivos.
BIBLIOGRAFÍA
1. Noris M, Remuzzi G. Atypical hemolytic-uremic syndrome. N Engl J Med. 2009 ;361:1676-87.
2. Loirat C, Fremeaux-Bacchi V. Atypical hemolytic uremic syndrome. Orphanet J Rare Dis. 2011;6:60.:1-30
3. S. Rodriguez de Córdoba TM. Síndrome hemolítico urémico atípico. Nefrología. 2011;2:58-65.
4. George JN, Nester CM. Syndromes of thrombotic microangiopathy. N Engl J Med.2014;371:1847-8.
5. Roumenina LT, Loirat C, Dragon-Durey MA, Halbwachs-Mecarelli L, Sautes-Fridman C, Fremeaux-Bacchi V. Alternative complement pathway assessment in patients with atypical HUS. J Immunol Methods. 2011;365:8-26.
6. Bresin E, Rurali E, Caprioli J, Sanchez-Corral P, Fremeaux-Bacchi V, Rodriguez de Cordoba S, et al. Combined complement gene mutations in atypical hemolytic uremic syndrome influence clinical phenotype. J Am Soc Nephrol. 2013 ;24:475-86.
7. Fremeaux-Bacchi V, Fakhouri F, Garnier A, Bienaime F, Dragon-Durey MA, Ngo S, et al. Genetics and outcome of atypical hemolytic uremic syndrome: a nationwide French series comparing children and adults. Clin J Am Soc Nephrol. 2013 ;8:554-62.
8. Esparza-Gordillo J, Goicoechea de Jorge E, Buil A, Carreras Berges L, Lopez-Trascasa M, Sanchez-Corral P, et al. Predisposition to atypical hemolytic uremic syndrome involves the concurrence of different susceptibility alleles in the regulators of complement activation gene cluster in 1q32. Hum Mol Genet. 2005 ;14:703-12.
9. Warwicker P, Goodship TH, Donne RL, Pirson Y, Nicholls A, Ward RM, et al. Genetic studies into inherited and sporadic hemolytic uremic syndrome. Kidney Int. 1998 ;53:836-44.
10. Fremeaux-Bacchi V, Dragon-Durey MA, Blouin J, Vigneau C, Kuypers D, Boudailliez B, et al. Complement factor I: a susceptibility gene for atypical haemolytic uraemic syndrome. J Med Genet. 2004 ;41:e84.
11. Noris M, Brioschi S, Caprioli J, Todeschini M, Bresin E, Porrati F, et al. Familial haemolytic uraemic syndrome and an MCP mutation. Lancet. 2003 ;362:1542-7.
12. Delvaeye M, Noris M, De Vriese A, Esmon CT, Esmon NL, Ferrell G, et al. Thrombomodulin mutations in atypical hemolytic-uremic syndrome. N Engl J Med. 2009 ;361:345-57.
13. Fremeaux-Bacchi V, Miller EC, Liszewski MK, Strain L, Blouin J, Brown AL, et al. Mutations in complement C3 predispose to development of atypical hemolytic uremic syndrome. Blood. 2008 ;112:4948-52.
14. Goicoechea de Jorge E, Harris CL, Esparza-Gordillo J, Carreras L, Arranz EA, Garrido CA, et al. Gain-of-function mutations in complement factor B are associated with atypical hemolytic uremic syndrome. Proc Natl Acad Sci U S A. 2007 ;104:240-5.
15. Noris M, Caprioli J, Bresin E, Mossali C, Pianetti G, Gamba S, et al. Relative role of genetic complement abnormalities in sporadic and familial aHUS and their impact on clinical phenotype. Clin J Am Soc Nephrol. 2010 ;5:1844-59.
16. Venables JP, Strain L, Routledge D, Bourn D, Powell HM, Warwicker P, et al. Atypical haemolytic uraemic syndrome associated with a hybrid complement gene. PLoS Med. 2006 ;3(10):e431.
17. Valoti E, Alberti M, Tortajada A, Garcia-Fernandez J, Gastoldi S, Besso L, et al. A novel atypical hemolytic uremic syndrome-associated hybrid CFHR1/CFH gene encoding a fusion protein that antagonizes factor H-dependent complement regulation. J Am Soc Nephrol. 2015 ;26:209-19.
18. Dragon-Durey MA, Loirat C, Cloarec S, Macher MA, Blouin J, Nivet H, et al. Anti-Factor H autoantibodies associated with atypical hemolytic uremic syndrome. J Am Soc Nephrol. 2005 ;16:555-63.
19. Dragon-Durey MA, Sethi SK, Bagga A, Blanc C, Blouin J, Ranchin B, et al. Clinical features of anti-factor H autoantibody-associated hemolytic uremic syndrome. J Am Soc Nephrol. 2010 ;21:2180-7.
20. Nozal P, Lopez-Trascasa M. M. Autoanticuerpos frente a proteínas de la vía alternativa del complemento en enfermedad renal. Nefrologia. 2016. http://dx.doi.org/10.1016/j.nefro.2016.01.014.
21. Jozsi M, Licht C, Strobel S, Zipfel SL, Richter H, Heinen S, et al. Factor H autoantibodies in atypical hemolytic uremic syndrome correlate with CFHR1/CFHR3 deficiency. Blood. 2008 ;111:1512-4.
22. Abarrategui-Garrido C, Martinez-Barricarte R, Lopez-Trascasa M, de Cordoba SR, Sanchez-Corral P. Characterization of complement factor H-related (CFHR) proteins in plasma reveals novel genetic variations of CFHR1 associated with atypical hemolytic uremic syndrome. Blood. 2009;114:4261-71.
23. Moore I, Strain L, Pappworth I, Kavanagh D, Barlow PN, Herbert AP, et al. Association of factor H autoantibodies with deletions of CFHR1, CFHR3, CFHR4, and with mutations in CFH, CFI, CD46, and C3 in patients with atypical hemolytic uremic syndrome. Blood. 2010 ;115:379-87.
24. Poolpol K, Orth-Holler D, Speth C, Zipfel PF, Skerka C, de Cordoba SR, et al. Interaction of Shiga toxin 2 with complement regulators of the factor H protein family. Mol Immunol ;58:77-84.
25. Ozaltin F, Li B, Rauhauser A, An SW, Soylemezoglu O, Gonul, II, et al. DGKE variants cause a glomerular microangiopathy that mimics membranoproliferative GN. J Am Soc Nephrol. 2013 ;24:377-84.
26. Lemaire M, Fremeaux-Bacchi V, Schaefer F, Choi M, Tang WH, Le Quintrec M, et al. Recessive mutations in DGKE cause atypical hemolytic-uremic syndrome. Nat Genet. 2013 ;45:531-6.
27. Bruneau S, Neel M, Roumenina LT, Frimat M, Laurent L, Fremeaux-Bacchi V, et al. Loss of DGKepsilon induces endothelial cell activation and death independently of complement activation. Blood. 2015 ;125:1038-46.
28. Sanchez Chinchilla D, Pinto S, Hoppe B, Adragna M, Lopez L, Justa Roldan ML, et al. Complement mutations in diacylglycerol kinase-epsilon-associated atypical hemolytic uremic syndrome. Clin J Am Soc Nephrol. 2014 ;9:1611-9.
29. Westland R, Bodria M, Carrea A, Lata S, Scolari F, Fremeaux-Bacchi V, et al. Phenotypic expansion of DGKE-associated diseases. J Am Soc Nephrol. 2014 ;25:1408-14.
30. Bu F, Maga T, Meyer NC, Wang K, Thomas CP, Nester CM, et al. Comprehensive genetic analysis of complement and coagulation genes in atypical hemolytic uremic syndrome. J Am Soc Nephrol. 2014 ;25:55-64.
31. Campistol JM, Arias M, Ariceta G, Blasco M, Espinosa L, Espinosa M, et al. Actualización en síndrome hemolítico urémico atípico: diagnóstico y tratamiento. Documento de consenso. Nefrologia. 2015 ;35:421-47.
32. Sellier-Leclerc AL, Fremeaux-Bacchi V, Dragon-Durey MA, Macher MA, Niaudet P, Guest G, et al. Differential impact of complement mutations on clinical characteristics in atypical hemolytic uremic syndrome. J Am Soc Nephrol. 2007 ;18:2392-400.
33. Mele C, Remuzzi G, Noris M. Hemolytic uremic syndrome. Semin Immunopathol. 2014 ;36:399-420
34. Noris M, Remuzzi G. Cardiovascular complications in atypical haemolytic uraemic syndrome. Nat Rev Nephrol. 2014 ;10:174-80.
35. J. FUERTES JLM, A. E. GONZÁLEZ , J. M. OLIVER , J. A. SOBRINO , L. SÁNCHEZ SICILIA , A. TORRE. Miocardiopatía dilatada y síndrome hemolítico urémico. Nefrologia. 1998;18:498-502.
36. Ardissino G, Tel F, Testa S, Marzano AV, Lazzari R, Salardi S, et al. Skin involvement in atypical hemolytic uremic syndrome. Am J Kidney Dis. 2014 ;63:652-5.
37. Le Quintrec M, Zuber J, Moulin B, Kamar N, Jablonski M, Lionet A, et al. Complement genes strongly predict recurrence and graft outcome in adult renal transplant recipients with atypical hemolytic and uremic syndrome. Am J Transplant. 2013 ;13:663-75.
38. Bell WR, Braine HG, Ness PM, Kickler TS. Improved survival in thrombotic thrombocytopenic purpura-hemolytic uremic syndrome. Clinical experience in 108 patients. N Engl J Med. 1991 ;325:398-403.
39. Caprioli J, Noris M, Brioschi S, Pianetti G, Castelletti F, Bettinaglio P, et al. Genetics of HUS: the impact of MCP, CFH, and IF mutations on clinical presentation, response to treatment, and outcome. Blood. 2006 ;108:1267-79.
40. Bresin E, Daina E, Noris M, Castelletti F, Stefanov R, Hill P, et al. Outcome of renal transplantation in patients with non-Shiga toxin-associated hemolytic uremic syndrome: prognostic significance of genetic background. Clin J Am Soc Nephrol. 2006 ;1:88-99.
41. Zuber J, Le Quintrec M, Sberro-Soussan R, Loirat C, Fremeaux-Bacchi V, Legendre C. New insights into postrenal transplant hemolytic uremic syndrome. Nat Rev Nephrol. 2011 ;7:23-35.
42. Ducloux D, Rebibou JM, Semhoun-Ducloux S, Jamali M, Fournier V, Bresson-Vautrin C, et al. Recurrence of hemolytic-uremic syndrome in renal transplant recipients: a meta-analysis. Transplantation. 1998 ;65:1405-7.
43. Cornec-Le Gall E, Delmas Y, De Parscau L, Doucet L, Ogier H, Benoist JF, et al. Adult-onset eculizumab-resistant hemolytic uremic syndrome associated with cobalamin C deficiency. Am J Kidney Dis. 2014 ;63:119-23.
44. Saland JM, Ruggenenti P, Remuzzi G. Liver-kidney transplantation to cure atypical hemolytic uremic syndrome. J Am Soc Nephrol. 2009 ;20:940-9.
45. Saland J. Liver-kidney transplantation to cure atypical HUS: still an option post-eculizumab? Pediatr Nephrol. 2014 ;29:329-32.
46. Coppo R, Bonaudo R, Peruzzi RL, Amore A, Brunati A, Romagnoli R, et al. Liver transplantation for aHUS: still needed in the eculizumab era? Pediatr Nephrol. 2016 ;31:759-68.
47. Loirat C, Fakhouri F, Ariceta G, Besbas N, Bitzan M, Bjerre A, et al. An international consensus approach to the management of atypical hemolytic uremic syndrome in children. Pediatr Nephrol. 2016 ;31:15-39.
48. Hill A, Hillmen P, Richards SJ, Elebute D, Marsh JC, Chan J, et al. Sustained response and long-term safety of eculizumab in paroxysmal nocturnal hemoglobinuria. Blood. 2005 ;106:2559-65.
49. Zuber J, Fakhouri F, Roumenina LT, Loirat C, Fremeaux-Bacchi V. Use of eculizumab for atypical haemolytic uraemic syndrome and C3 glomerulopathies. Nat Rev Nephrol. 2012 ;8:643-57.
50. Legendre CM, Licht C, Muus P, Greenbaum LA, Babu S, Bedrosian C, et al. Terminal complement inhibitor eculizumab in atypical hemolytic-uremic syndrome. N Engl J Med. 2013 ;368:2169-81.
51. Licht C, Greenbaum LA, Muus P, Babu S, Bedrosian CL, Cohen DJ, et al. Efficacy and safety of eculizumab in atypical hemolytic uremic syndrome from 2-year extensions of phase 2 studies. Kidney Int. 2015 ,87;1061-1073
52. Rathbone J, Kaltenthaler E, Richards A, Tappenden P, Bessey A, Cantrell A. A systematic review of eculizumab for atypical haemolytic uraemic syndrome (aHUS). BMJ Open. 2013;3:e003573.
53. Greenbaum LA, Fila M, Ardissino G, et al. Eculizumab is a safe and effective treatment in pediatric patients with atypical hemolytic uremic syndrome. Kidney Int. 2016;89:701-711.
54. Pelicano MB, de Cordoba SR, Diekmann F, Saiz M, Herrero S, Oppenheimer F, et al. Anti-C5 as prophylactic therapy in atypical hemolytic uremic syndrome in living-related kidney transplantation. Transplantation. 2013 ;96:e26-9.
55. Zuber J, Le Quintrec M, Krid S, Bertoye C, Gueutin V, Lahoche A, et al. Eculizumab for atypical hemolytic uremic syndrome recurrence in renal transplantation. Am J Transplant. 2012 ;12:3337-54.
56. Zimmerhackl LB, Hofer J, Cortina G, Mark W, Wurzner R, Jungraithmayr TC, et al. Prophylactic eculizumab after renal transplantation in atypical hemolytic-uremic syndrome. N Engl J Med. 2010 ;362:1746-8.
57. Nester C, Stewart Z, Myers D, Jetton J, Nair R, Reed A, et al. Pre-emptive eculizumab and plasmapheresis for renal transplant in atypical hemolytic uremic syndrome. Clin J Am Soc Nephrol. 2011 ;6:1488-94.
58. Chatelet V, Lobbedez T, Fremeaux-Bacchi V, Ficheux M, Ryckelynck JP, Hurault de Ligny B. Eculizumab: safety and efficacy after 17 months of treatment in a renal transplant patient with recurrent atypical hemolytic-uremic syndrome: case report. Transplant Proc. 2010 ;42:4353-5.
59. Duran CE, Blasco M, Maduell F, Campistol JM. Rescue therapy with eculizumab in a transplant recipient with atypical haemolytic-uraemic syndrome. Clin Kidney J. 2012 ;5:28-30.
60. Al-Akash SI, Almond PS, Savell VH, Jr., Gharaybeh SI, Hogue C. Eculizumab induces long-term remission in recurrent post-transplant HUS associated with C3 gene mutation. Pediatr Nephrol. 2011 ;26:613-9.
61. Nishimura J, Yamamoto M, Hayashi S, Ohyashiki K, Ando K, Brodsky AL, et al. Genetic variants in C5 and poor response to eculizumab. N Engl J Med. 2014 ;370:632-9.
62. Bouts A, Monnens L, Davin JC, Struijk G, Spanjaard L. Insufficient protection by Neisseria meningitidis vaccination alone during eculizumab therapy. Pediatr Nephrol. 2011 ;26:1919-20.
63. Noris M, Galbusera M, Gastoldi S, Macor P, Banterla F, Bresin E, et al. Dynamics of complement activation in aHUS and how to monitor eculizumab therapy. Blood. 2014 ;124:1715-26.
64. Volokhina EB, van de Kar NC, Bergseth G, van der Velden TJ, Westra D, Wetzels JF, et al. Sensitive, reliable and easy-performed laboratory monitoring of eculizumab therapy in atypical hemolytic uremic syndrome. Clin Immunol. 2015 ;160:237-43.
65. Bu F, Meyer NC, Zhang Y, Borsa NG, Thomas C, Nester C, et al. Soluble c5b-9 as a biomarker for complement activation in atypical hemolytic uremic syndrome. Am J Kidney Dis. 2015 ;65:968-9.
66. Ardissino G, Testa S, Possenti I, Tel F, Paglialonga F, Salardi S, et al. Discontinuation of Eculizumab Maintenance Treatment for Atypical Hemolytic Uremic Syndrome: A Report of 10 Cases. Am J Kidney Dis. 2014 ;64:633-637.
67. Wetzels JF, van de Kar NC. Discontinuation of eculizumab maintenance treatment for atypical hemolytic uremic syndrome. Am J Kidney Dis. ;65:342.





